Clear Sky Science · zh
缓殖子亚型主导弓形虫发育的分岔路口
常见寄生虫中的隐匿阶段
弓形虫是一种微小的寄生虫,悄然感染了全球约三分之一的人群,通常受感染者并不自知。但在免疫系统受损的人群——例如接受化疗的癌症患者或艾滋病患者——寄生虫可能从休眠状态中苏醒,导致严重甚至致命的脑疾病。本研究深入探查该休眠阶段,提出了一个简单却关键的问题:所有“睡着”的寄生虫都是一样的吗,还是存在具有不同功能的多种类型?
为什么休眠寄生虫很重要
在长期感染期间,弓形虫藏匿在大脑和肌肉中坚固的微小囊泡内,称为组织囊。每个囊内包含数百个缓殖子——寄生虫的缓慢生长、休眠形式。这些缓殖子构成了维持终身感染的储备,并能在短时间内转换为快速生长的速殖子,导致组织损伤并在体内扩散。由于现有药物无法清除这些囊,弄清楚囊内具体发生了什么,对预防易感患者的再激活至关重要。
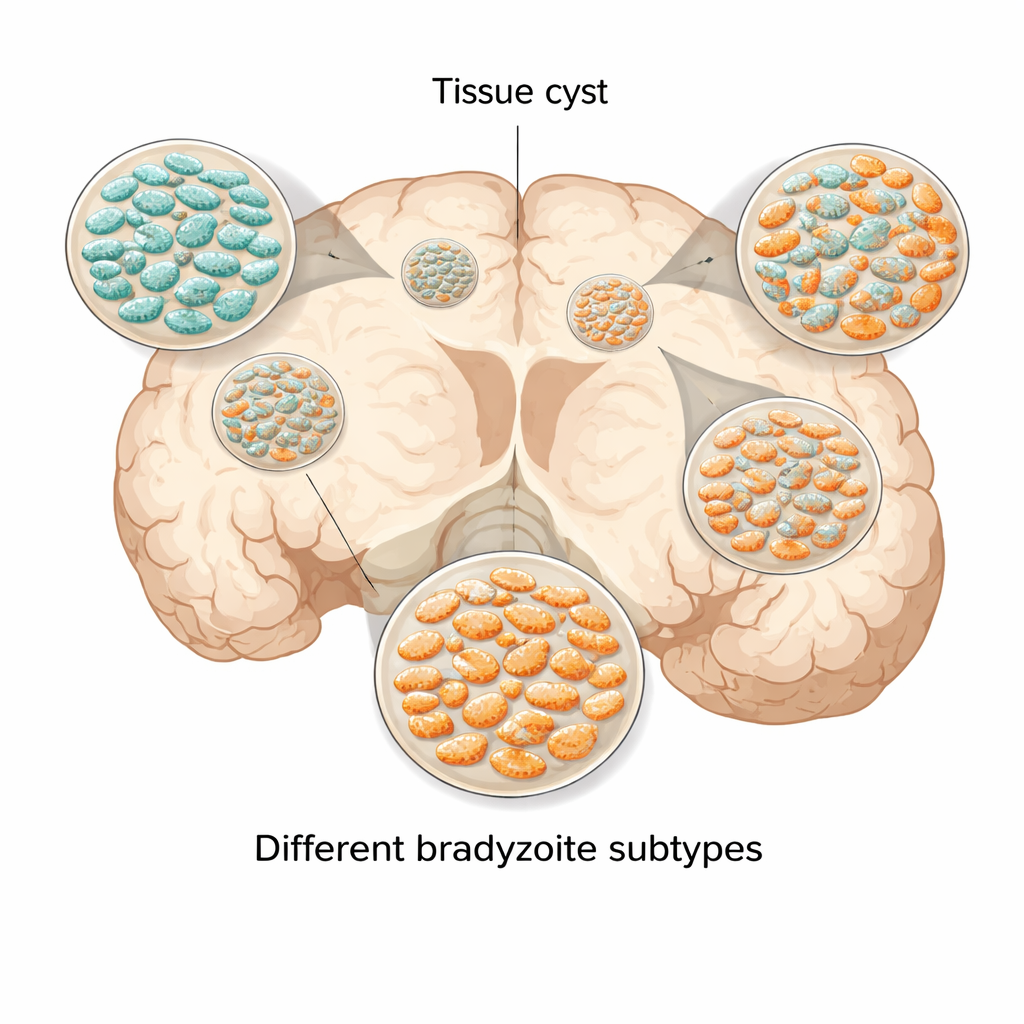
在囊内发现不同“个性”
研究者关注一种名为 SRS22A 的表面分子,该分子存在于小鼠部分缓殖子上,但在标准体外培养的囊中奇怪地缺失。借助专门制备的抗体作为分子“高亮标记”,他们显示小鼠脑内的囊并非均一。有些囊几乎完全由 SRS22A 阳性的寄生虫构成,有些完全缺乏该标记,还有许多囊包含两者混合的情况。这些模式随感染进程而变化,表明囊在生长、破裂和重建的过程中保持着丰富的内部多样性,而非收敛到单一的成熟终点。
两种主要命运:扩散与驻留
为检验这些差异的意义,团队将小鼠大脑中的 SRS22A 阳性和阴性缓殖子分离,并观察每组在体外脑细胞培养和活体小鼠中的行为。SRS22A 阳性寄生虫迅速转化为快速复制的速殖子,能够穿过细胞层并扩散至小鼠器官。在感染早期,携带此类寄生虫的动物体内寄生虫数量更多,并在后期形成更多脑囊。相反,SRS22A 阴性寄生虫倾向于保持缓殖子状态,缓慢增殖并构建新的囊壁。与驱动爆发性扩散不同,这类寄生虫似乎更倾向于默默维持长期储备。
单细胞谱系揭示五个亚型
更精细地看,科学家们使用单细胞 RNA 测序技术,读取数千个单体寄生虫中被激活的基因,这揭示了慢性脑囊内至少五种主要的缓殖子亚型,每种具有独特的基因表达“指纹”。其中一组富含 SRS22A 及其他通常在寄生虫猫期间出现的标记,可能准备在被猫捕食的猎物进入猫体内后恢复性生殖。其它亚型则激活了与侵入工具或囊壁构建相关的基因,暗示有些寄生虫准备突破并侵入新细胞,而另一些则在加固包裹群体的保护外壳。
重塑简单生命周期的认知
综合来看,这些发现推翻了课本中弓形虫从快速速殖子缓慢转为单一、稳定的“休眠”缓殖子阶段的简单图景。相反,每个囊更像一个由各司其职的专科组成的小村落:有些寄生虫随时准备突破并扩散,有些负责通过构建新囊加深慢性感染,还有些可能为进入猫宿主做准备。这种复杂性有助于解释为何只产生部分类型的实验室模型可能无法体现真实感染中的关键行为,也解释了为什么仅靶向某一阶段的药物常常难以治愈疾病。
对患者意味着什么
对于携带弓形虫感染的人而言,该研究传达的信息是:组织中“睡着”的寄生虫并非全然相同。某些亚型似乎是引发危险性爆发的真正引擎,而另一些则维持隐匿的慢性感染或为传播做好准备。通过识别诸如 SRS22A 的表面标记和区分这些亚型的基因模式,研究人员现在有了一条路线图,可用于设计更贴近真实感染的实验模型、疫苗和药物,专门针对最有可能导致严重疾病的形式。长期来看,这可能带来既能控制症状又能防止寄生虫再次苏醒的治疗方法。
引用: Ulu, A., Srivastava, S., Kachour, N. et al. Bradyzoite subtypes rule the crossroads of Toxoplasma development. Nat Commun 17, 1783 (2026). https://doi.org/10.1038/s41467-026-68489-y
关键词: 弓形虫, 缓殖子, 组织囊囊, 寄生虫再激活, 单细胞 RNA 测序