Clear Sky Science · zh
DNA复制网络中的连续可调多稳态
从简单开关到多重可能状态
生物系统——从分裂的细胞到发育中的胚胎——很少像只能开或关的简单灯开关那样运作。相反,它们常常保持许多长时间稳定的状态,更像可以停在无数位置的调光开关。本文报道了一种基于DNA的化学网络,其行为更像这种调光开关:它不仅能稳定维持少数离散状态,而是能够维持沿连续谱的任意组成。这种能力可能成为未来智能材料、分子记忆及处理模拟而非仅数字信息的生化计算机的重要基础。
为何多稳态重要
许多细胞决策——例如干细胞是否分化、细胞是否自毁,或基因网络是否记住过去的信号——依赖于“多稳态”,即在相同条件下能够停留在多于一个的稳定活动模式。传统的合成版本通常由基因电路、酶或相互开启/关闭的DNA链构成。这些设计通常仅产生少数离散结果,比如具有两种长寿命状态的双稳态开关。将该思路扩展更大规模很困难:一个N态系统大致需要 N×(N−1) 个精细调节的抑制连接,而且系统仍只在少数固定点之间跳跃,而不是在平滑的连续可能性范围内变化。
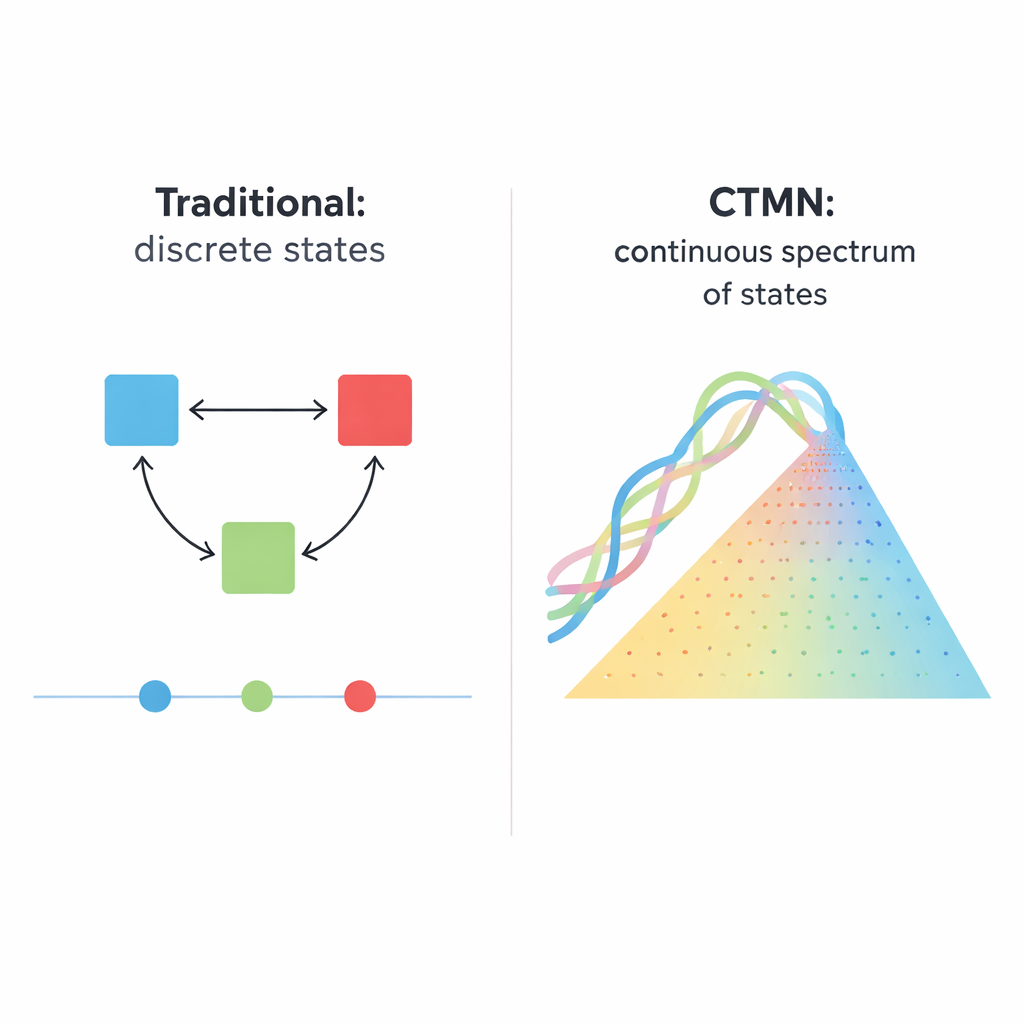
一种新型DNA网络:连续可调
作者提出了不同的设计原则,并在他们称之为连续可调多稳态网络(CTMN)的系统中实现。与依赖许多独立抑制信号的做法不同,他们利用通过可逆链交换反应相连的DNA复制模块之间的直接竞争。每个模块由设计的DNA双链构成,这些双链既能参与链置换,也能作为DNA聚合酶的模板,在切割并再生关键片段的切口酶帮助下发挥作用。化学燃料——称为dNTP的核苷酸构件——驱动持续的聚合和切口反应,使系统远离平衡。在这些条件下,竞争模块有效地“冻结”成其初始相对比例,不仅产生两三种结果,而是产生一条连续的长寿稳态线(或对于更多模块则形成一个平面)。
分子装置如何锁定记忆
在最简单的双模块网络CTMN‑1中,研究团队通过实验和详细的动力学建模表明,系统可稳定地落入一族稳定混合态,几乎覆盖从“主要为模块A”到“主要为模块B”的整个范围。聚合将活性双链转化为暂时从链交换竞争中移除的延伸形式;随后切口再将其还原,闭合一个自我调节回路。当两个模块共享该回路时,它们相互抑制互相转换的能力非常强,使系统在有燃料供应的情况下长时间保持接近初始组成。对底层方程的线性稳定性分析表明存在一个整体流形——实质上的连续稳态集合,这与去除酶或燃料时出现的单一稳定点形成对比。
可编程响应与分子记忆
由于网络的状态储存在DNA组成中,它可以以可编程的方式被引导和读取。作者设计了短RNA“触发物”,能暂时结合特定DNA链以偏向竞争,从而将网络推向新的组成。即便RNA被酶降解,新状态仍能持续存在,充当一种分子记忆。重复或更强的刺激会使系统沿连续状态平滑移动,而不是在简单的开/关位置之间翻转。此外,DNA复制产物本身可以被定制为下游过程的信号:在示例中,CTMN‑1的不同状态能选择性地激活两种DNA催化剂之一,或将RNA转录偏向两种信使链之一,而不破坏底层的多稳态特性。
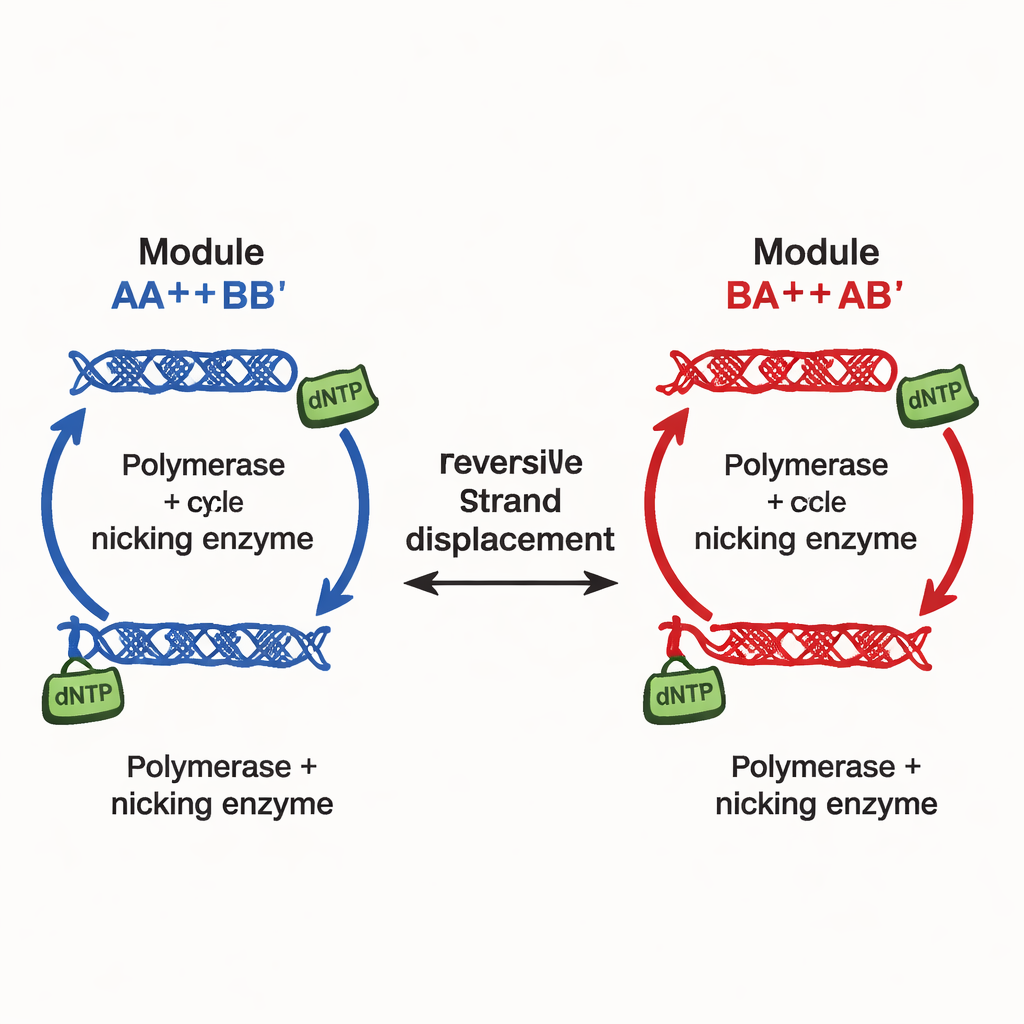
扩展到复杂的分子“调光器”
为了证明该策略具有可扩展性,研究者构建了一个三模块网络CTMN‑2,通过加入更多设计的DNA双链,这些双链共享一个通用的交换域但编码不同的复制模板。现在可能的稳态填满了二维区域,像三角相图中的点分布,而不是简单的一条线。实验再次确认,只要存在燃料和酶,许多不同的组合就是稳定的,而当能量供应被移除时,所有状态都会塌缩到单一的平衡点。因为新增模块只需新的DNA构件插入相同的置换框架,整体连线复杂度不会像传统设计那样急剧增加。
对未来分子技术的意义
对非专业读者而言,核心信息是作者已将DNA复制网络变为一种高度灵活的模拟存储器。与其在少数预设选项中选择,不如该系统能可靠地保持数十种实验上可区分的状态之一,每种状态由各DNA模块的相对含量定义,并能将短暂的化学脉冲转换为沿该连续体的长期位移。由于输出DNA链是可编程的且与稳定机制解耦,该框架原则上可用来以精细的等级控制调节各种下游生化反应或材料特性。因此这项工作指向了更类似于神经或机械模拟系统而非简单数字开关的分子设备,它们能计算、记忆和适应。
引用: Zhong, R., Fu, Y., Jiang, S. et al. Continuously tunable multistability in DNA replication networks. Nat Commun 17, 1782 (2026). https://doi.org/10.1038/s41467-026-68488-z
关键词: DNA 多稳态, 分子记忆, 合成生化网络, DNA 链置换, 模拟分子计算