Clear Sky Science · zh
从空间转录组学数据稳健且可解释地预测基因标记和细胞类型
将常规组织切片转化为分子地图
当进行活检时,医生通常只能通过显微镜看到粉红与紫色染色下的细胞形态与排列。但在这些颜色之下隐藏着基因开关的世界,决定着肿瘤如何生长并如何对治疗作出反应。本研究介绍了STimage,一种新的人工智能(AI)系统,旨在直接从标准病理图像读取该分子“脚本”,有望在无需额外实验检测的情况下提供更快、更廉价的分子见解。
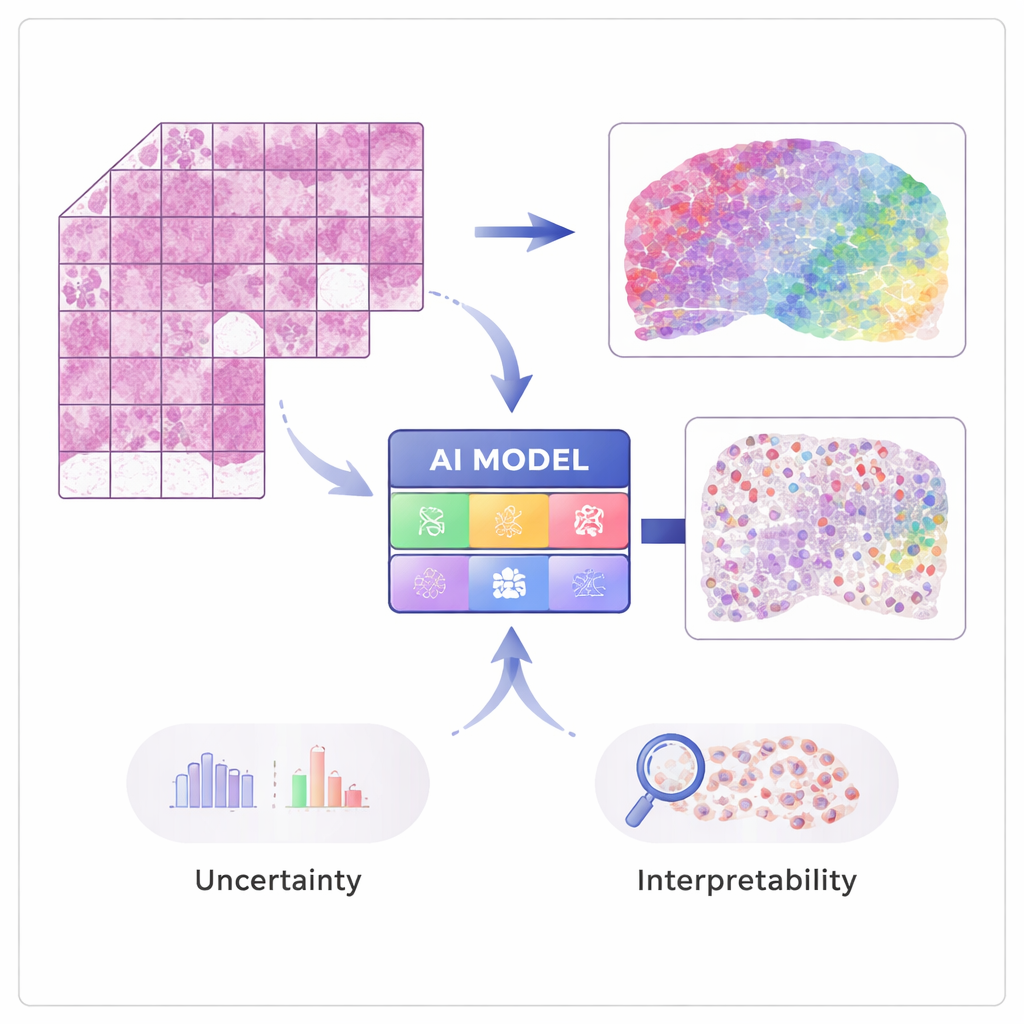
从图像到基因活性
现代“空间转录组学”技术能够在保留信号原位的同时测量成千上万个基因的活性。这些方法功能强大但成本高昂,尚未在医院中普及。STimage 在数量有限的此类空间数据集上进行训练,每个组织图像都与许多微小取点处的详细基因测量相匹配。该AI学习将苏木精-伊红(H&E)切片中的局部视觉模式——例如细胞核的密度或不规则性——与潜在的基因活性关联起来,以便在以后仅凭普通图像预测基因表达和细胞类型。
构建更可信的AI病理学家
这项工作的关键目标不仅是准确性,还包括可靠性和可解释性。STimage 并非仅输出每个基因的单一数值,而是预测完整的概率分布,描述每个位置上基因活性的可能范围。它还区分两类不确定性:一种由噪声或数据变异驱动,另一种反映模型自身的知识缺乏。通过训练多种略有不同的模型并对其取平均——即“集成”方法——研究人员既提高了性能,又更加清晰地识别出系统何处自信、何处不自信,这对临床决策至关重要。
跨癌种、技术与医院的测试
团队在来自乳腺、皮肤和肾脏癌症的多样数据集以及一种免疫相关的肝病数据上评估了 STimage。它学会预测重要的癌症和免疫标志物,常常与独立实验中观察到的真实空间模式相匹配。该模型在面对来自不同实验室、样本制备方法,甚至不同底层技术(包括单细胞分辨率平台和较旧的低分辨率系统)的数据时依然表现稳健。在与若干现有AI工具的直接比较中,STimage 及其集成变体通常表现优异,尤其是在评估预测模式与组织中真实基因活性分布的匹配程度时。
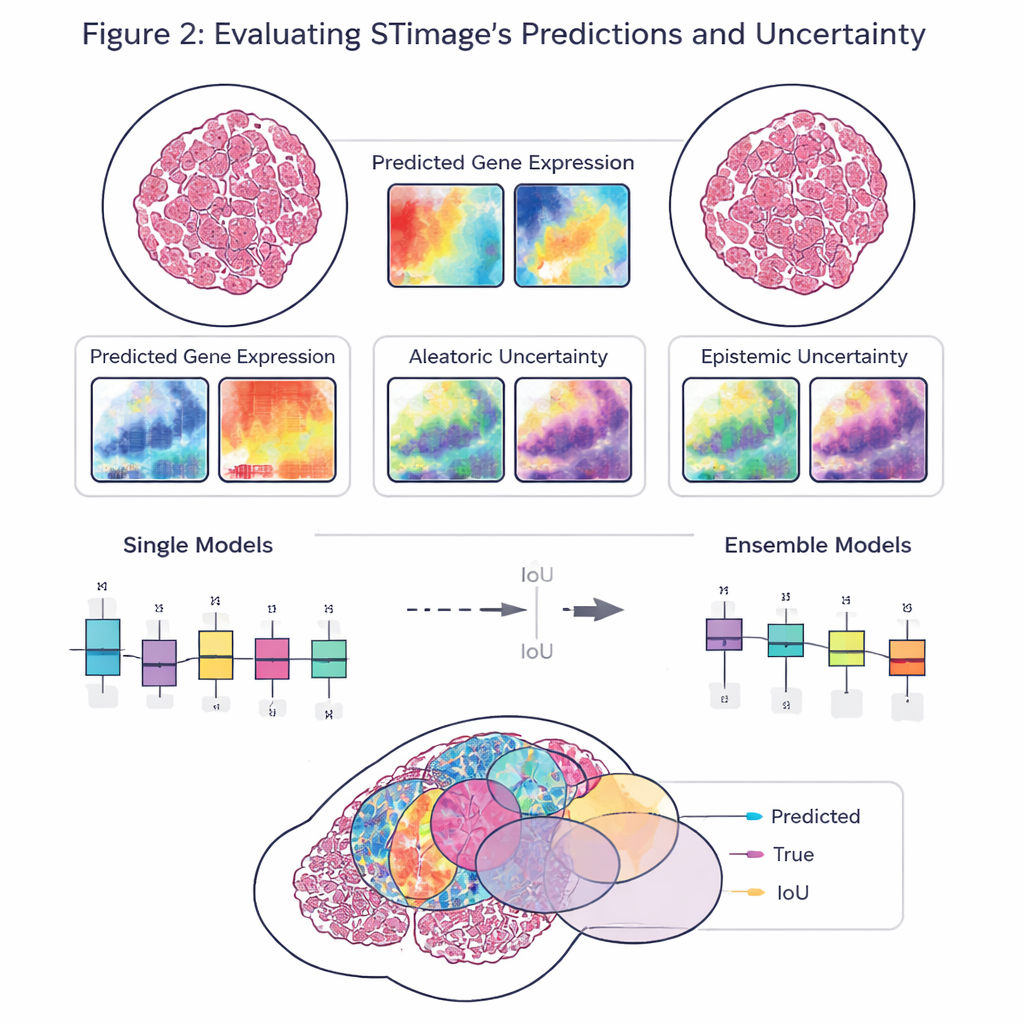
洞察肿瘤内部:细胞、存活与药物反应
STimage 不仅能预测基因,还能推断每个区域占据的细胞类型,使用那些每个细胞身份已知的高分辨率数据集。该模型能够区分癌细胞与免疫细胞及支持细胞,并绘制它们在切片中的排列。作者随后将 STimage 应用于来自癌症基因组图谱(TCGA)的大量常规癌症图像。即使在没有空间测量的情况下,AI 预测的基因谱也与真实的整体基因数据高度一致。这些预测足以将患者分为高风险和低风险组,并有助于区分更有可能对某些乳腺癌疗法产生完全反应的患者。
这对未来患者意味着什么
对患者和临床医生而言,STimage 的前景是为熟悉的病理切片提供一种“分子叠加”。未来,一张扫描的图像或许就能揭示哪些区域存在侵袭性基因程序、免疫细胞如何分布,以及哪些标志物指示更好或更差的预后或不同的药物反应,而无需下多项昂贵检测。尽管该方法仍在优化中,与真实测量的相关性尚不完美,但其捕捉空间模式、估计自身不确定性并突出驱动预测的细胞的能力,使其成为迈向更具信息性、透明化数字病理学的切实一步。
引用: Tan, X., Mulay, O., Xie, J. et al. Robust and interpretable prediction of gene markers and cell types from spatial transcriptomics data. Nat Commun 17, 1781 (2026). https://doi.org/10.1038/s41467-026-68487-0
关键词: 数字病理学, 空间转录组学, 癌症生物标志物, 深度学习, 肿瘤微环境