Clear Sky Science · zh
冷冻电子断层显微镜揭示黄病毒复制、出芽与成熟的耦合
脑部感染性病毒如何劫持细胞膜
黄病毒是一大类病毒,包含导致登革热和蜱媒脑炎的病原体,能够侵入脑组织并引发严重疾病。然而,这些微小病原体如何在细胞内复制自身并组装新的病毒颗粒,长期以来仍多所不明。本研究利用先进的冷冻三维电子成像技术,在接近天然状态下观察蜱媒黄病毒在人体细胞和小鼠脑组织内的活动,揭示了基因组复制、病毒组装与成熟之间出人意料的紧密耦合。
隐藏在细胞膜内的病毒工厂
黄病毒复制时并非简单地在细胞内自由漂浮。它们重塑一种称为内质网(ER)的细胞膜系统,形成称为复制器官(replication organelles)的专门囊室。这些囊室看起来像内质网表面的微小向内芽泡,作为受保护的腔室用于复制病毒RNA基因组。研究者利用冷冻电子断层技术——一种能产生细胞近原生状态三维快照的手段——在被一种与蜱媒脑炎病毒相关的蜱媒黄病毒感染的人肺细胞中可视化了这些芽泡。他们发现,被感染区域周围的内质网膨胀并充斥着这些复制器官的簇状结构,有的空旷,有的则充满致密的、线状的RNA。
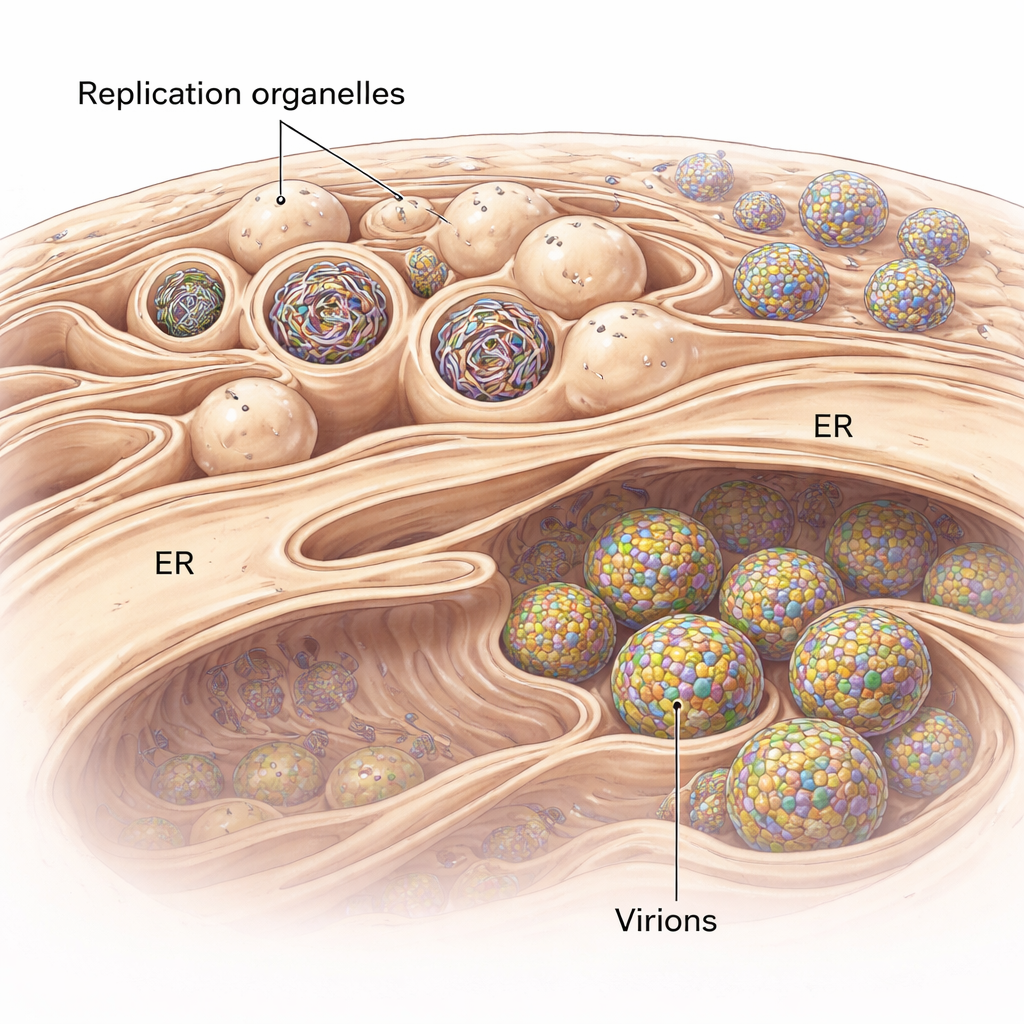
构建“完美病毒泡泡”
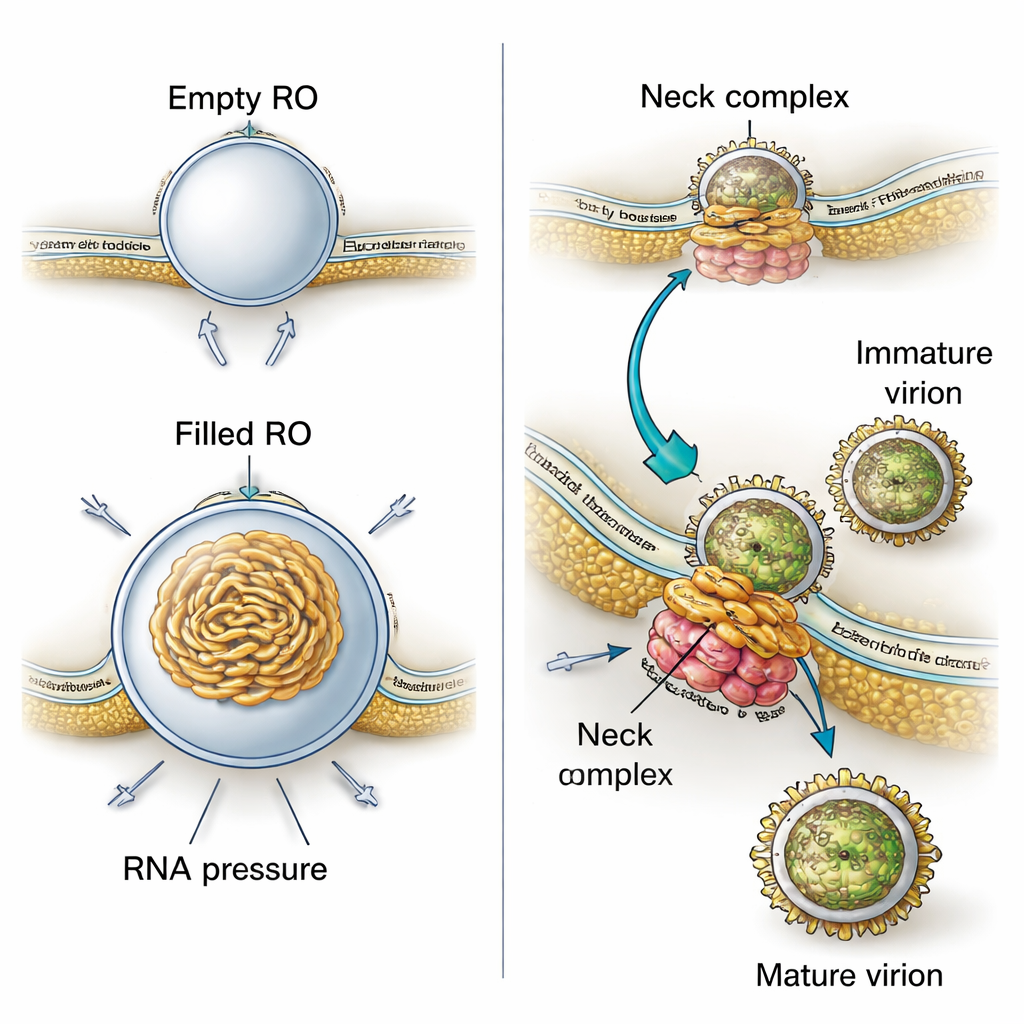
为何这些膜囊呈现出如此精确的芽状形态?通过将三维影像与物理建模结合,作者展示了两种力共同起作用。首先,复制器官的膜比正常内质网持续更厚,这表明病毒蛋白或改变的脂质使膜变得更硬并产生曲率,从而在任何RNA进入之前就把膜塑造成稳定的芽泡。其次,当病毒RNA存在时,它在囊室内盘绕并向外推挤,增大芽泡的体积。根据测得的尺寸进行的计算表明,每个充满物的器官很可能承受着相当于大约一份双链形式病毒基因组的压力。这意味着病毒既利用预成形的膜结构,也利用其遗传物质的物理推力来建造并稳定其微型工厂。
装配线:从基因组复制到新病毒
该研究还揭示了病毒生成与这些复制位点之间的密切联系。在三维观测中,研究者经常看到新的病毒颗粒就在复制器官旁形成,向相邻的类内质网空间出芽。未成熟的颗粒表面带有刺状突起,而较成熟的颗粒则显得光滑。断层图中测得的距离显示,未成熟颗粒位于比成熟颗粒更接近复制器官的位置,这暗示随着颗粒在交织的膜隔室中仅短距离移动,它们就经历了向具有感染性的结构改变。每个复制芽与细胞质相连处狭窄“颈部”上有一个大型蛋白复合体,似乎将复制器官系连到相邻发生出芽的膜上。该复合体很可能充当分子拉链,协调RNA的产生与将该RNA封装进新病毒颗粒的过程。
通过单个氨基酸微调成熟
为探究病毒成熟的调控机制,团队比较了两种嵌合病毒株,它们在宿主酶furin识别位点上仅有一个氨基酸的差异。该酶切割一种病毒表面蛋白,帮助将未成熟的刺状颗粒转变为光滑的成熟颗粒。在试管中进行的切割测定和感染细胞中,位点为精氨酸(arginine)的变体比位点为谷氨酰胺(glutamine)的变体被切割得更快。在通过冷冻电子断层在细胞中可视化时,切割更快的病毒在复制器官附近产生了更高比例的成熟颗粒。尽管在显微结构上存在这些差异,但在小鼠模型中两种变体表现出相似的生长和致病模式,这表明病毒在仍保持传染性的同时可以容忍一定范围的成熟效率变动。
在大脑中直接观察感染过程
大多数病毒结构学研究依赖细胞系,但这项工作延伸到了活组织。研究者从感染小鼠中分离出一种称为脉络丛的脑结构,并使用高压冷冻与聚焦离子束铣削制备用于冷冻电子断层。即便在这一复杂环境中,他们也观察到了相同的典型特征:复制器官簇、增厚的膜以及附近充满成熟病毒颗粒的囊泡。这表明在培养细胞中观察到的膜重塑与高度耦合的复制—组装—成熟序列,也在这些病毒致病的大脑中发挥作用。
为何这些隐秘流程重要
对非专业读者而言,核心信息是:这些侵袭大脑的病毒在我们细胞内运行着高度有序的装配线。它们将细胞膜雕塑成微小加压的囊室用于基因组复制,将这些囊室直接连接到新颗粒出芽的位点,甚至在离原始复制位点仅几步之遥处就开始最终的成熟步骤。鉴别出增厚的复制膜、跨颈部的蛋白复合体以及紧密交织的成熟隔室,不仅解释了黄病毒为何能高效复制,还为设计破坏病毒隐藏工厂与装配轨道的抗病毒药物指明了新的靶点。
引用: Dahmane, S., Schexnaydre, E., Zhang, J. et al. Cryo-electron tomography reveals coupled flavivirus replication, budding and maturation. Nat Commun 17, 828 (2026). https://doi.org/10.1038/s41467-026-68483-4
关键词: 黄病毒, 冷冻电子断层显微镜, 复制器官elles, 病毒成熟, 蜱媒脑炎