Clear Sky Science · zh
基于光谱电化学的铜钴催化剂对CO2与亚硝酸盐共同电催化合成尿素的机理洞见
把废气变成肥料
尿素肥料是现代农业的基础,但传统的生产方式耗能大且碳排放高。本文探索了一种截然不同的路径:用电力将二氧化碳(CO2)和含氮废弃物(例如来自排放或废水的亚硝酸盐)直接转化为尿素。对普通读者而言,这一思路的吸引力显而易见:一条可减少排放、利用废物流作为原料,并可以由可再生电力驱动的必需肥料生产路线。
为什么要重新思考尿素的制备方式?
如今,尿素大多通过先用氮气和化石能源来源的氢气制备氨(哈伯—博世工艺),再在高温高压下将氨与CO2反应制得。这个反应链高度集中、资本密集,且每生产一吨尿素就排放近一吨CO2。随着全球肥料需求增长,环境代价也随之增加。一种替代方案是完全绕过化石燃料,用电力——最好是可再生电力——驱动关键化学步骤,并利用目前被视为废物的CO2和氮氧化物(NOx)作为原料。
铜与钴的新角色
作者制备了通过共溅射将铜(Cu)与钴(Co)薄膜沉积到碳纸上的催化剂,并精细调控Cu:Co比例。他们聚焦于在中性pH水溶液中同时对CO2和亚硝酸盐(NO2⁻)进行电化学还原,这一条件有利于形成制造尿素所需的碳—氮(C–N)键。表现最好的组成是1:1的Cu–Co混合物,在适度施加电压下,催化剂的尿素产率约为每克催化剂每小时61毫摩尔。显微镜和X射线测量显示金属在原子尺度上混合紧密,并在运行过程中大部分保持金属态,为CO2和亚硝酸盐的高效反应提供了稳健的平台。 
催化剂如何分工协作
用这种方法制备尿素具有挑战性,因为更简单的反应——如析氢或单独还原CO2或亚硝酸盐——会强烈竞争。研究者发现关键在于铜位点与钴位点之间的“分工协作”。电化学测试表明,单独的铜主要把CO2还原成含碳燃料和化学品,而单独的钴主要把亚硝酸盐还原为氨,二者均不产尿素。只有当Cu与Co原子紧密混合时,才观察到显著的尿素生成。反应中采集的光谱“快照”检测到表面键合的特征碎片:来自CO2的碳物种(*CO 和 *COOH)更倾向于结合在铜上,而来自亚硝酸盐的含氮物种(*NH2 及相关基团)更倾向于结合在钴上。在Cu与Co的边界处,这些碎片可以相遇并偶联,形成尿素的C–N骨架。
为键合找到合适的条件
研究显示,仅靠成分还不够;周围的电解液和膜也必须调控到位。尿素仅在中性碳酸氢盐电解质中出现,该环境既保持足够的溶解CO2可用,又提供恰到好处的质子(氢离子)以驱动“质子耦合电子转移”步骤,而不会使表面被过量的析氢反应淹没。在强酸性或强碱性条件下,尿素要么无法形成,要么很快分解为更简单的产物。使用不同氮源的实验表明,亚硝酸盐对尿素形成尤为有效,优于硝酸盐和羟胺。长时间的测试表明,Cu–Co薄膜相对稳定,仅有适度的金属损失并能维持尿素产出。
用理论窥探催化机理
为理解为什么这种串联催化剂能如此有效,研究团队借助基于密度泛函理论的计算机模拟。这些计算支持了铜更容易结合CO2衍生物,而钴更易活化亚硝酸盐并稳定含氮碎片的观点。模拟指出一个特定步骤是能垒瓶颈:将来自亚硝酸盐的*NH2 碎片与来自CO2的*COOH 碎片偶联,形成一个中间体通常写作 *NH2CO。一旦该中间体形成,后续通往尿素的步骤相对容易。与纯铜或纯钴相比,Cu–Co界面降低了这一关键偶联步骤的能量代价,解释了实验上双金属体系尿素产率提高的现象。 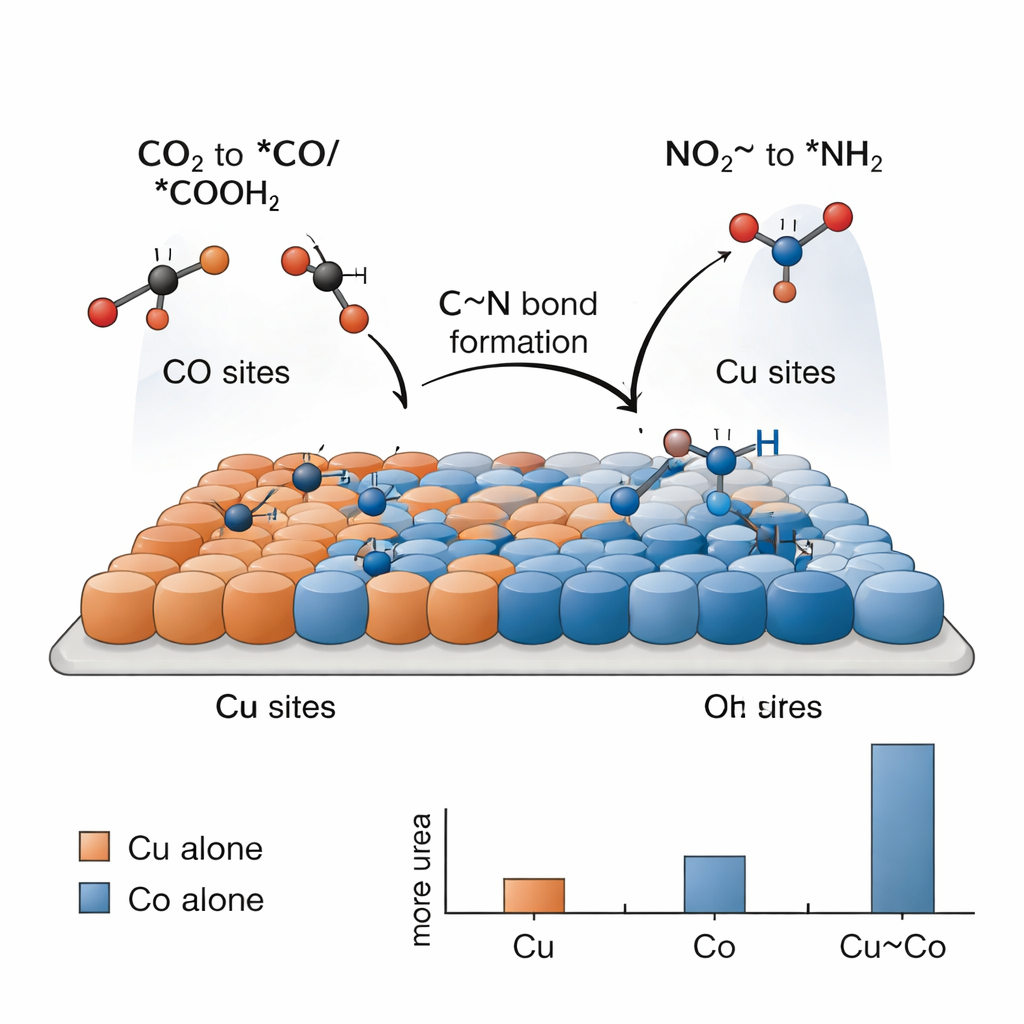
从实验室洞见走向更绿色的肥料
在实际层面上,这项工作尚不足以取代现有的大型尿素工厂,但它阐明了未来电化学路线如何设计。通过展示铜与钴可以协同工作——一个提供活化的碳物种,另一个提供活化的氮物种,并在精细控制的质子条件下共同作用——该研究为面向更清洁、可能去中心化的尿素生产描绘出一条现实可行的路径,使CO2和氮废物流成为资源而非污染物。
引用: Ramadhany, P., Trần-Phú, T., Yuwono, J.A. et al. Spectroelectrochemical insight into copper cobalt catalysts for CO2 and nitrite co-electroreduction to urea. Nat Commun 17, 1776 (2026). https://doi.org/10.1038/s41467-026-68481-6
关键词: 电化学合成尿素, 铜钴催化剂, CO2 利用, 亚硝酸盐还原, C–N 键偶联