Clear Sky Science · zh
选择性抑制人类 GABA 转运蛋白 GAT3 的结构基础
为何抑制性信号至关重要
大脑依赖兴奋信号与抑制信号之间的微妙平衡。GABA 是一种关键的抑制性递质,有助于防止与癫痫、中风损伤和阿尔茨海默病等疾病相关的失控活动。本研究聚焦于一种名为 GAT3 的蛋白,它负责清除神经细胞周围的 GABA。通过以原子级别揭示一种新分子如何结合并关闭 GAT3,研究人员提供了一条结构学路线图,可用于设计下一代药物,温和地增强大脑的天然“刹车”机制。
大脑自身的刹车踏板
GABA 是中枢神经系统中主要的抑制性(或“平静”)神经递质。GABA 从神经末梢释放后必须迅速被清除,以便大脑回路能重置。负责这一清除的,是将 GABA 泵回细胞内的转运蛋白。大脑中以两种转运蛋白为主:主要位于神经元上的 GAT1,以及位于支持细胞(星形胶质细胞)上的 GAT3。尽管一种阻断 GAT1 的药物(替加宾)数十年来一直用于治疗癫痫,但针对 GAT3 的类似药物发展较慢。GAT3 特别值得关注,因为它控制突触外的 GABA 水平,并塑造持久的、背景性的抑制,从而对大脑活动进行精细调节。 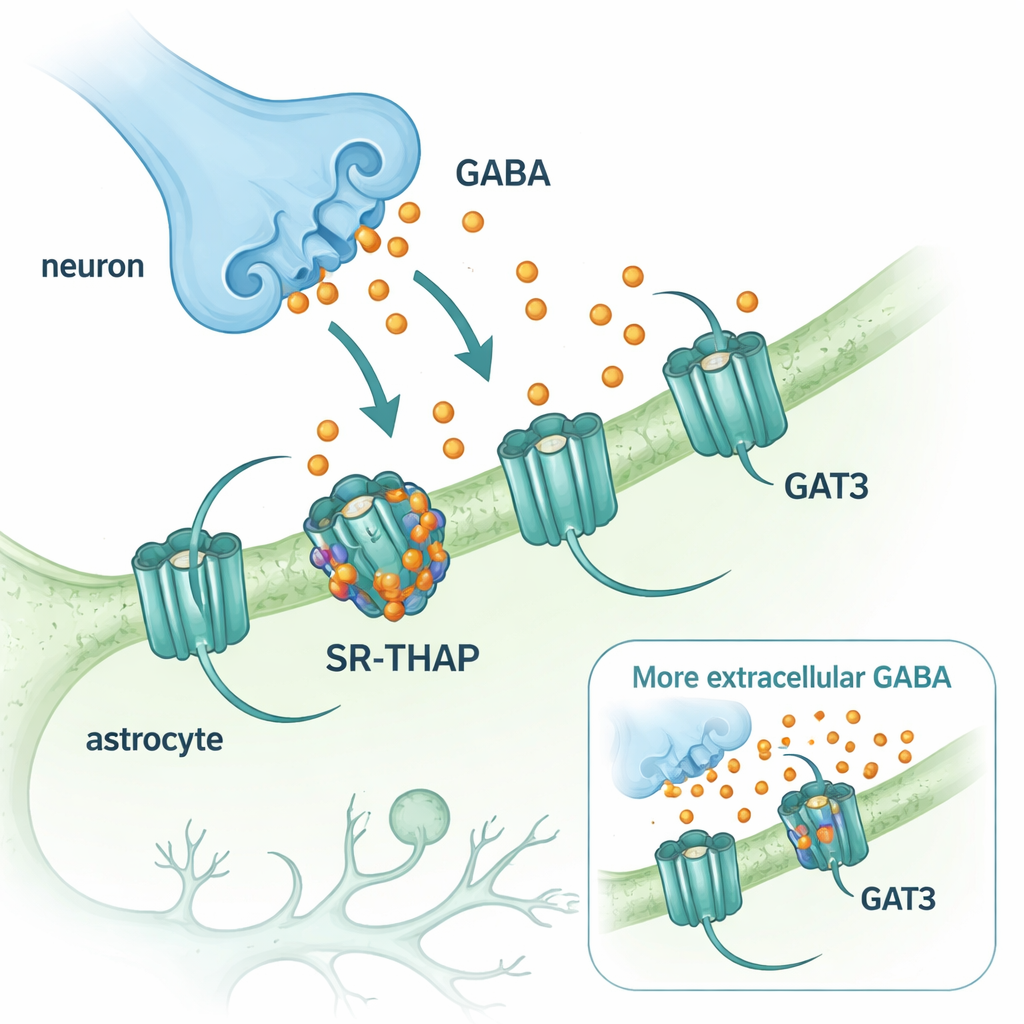
设计更精确的分子“锁”
抑制 GAT3 的尝试一直受限于缺乏详细的结构信息。过去许多化合物是通过反复试验而来的,通常是对已知的类似 GABA 的分子进行体积增大的改造。已知效果较好的一种化合物 (S)-SNAP-5114,证明在化学上不稳定且难以在活体动物中使用。研究者基于这一类更稳定的类似物,开发出 SR-THAP,一种旨在更贴合 GAT3 且更耐降解的小分子。在人体细胞培养实验中,SR-THAP 强效阻断 GAT3,并以非竞争性方式起作用:它并非简单地与 GABA 在常规位点竞争,而是改变转运蛋白的工作方式,降低其最大运输能力。
以近原子分辨率观测 GAT3
为确切理解 SR-THAP 的作用机制,团队使用了冷冻电子显微镜,这是一种用电子成像快速冷冻蛋白并重建其三维形态的技术。他们解析了三种人类 GAT3 的构象:与 SR-THAP 结合、与 GABA 结合、以及无底物状态。三者都显示了与相关神经递质转运蛋白相似的典型结构:跨膜的 12 根密集排列的螺旋,形成 GABA 及其伴随离子(钠和氯)通过的中轴通道。在与 GABA 结合的结构中,转运蛋白处于“向内闭合”状态——GABA 和一枚钠离子被夹在中间,既与外界也与细胞内侧封闭。一种关键的芳香族氨基酸与 GABA 的氨基形成了专门的相互作用,有助于解释 GAT3 如何识别其底物。
SR-THAP 如何楔入并开启转运蛋白
形成鲜明对比的是,SR-THAP 结合的结构捕捉到 GAT3 的“向内开放”状态,蛋白的内侧朝向细胞内部张开。SR-THAP 深嵌在这一内腔中,楔入通常在运输周期中移动的几根螺旋之间。它占据了三个具有不同化学性质的小口袋,与一系列氢键和疏水接触相互作用。这一位置有效地卡住了转运蛋白,使 GABA 和离子无法完成它们的运输路径。作者展示了一些位于此腔内的特定氨基酸在 GAT3 与其近亲之间存在差异;替换其中某些残基会改变运输活性和 SR-THAP 的效力,帮助解释该抑制剂为何对 GAT3 的选择性远高于对 GAT1 或相关转运蛋白。
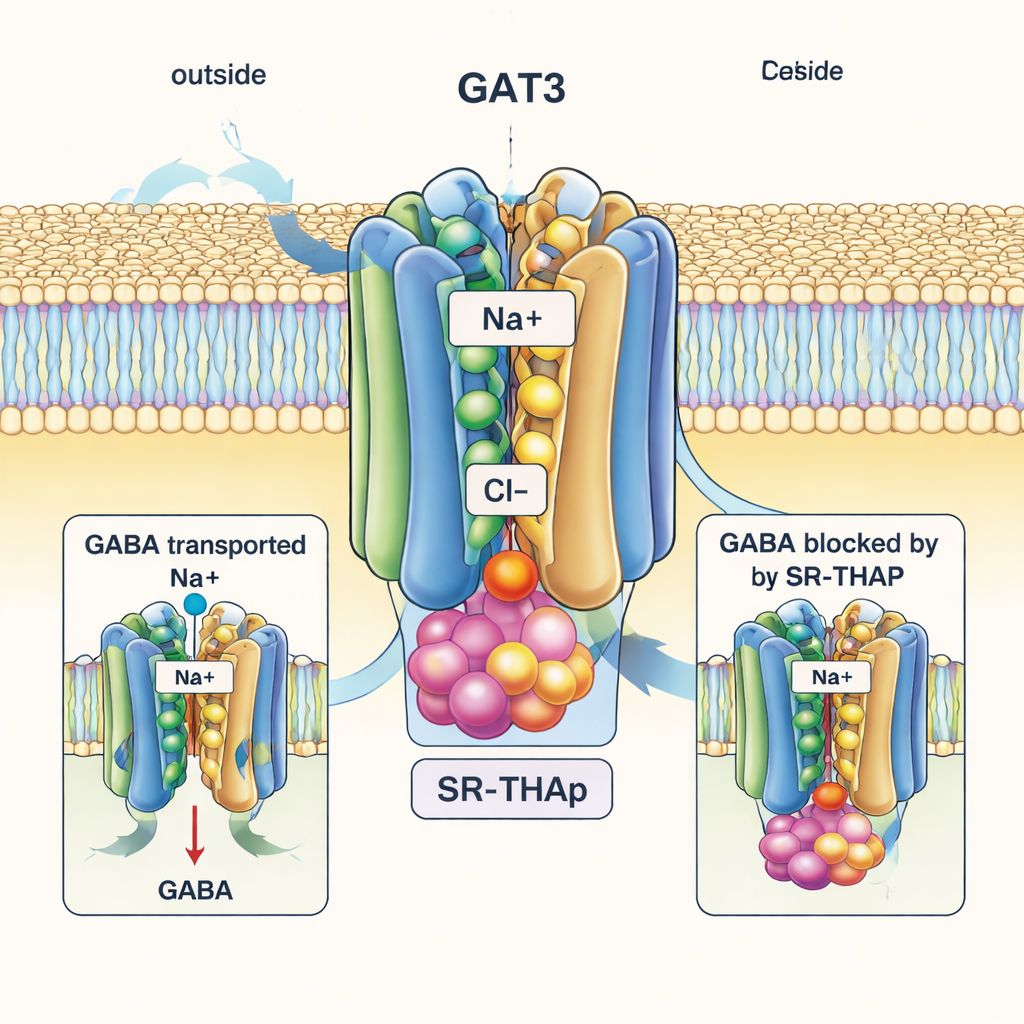
为新型癫痫和脑健康药物打开大门
这些结构共同揭示了 GAT3 在移动 GABA 时如何在不同形态间循环,以及 SR-THAP 如何利用一个较少保守的内腔来冻结该循环。对非专业读者来说,关键要点是:这项研究提供了关闭 GAT3 的详细分子蓝图,并具有高度选择性。此类化合物可更精细地提升抑制性 GABA 水平,相较现有药物可能带来新的治疗方法或研究工具,用于癫痫、中风康复、阿尔茨海默病及其他抑制信号受扰动的疾病。
引用: Mortensen, J.S., Bavo, F., Jensen, M.H. et al. Structural basis for selective inhibition of human GABA transporter GAT3. Nat Commun 17, 1774 (2026). https://doi.org/10.1038/s41467-026-68479-0
关键词: GABA 转运蛋白, GAT3, 癫痫, 低温电子显微镜, 神经递质抑制