Clear Sky Science · zh
一种随机机制驱动AAA+机器ClpB中快速底物转位
细胞机器如何维持蛋白质运动
在每个细胞内,微小的分子机器持续拉扯、牵引并重塑蛋白质,以防止它们聚集并修复损伤。其中一种叫做ClpB的机器能帮助拯救纠缠的蛋白质——这一工作在细胞应激条件下对生存至关重要。本研究提出一个简单但深刻的问题:ClpB如何将化学燃料ATP转化为将蛋白链牵引通过中心孔的机械功?它是以整齐有序、像时钟一样的步进方式进行,还是以更随机、扩散式的方式工作?
工作的蛋白质救援环
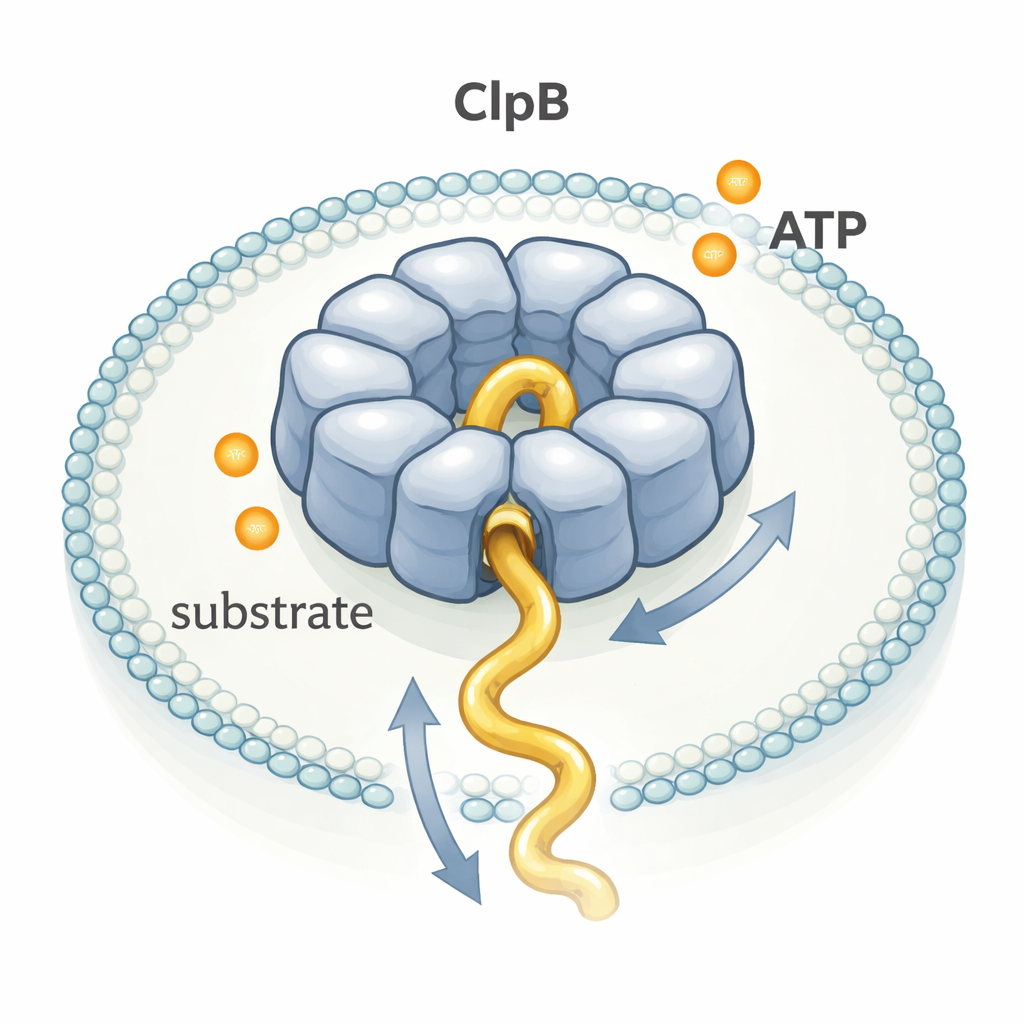
ClpB属于一个被称为AAA+的酶大家族,能组装成具有中心通道的环形结构。许多成员已通过冷冻电子显微镜被描绘出极为精细的结构,从而催生了一种流行的“手递手”模型:每水解一分子ATP就驱动一个小而精确的步进,就像一队人依次拉动绳子。然而,其他实验提示ClpB移动蛋白的速度可能远高于其缓慢ATP消耗率所能解释的速度。为了解开这一矛盾,作者实时观察了单个ClpB分子将一条柔性的测试蛋白κ-酪蛋白通过其孔道的过程。
逐个分子地观察
研究者将单个ClpB环和单条κ-酪蛋白一同困在贴附于玻璃表面的微小脂质囊泡内。他们在ClpB和蛋白链的特定位点连接了荧光染料,然后使用单分子FRET,这是一种报告纳米尺度距离变化的技术。当κ-酪蛋白滑入ClpB孔中时,染料靠近,FRET突然升高呈短暂尖峰;当链离开时,信号又下降。通过测量数千个此类尖峰的持续时间和高度,他们推断出蛋白链段穿过孔道的速度和距离。
快速、低燃料驱动且几乎不受温度影响
出人意料的是,转位事件极其快速:标记的κ-酪蛋白片段通常在约1–2毫秒内穿过孔道数纳米——大约比ClpB平均ATP水解事件之间的时间快一千倍。大多数事件如此短暂,且呈宽广的幂律分布,而非单一特征时间尺度。将温度从10°C改变到32°C几乎不减慢这些运动,表明与经典“动力冲程”马达(如驱动蛋白质的动力蛋白)相比,运动的能量势垒非常小。同样,降低ATP浓度大幅减少事件发生的频率,但对每次事件的持续时间几乎没有影响。换言之,ATP更多地控制ClpB何时参与以及它多频繁行动,而不是单次穿插突发的速度。
往返运动带有向前偏置
为了判断蛋白链是否总是单向移动,团队进行了更复杂的三色FRET实验,分别将染料标记在孔的两端和底物上。这使他们能够区分κ-酪蛋白是从环的上方还是下方进入,以及它是完全通过还是中途退回。他们发现了六种不同的模式:完整的向前和向后穿过、更长的“部分”访问(链在离开前在孔两端都进行取样)以及只在某一端发生的短暂接触。大约四分之三的完整事件是向前的,但相当一部分事件是向后的,表明ClpB允许底物进行双向扩散,仅具有温和的向前偏置。当ATP被一种慢速水解的类似物替换时,事件变得稀少且明显变慢,且向前偏好基本消失。
布朗式马达,而非简单绞车
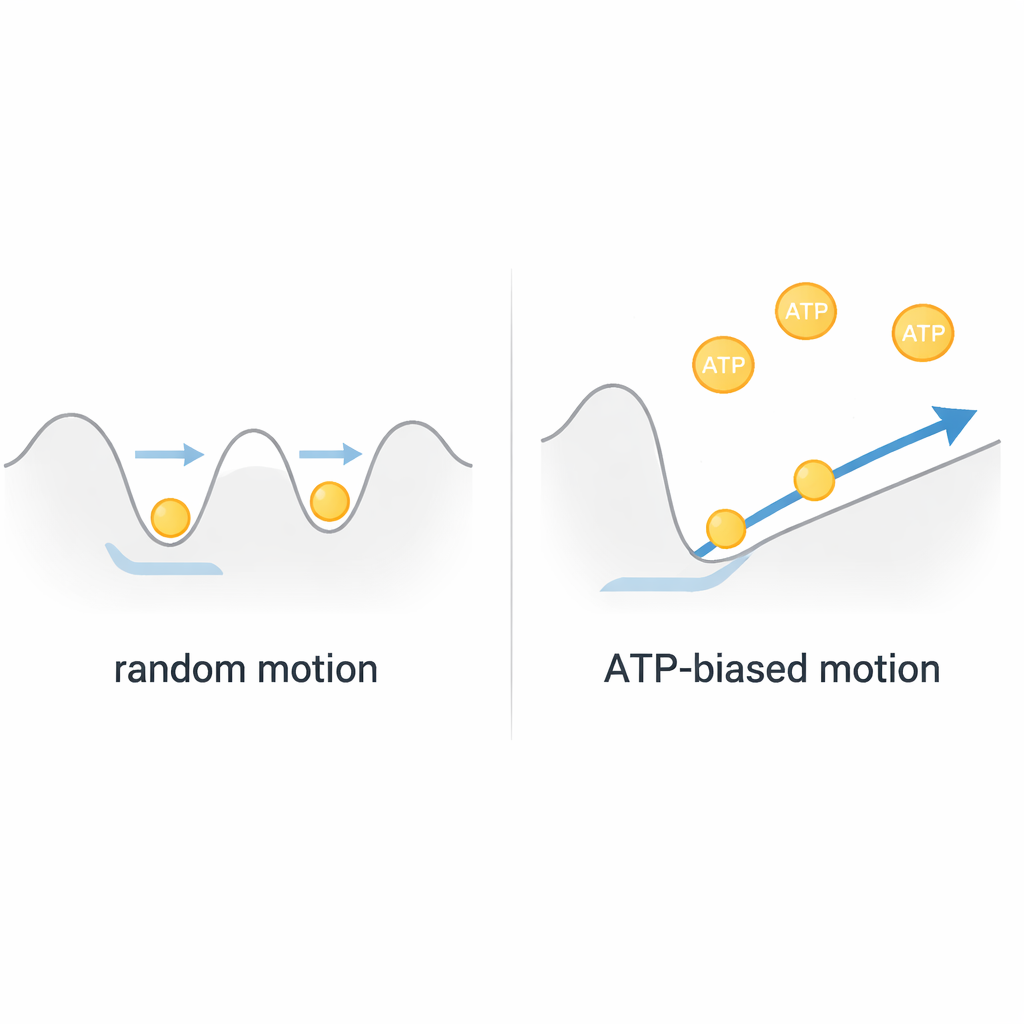
将这些观察结果组合起来,作者得出结论:ClpB更像一个布朗式马达,而不是一个刚性的、燃料驱动的绞车。蛋白链在孔内于浅能量景观中热学抖动,以高速来回运动。ATP并不直接驱动大幅、离散的牵拉冲程;相反,它通过孔环内“孔环(loop)”的快速运动调节该能量景观的形状,微妙地偏向一个方向。因为每次完整的穿插事件仅与大约一到两个ATP分子的消耗相关,ClpB通过整流随机运动而不是与之对抗,从而实现高度高效且快速的运输。这一观点改写了我们对许多AAA+机器的理解,提示生物纳米马达往往可能利用随机性而非消除它。
引用: Casier, R., Levy, D., Riven, I. et al. A stochastic mechanism drives fast substrate translocation in the AAA+ machine ClpB. Nat Commun 17, 1773 (2026). https://doi.org/10.1038/s41467-026-68478-1
关键词: 蛋白质转位, AAA+ 机器, 布朗马达, 分子伴侣, 单分子FRET