Clear Sky Science · zh
人类小电导钙激活钾通道 SK2 的抑制与激活的结构机制
为何微小的钾通道很重要
你的每一次思考与每一次心跳都依赖于细胞内的电信号。这些信号由微观孔道(称为离子通道)调节,允许带电原子流入或流出。小电导钙激活钾通道(SK 通道)家族就是其中一类,参与控制神经元放电频率和心脏节律。本文以原子级细节揭示了不同药物与一种蜜蜂毒素如何关闭或增强该家族的一个关键成员——人类 SK2 通道——这些见解可为治疗从房颤到震颤和记忆障碍等疾病提供指导。
SK2 通道如何作为细胞的制动装置
SK2 通道嵌于细胞膜中,充当电活动的微小制动器。当细胞在电信号期间短暂充满钙离子时,一个称为钙调蛋白(calmodulin)的辅助蛋白感知到钙浓度升高。钙调蛋白附着在 SK2 的内侧,当其结合钙后,会像拉绳一样牵动通道的一部分,打开允许钾离子流出的门。这种向外的钾流有助于在细胞放电后使其恢复静息,从而影响神经元发送信号的频率以及心肌细胞跳动的可靠性。因为 SK1–3 在大脑与心脏广泛存在,且 SK2 是特别重要的亚型,精确理解它们如何开关并如何响应药物,对于设计更精确的药物至关重要。
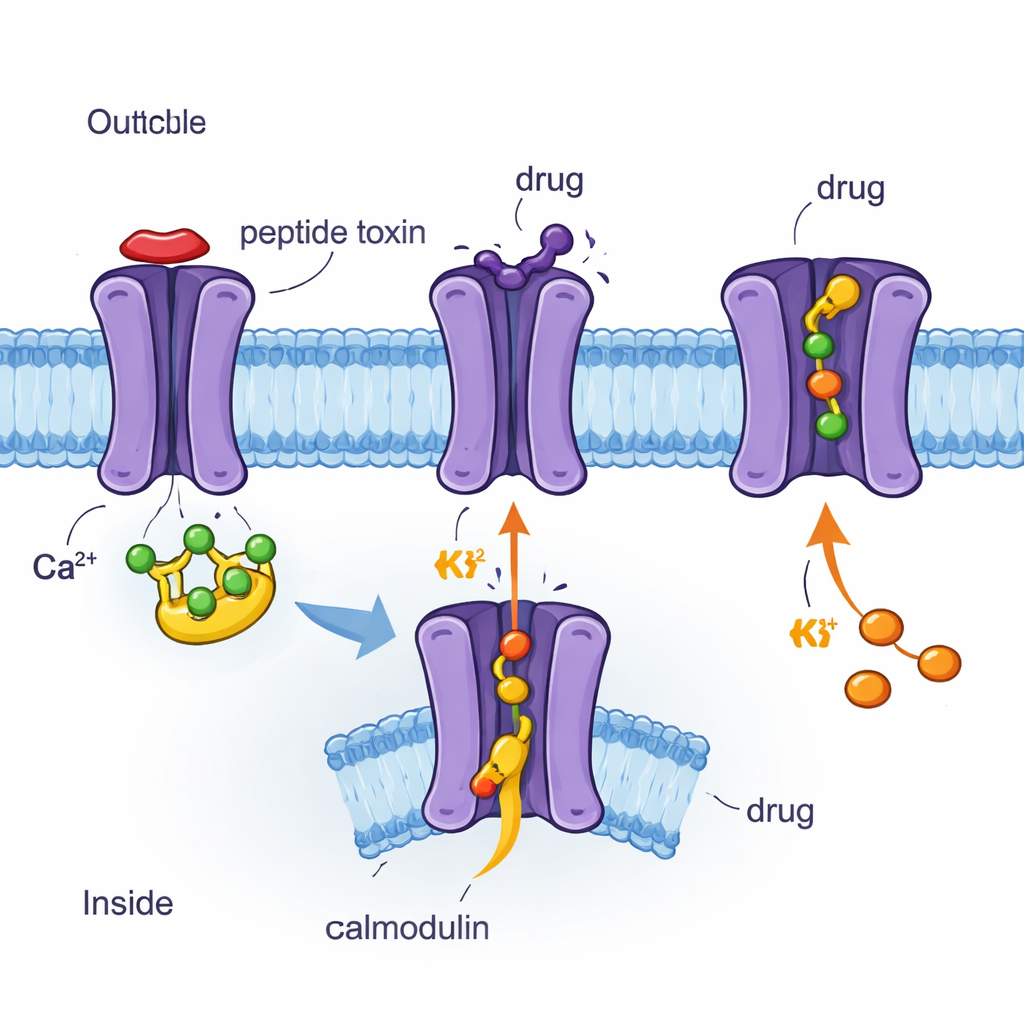
用冷冻电镜逐原子观察通道与药物
作者使用冷冻电镜(cryo‑EM)——一种能在近原子分辨率下成像速冻蛋白的技术——确定了四种人类 SK2 通道与钙调蛋白及不同分子结合的三维结构。这些配体包括蜜蜂毒肽 apamin、合成阻断剂 UCL1684、临床抑制剂 AP30663 以及临床激活剂 CAD‑1883。所有四种结构均显示 SK2 为一个跨膜的四聚体,钙调蛋白附着在内侧。比较这些“快照”揭示了通道哪些部位是刚性的、哪些是柔性的,以及在闭合或开放状态下钙调蛋白如何移动。研究者还将这些结构与细胞电生理测量结合,测试特定氨基酸突变如何改变通道对各个化合物的反应。
封堵外部通道口的蜜蜂毒素与实验室合成药
Apamin 是来自蜂毒的小肽,长期以来被用作研究中极其有效且选择性的 SK2 阻断剂。新结构显示 apamin 像软木塞一样结合在 SK2 孔的外部通道口。它嵌入由两个螺旋之间的一段短环(S3–S4 链接)形成的杯状前室,该区域在 SK2 中被良好组织,而在相关通道 SK4 中较为松散,这解释了 SK4 对 apamin 不敏感的原因。apamin 上带正电的关键残基伸入通道的四个芳香族侧链之间,形成强烈的静电与堆积相互作用,完全封闭了钾离子通路。合成的双喹啉化合物 UCL1684 基本占据相同的外部口袋并阻断离子出口,但其较小的体积使其能坐得更深,模拟 apamin 中关键正电位点的位置。改变塑造该前室的通道残基会显著降低对 apamin 的敏感性,对 UCL1684 的影响则较小,证实了这个特定外环是毒素与药物作用的主要决定因素。
中央塞子与内部楔块如何微调活性
相反,临床候选药 AP30663 结合于 SK2 的中央空腔内,位于选择性滤器(负责识别钾离子)下方。在那里它充当一个物理塞子,楔入在排列于孔内的特定侧链之间。对这些侧链的改变削弱了 AP30663 抑制 SK2 的能力,序列比较也解释了其近亲为何能区分 SK1–3 与 SK4。用于运动障碍的正向调节剂 CAD‑1883 则采用另一种策略:它滑入位于钙调蛋白 N 叶与将钙调蛋白运动耦合到通道门的短链接(S4–S5)之间的接口的口袋。通过加强该口袋的接触,CAD‑1883 实际上将钙调蛋白与 SK2 粘合在一种可以拉开内门并扩张孔的构象中。结构比较显示 CAD‑1883 结合状态类似于完全开放的通道,尽管在长时间开启后选择性滤器可能会进入失活构象。
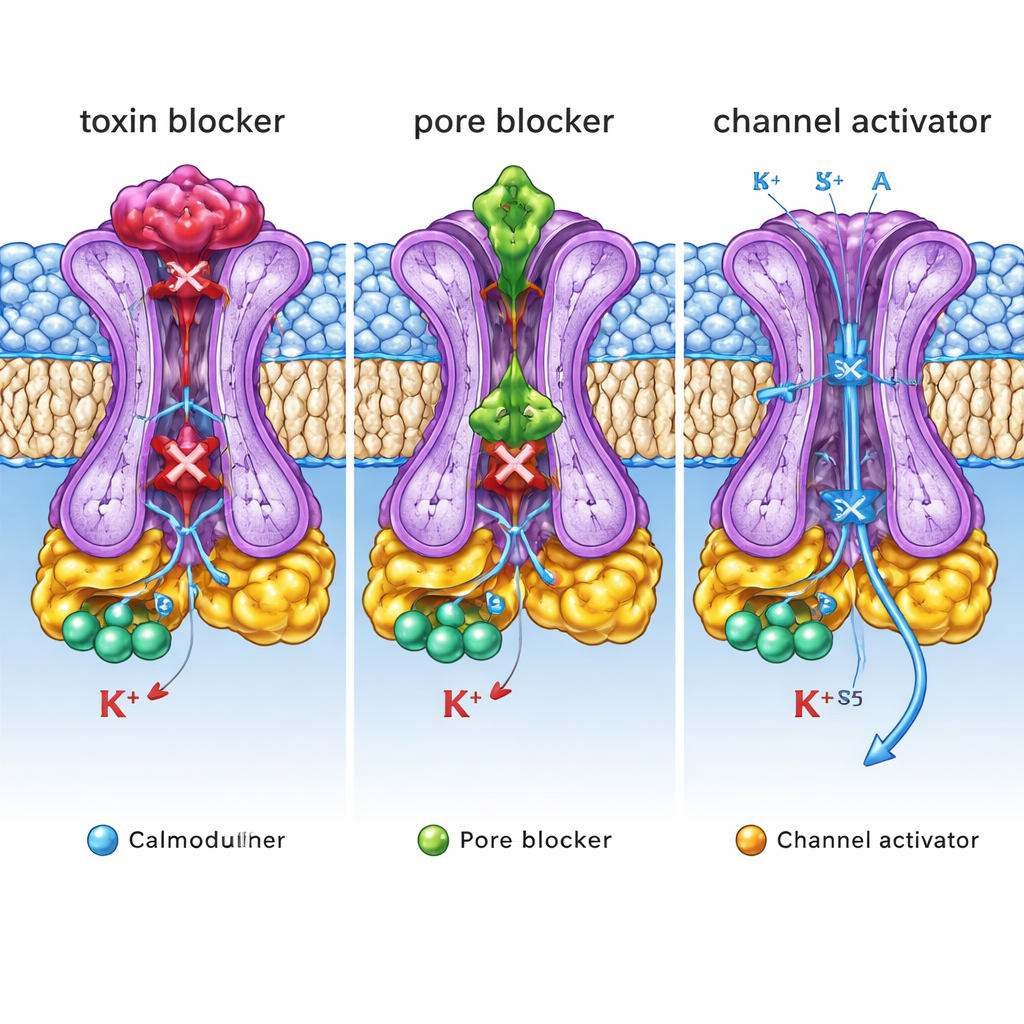
这些结构蓝图对医学意味着什么
总体来看,这些结构揭示了单一 SK2 通道上的三处不同“控制旋钮”:一个供毒素和部分阻断剂停驻的外部盖,一个其他抑制剂堵塞流动的内部孔腔,以及一个激活剂稳定开放状态的侧面口袋。对非专业读者而言,关键结论是:同一离子通道可以通过抓住截然不同的结构把手被向上或向下调节。通过以原子精度绘制这些把手并将其与功能效应关联,本研究为设计下一代选择性抑制或增强 SK2 活性的分子提供了详尽蓝图。这样的定制药物有朝一日可望更少副作用地帮助规范异常脑节律、缓解震颤或纠正不规则心跳。
引用: Ma, B., Wu, D., Cao, E. et al. Structural mechanisms for inhibition and activation of human small-conductance Ca2+-activated potassium channel SK2. Nat Commun 17, 1770 (2026). https://doi.org/10.1038/s41467-026-68475-4
关键词: SK2 钾通道, 钙激活通道, 冷冻电镜结构, 离子通道调节剂, 房颤与震颤