Clear Sky Science · zh
通过活体成像揭示杜氏肌营养不良症中干细胞迁移和分裂受损
为何这则肌肉故事重要
杜氏肌营养不良症(DMD)是一种致命的儿童疾病,会逐步破坏肌肉。几十年来,大多数研究集中在DMD中崩解的大型肌纤维上。本研究表明,另一个更“安静”的参与者也出现了问题:肌肉自身的干细胞,通常负责修复损伤。通过在小鼠肌肉及单根肌纤维上对这些细胞进行实时观察,作者揭示了DMD中干细胞如何迷失方向,为能更有效促进肌肉再生的治疗策略提供了新思路。
肌肉的内建修复小队
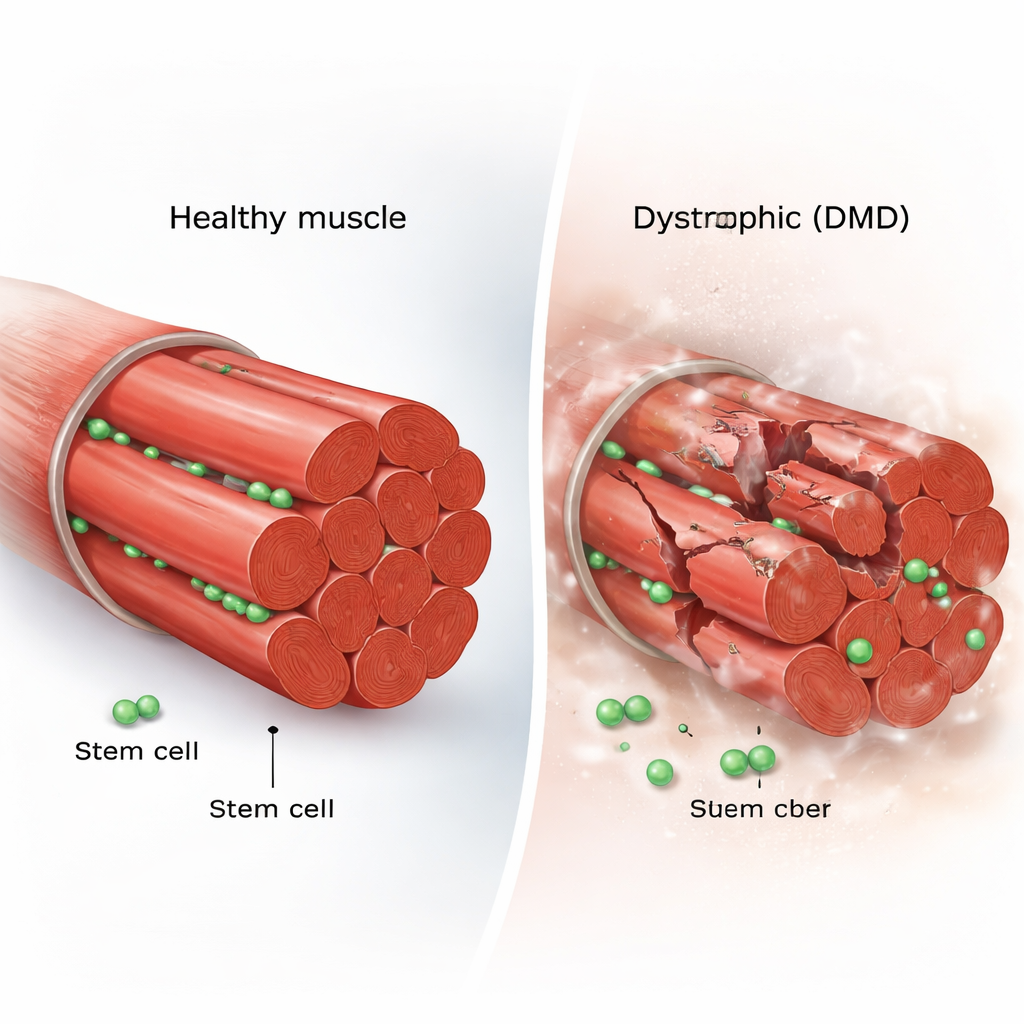
每条骨骼肌纤维两侧都驻留着少量肌肉干细胞,称为肌卫星细胞。在健康肌肉中,这些细胞大多数时间处于静眠状态。受伤时,它们被唤醒、分裂,并要么生成新的干细胞以补充储备,要么产生特化细胞融入受损纤维。这种自我更新与分化之间的精细平衡维持着终生的肌肉强度。然而在DMD中,由于缺乏关键结构蛋白肌萎缩蛋白(dystrophin),肌纤维反复撕裂,人们便质疑修复小队本身是否也会耗竭或走偏。
拍摄正在行动的干细胞
为了解答这一点,研究者使用了mdx小鼠——DMD的常用模型——并对其肌肉干细胞进行了工程改造,使其在显微镜下能够发光可见。随后他们进行了体内成像(intravital imaging),这项技术能在麻醉动物体内对活细胞进行数小时的拍摄。研究团队还开发了一种定制“微孔”体系,用以在培养中固定单根肌纤维,同时追踪每一次干细胞分裂和移动。这种双重方法使他们能从静息状态一路跟踪个体细胞,观察其反复分裂、迁移并最终融入新肌纤维的过程,捕捉到静态快照容易遗漏的行为。
修复细胞的匆忙与绊脚
在受伤的健康肌肉中,由干细胞衍生的肌源性细胞伸长并沿着纤维爬行,轨迹相对笔直且有方向性,分裂与扩散效率较高。相比之下,病变(mdx)细胞常常变得圆润且迟缓。它们移动更慢、方向性差,且有一部分几乎静止不动。研究组还发现,mdx细胞比正常细胞更早融合成新肌纤维,且许多子代在分裂后并未分离而是一起迁移。总体上,mdx肌肉显示出“过早分化”的迹象:干细胞匆忙变成肌细胞并形成纤维,而不是维持一个可持续修复的充足储备。
失衡的细胞分裂与混乱的微环境
在离体单根纤维上,研究者能够对每个干细胞的分裂方式进行分类。在健康肌肉中,大多数分裂是对称且平衡的——许多分裂产生两个可继续增殖的子代,从而扩展修复池,而较少产生两个终末分化的细胞。非对称分裂(一个子代保持为干细胞,另一个投入修复)相对少见但存在。在mdx肌肉中,分裂模式发生了显著转变:对称分裂更倾向于产生两个分化细胞,生成两个更新细胞的分裂明显减少。异体移植实验(将健康干细胞置于病变纤维上,反之亦然)显示,迁移缺陷在很大程度上由受损的纤维环境决定,而mdx干细胞过度分化的行为则随细胞本身而来,部分由其炎症历史塑造。
错配的信号及其对治疗的意义
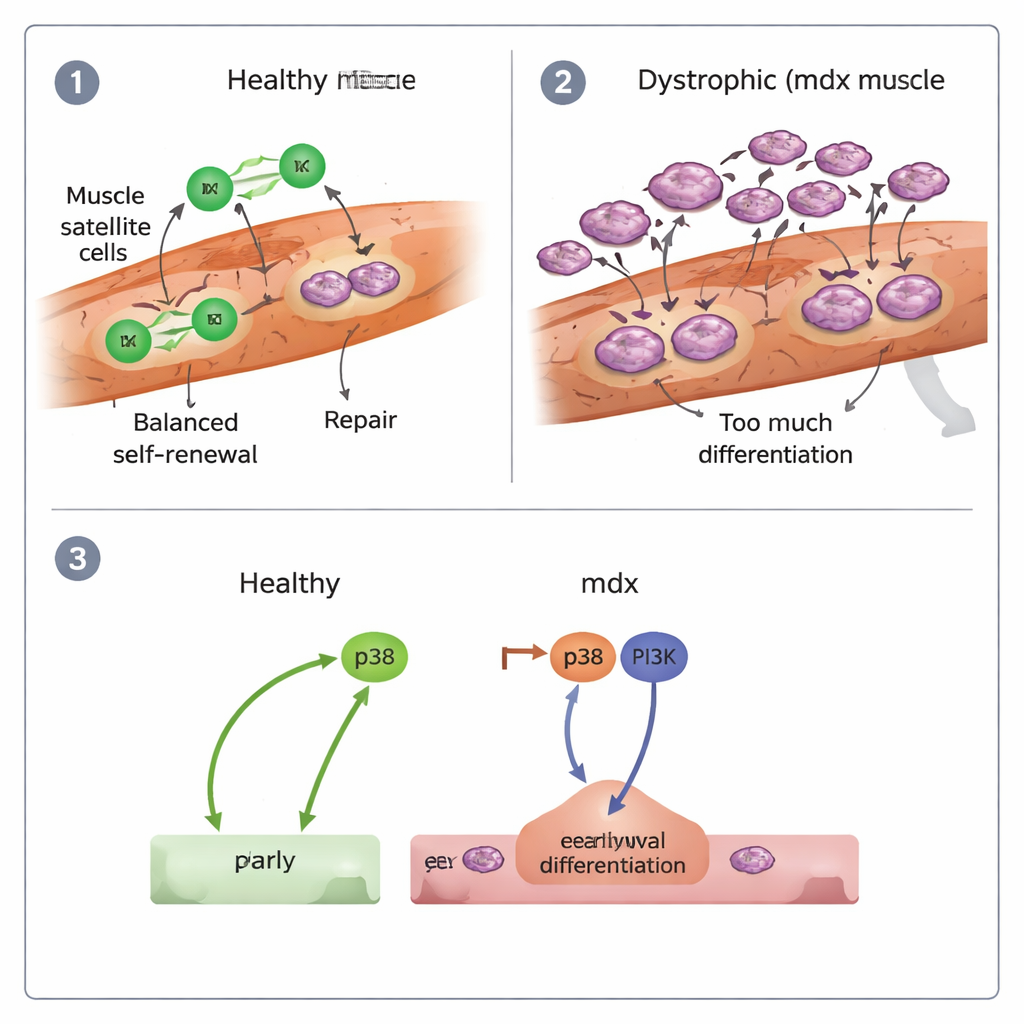
作者还探究了推动干细胞分化的分子开关,重点关注两条信号通路:p38和PI3K。在健康细胞中,抑制p38会显著减少分化,而抑制PI3K影响不大。然而在mdx细胞中,必须同时阻断这两条通路才能抑制过度分化,且即便如此,它们的增殖能力仍然较差。这提示DMD干细胞受p38与PI3K联合活性驱动而进入“早期耗竭”状态,导致再生启动迅速但难以维持。
对杜氏的新认识:也可视为一种干细胞疾病
对于普通读者来说,核心信息是:DMD不仅仅是脆弱肌纤维的问题;同样是负责修复的系统出了问题。在病变肌肉中,干细胞移动效率下降、分裂方式导致储备耗尽,并对关键生长信号产生异常反应。通过厘清哪些缺陷源自受损的肌肉环境、哪些是干细胞固有改变的结果,这项工作提出了新的策略:调节p38和PI3K信号、恢复平衡的细胞分裂或改善局部微环境,或能更有效地重建肌肉,并延长基因或细胞治疗为杜氏患者带来的益处。
引用: Sarde, L., Letort, G., Varet, H. et al. Impaired stem cell migration and divisions in Duchenne muscular dystrophy revealed by live imaging. Nat Commun 17, 1769 (2026). https://doi.org/10.1038/s41467-026-68474-5
关键词: 杜氏肌营养不良症, 肌肉干细胞, 细胞迁移, 干细胞分裂, 再生医学