Clear Sky Science · zh
H3K27me3 依赖的印记与转录调控在小鼠早期胚胎中需要 EZHIP 对 PRC2 活性的限制
为什么微小的胚胎需要精确的基因时序
每一种哺乳动物的生命都始于一个单细胞,该细胞携带来自母方和父方的各一套染色体。尽管这两份遗传信息的 DNA 字母几乎相同,但它们被不同的化学标签包裹,这些标签帮助决定哪些基因被打开或关闭。本研究探讨了在小鼠受精后头几天内,这类标记系统如何被保持平衡,以及扰乱这种平衡为何会使正常发育偏离轨道。
两位亲本,两种不同的基因组包装方式
在哺乳动物中,某些基因的表现取决于它们来自母亲还是父亲,这一现象被称为基因组印记。经典的印记依赖于 DNA 本身的化学标记,但近年来科学家发现第二种更短暂的印记类型依赖于组蛋白修饰 H3K27me3。组蛋白像线轴一样缠绕 DNA,而 H3K27me3 往往会抑制附近基因的表达。在正常的小鼠胚胎中,母源基因组在受精后携带比父源基因组更多的这种标记,帮助沉默特定的母源基因拷贝,同时允许父源拷贝发挥作用。
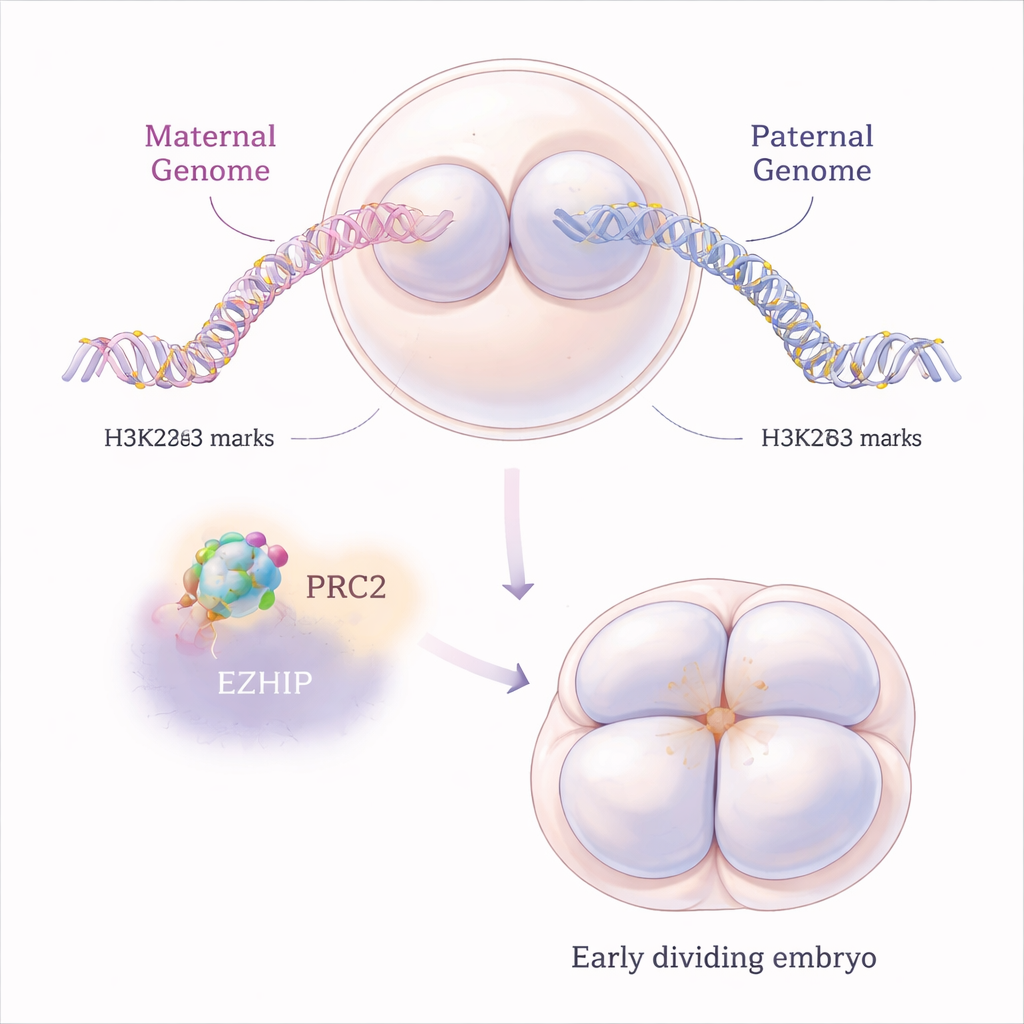
对强效抑制器的一种分子刹车
H3K27me3 由一个称为 PRC2 的大型蛋白机器添加到染色质上。作者关注的是 EZHIP,这是一种与 PRC2 结合并减缓其活性的较少为人知的蛋白。小鼠卵细胞产生大量 Ezhip RNA,所翻译出的 EZHIP 蛋白在胚胎早期的几个细胞分裂周期内仍然存在。通过研究母体缺失 Ezhip 的小鼠,研究者探究了当这道天然刹车被移除会发生什么。他们发现,在没有 EZHIP 的情况下,卵子和早期胚胎获得了额外的 H3K27me3 标记,但呈现出一种出人意料的“扁平化”形态:抑制性标记不是形成锋利、界定明确的区域,而是更广泛地扩散,模糊了正常模式,影响了母源和父源染色体。
过度抑制如何破坏印记
利用灵敏的基因组定位方法,研究团队显示来自缺乏 Ezhip 的卵子发育而成的胚胎中,母源与父源 H3K27me3 景观之间的常见不对称性在很大程度上丧失。许多通常只在一方等位基因上保有 H3K27me3 的区域,现在在双方都获得了该标记,或其模式被涂抹开来。该变化对那些通常由 H3K27me3(而非 DNA 甲基化)控制的印记基因产生了重要后果。在对照胚胎中,这些基因倾向于主要从父源等位基因表达。然而在缺乏母源 EZHIP 的胚胎中,同样的基因常常从双亲拷贝同时被激活,且许多基因的总体 RNA 水平反而上升,而不是被双重沉默。
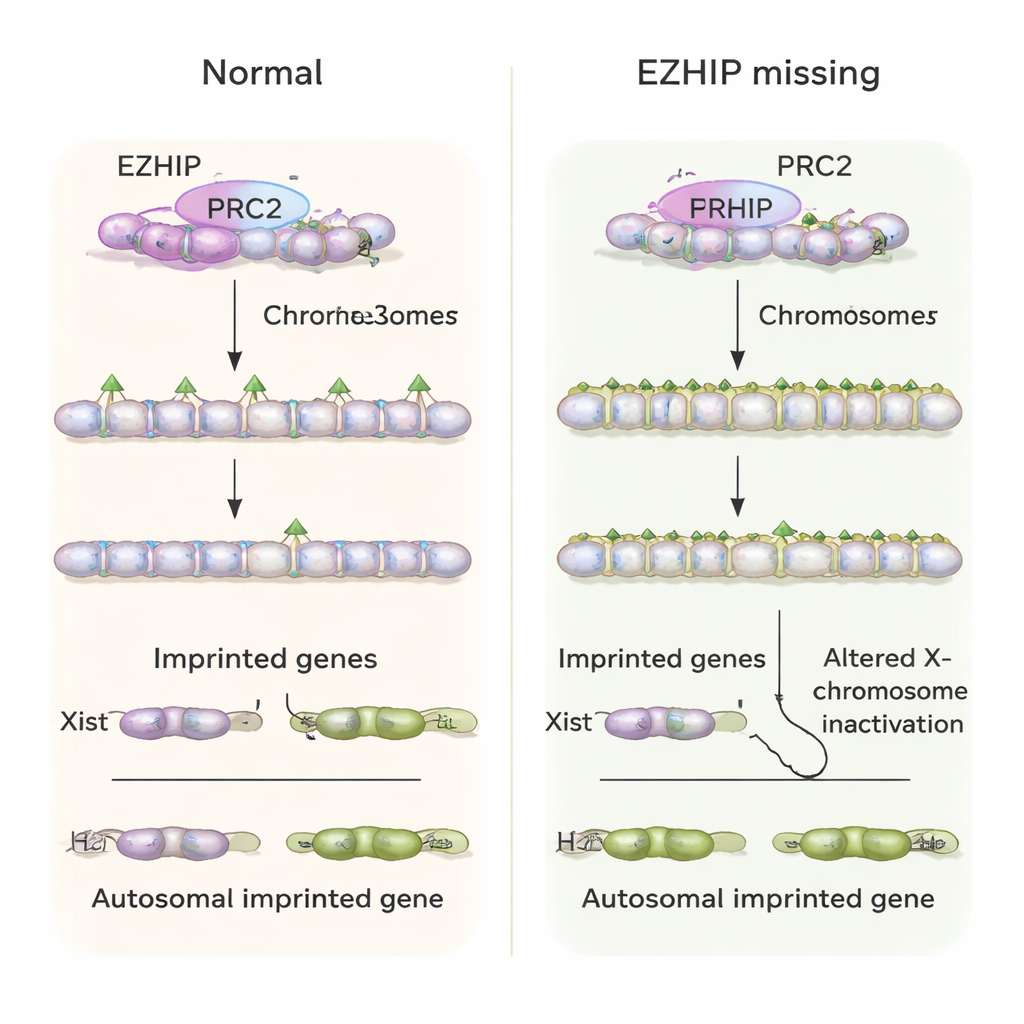
X 染色体控制和胚胎健康受损
一个关键的 H3K27me3 依赖性印记基因是 Xist,一种长 RNA,可在雌性细胞中包裹并使一条 X 染色体失活,以实现与雄性基因剂量的平衡。通常,早期小鼠胚胎中雌性仅在父源 X 上表达 Xist,而雄性则根本不表达。在缺乏母源 EZHIP 的情况下,作者观察到雌性胚胎常常在两条 X 染色体上都表达 Xist,而雄性胚胎也“不恰当地”在其唯一的 X 上激活 Xist。这导致了 X 连锁基因异常的失活模式。在个体水平上,出生于 Ezhip 缺失母鼠的后代数量减少,胚胎表现出生长改变以及支持胎盘的额外胚外组织出现问题,这与早期印记失败所致的长期发育压力一致。
过犹不及
对非专业读者而言,似乎更多的沉默性标记如 H3K27me3 会简单地使更多基因沉默,这种直观想法也不足为奇。但这项工作表明,将基因组以错误模式过度载入此类标记反而会削弱它们作为精确开关的能力。通过移除 EZHIP,研究者释放了 PRC2,使 H3K27me3 广泛扩散,导致印记信号模糊,关键调控因子如 Xist 被错误控制。该研究强调,早期胚胎不仅依赖于正确的分子存在,还依赖于将这些分子的活性严格调谐,以便以适当的平衡读取母源与父源基因组。
引用: Diop, S., Richart, L., Petitalot, A. et al. H3K27me3-dependent imprinting and transcriptional regulation in early mouse embryos requires EZHIP-mediated restriction of PRC2 activity. Nat Commun 17, 1758 (2026). https://doi.org/10.1038/s41467-026-68467-4
关键词: 表观遗传学, 基因组印记, 早期胚胎发育, X 染色体失活, Polycomb PRC2