Clear Sky Science · zh
利用葡聚糖诱导的训练免疫对巨噬细胞进行表观遗传与代谢重编程以增强结直肠癌疫苗应答
唤醒机体的第一线应答者
结直肠癌是全球最致命的癌症之一,目前大多数患者无法从现有免疫疗法中获益。这项研究探讨了一个引人注目的想法:如果我们能“训练”固有免疫系统——机体的第一线应答者——去记住危险信号并帮助疫苗更有效地对抗结直肠肿瘤,会怎样?研究者使用来自酵母的天然多糖β‑葡聚糖,展示了如何重编程早期免疫细胞,使癌症疫苗能够诱导更强、更持久的抗肿瘤反应。
为何结直肠癌需要新的防御手段
结直肠癌每年导致近一百万人死亡,并且年轻成人的发病率在上升。手术、化疗和放疗等标准治疗在某些情况下有效,但许多患者出现复发并承受严重副作用。较新的免疫药物,如检查点抑制剂,仅在携带特定DNA修复缺陷的一小部分结直肠癌患者中表现出良好疗效。对于大多数患者,这些药物甚至实验性癌症疫苗都难以奏效,因为肿瘤微环境被抑制免疫攻击的细胞和信号所主导。
教会固有免疫新技巧
机体的固有免疫细胞——尤其是巨噬细胞——通常对威胁反应迅速但短暂,长期被认为缺乏记忆。然而,过去十年的研究揭示了“训练免疫”现象:强烈的初始刺激会在这些细胞上留下持久痕迹,使其在之后能更强烈地反应。作者使用β‑葡聚糖(一种酵母细胞壁成分)来诱导这种训练状态。在小鼠中,短时处理整个β‑葡聚糖颗粒在基因表达和细胞代谢层面重编程了巨噬细胞。当这些受训小鼠随后接种一种基于工程化腺病毒的结直肠癌疫苗(称为PeptiCrad)时,其免疫系统产生了更强效的杀伤性T细胞,这些T细胞更善于识别并攻击肿瘤特异性靶点。 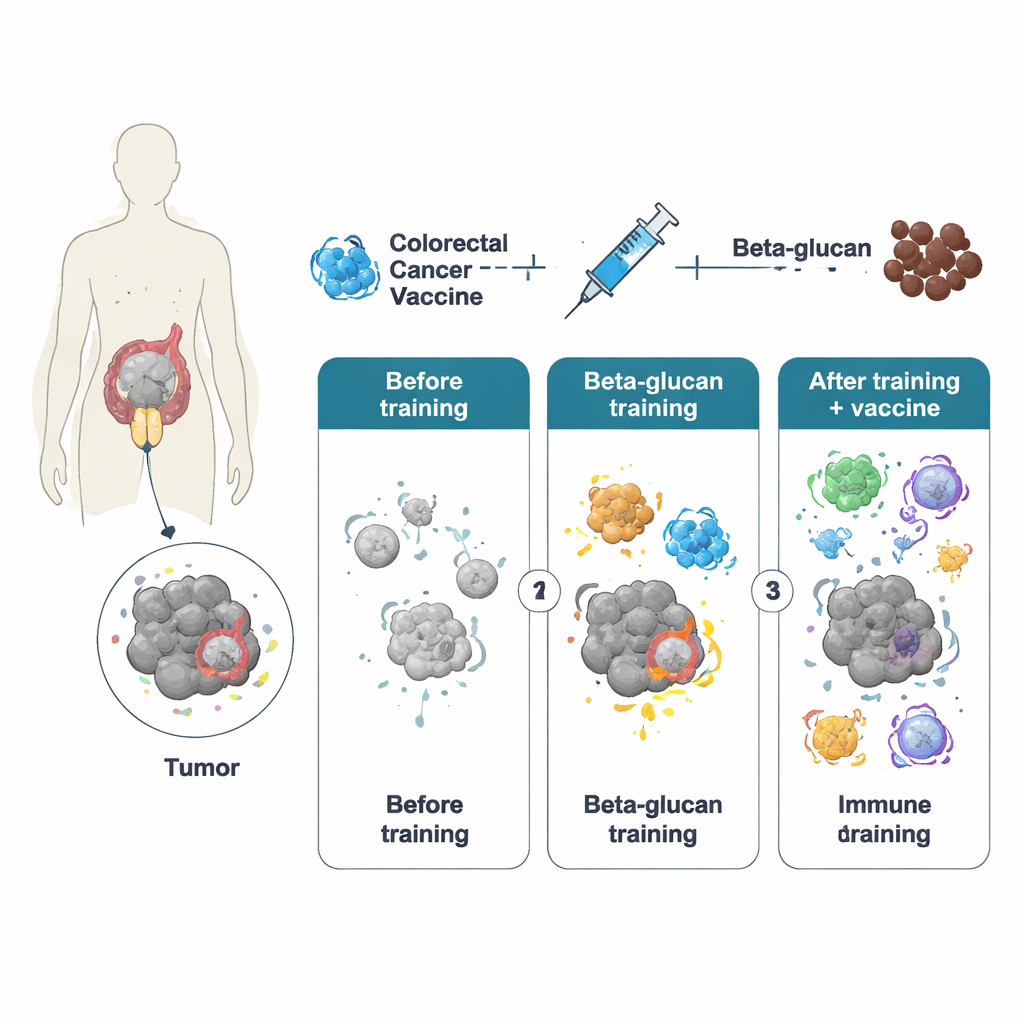
在肿瘤内重接能量与通讯线路
进一步研究中,研究者从肿瘤中分离免疫细胞并逐细胞分析其代谢与基因活动。他们发现受训巨噬细胞转入了一种高速代谢模式,类似于“瓦尔堡效应”,即细胞快速燃烧糖并将资源转向构建生长与功能所需的分子。这些细胞还增强了肌酸代谢——这在运动补剂领域更为人知——帮助提供产生炎性分子所需的额外能量。同时,DNA相关蛋白上的特定化学修饰(尤其是H3K4me3的增加)标记了与趋化因子产生相关的基因,有效地锁定了一套促炎、抗肿瘤的程序并得以长期维持。
构建免疫接力队伍
单细胞测序显示肿瘤内不同免疫细胞之间存在分步接力。首先,受训巨噬细胞释放两种关键信号CXCL9和CXCL10的高水平,它们通过受体CXCR3吸引自然杀伤(NK)细胞。被招募入的NK细胞不仅直接杀伤癌细胞,还分泌另一种信使CCL5,进而吸引一种称为cDC1的专职树突状细胞亚群。这类树突状细胞擅长向T细胞呈递肿瘤抗原。结果是更多的CD8 T细胞被激活并转变为效应记忆细胞——在再次遇到肿瘤时能迅速且强烈地应答。阻断肌酸利用、耗尽巨噬细胞或NK细胞,或干扰这些趋化因子通路都会削弱肿瘤控制,强调了疫苗成功对这一巨噬细胞–NK–树突状细胞–T细胞回路的依赖性。 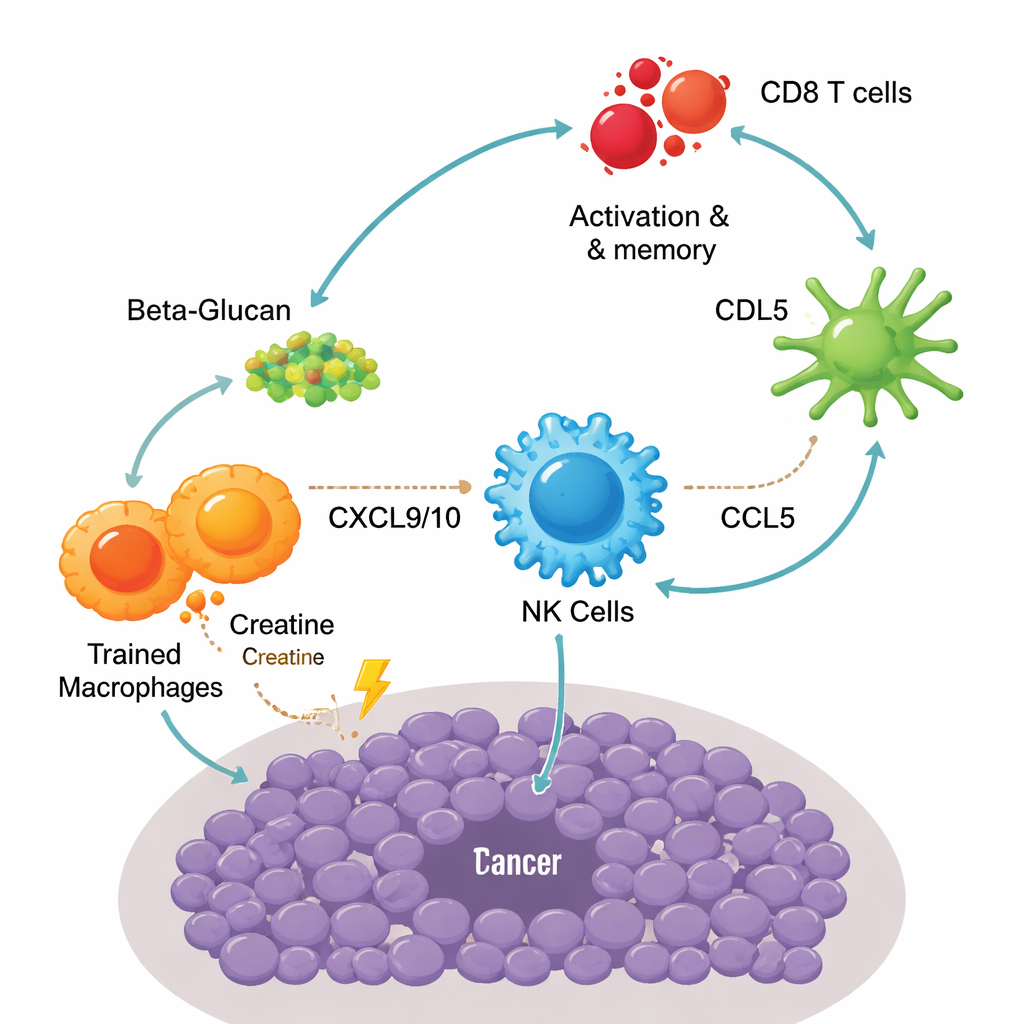
从小鼠模型到人类肿瘤类器官
研究团队在多个结直肠癌小鼠模型中验证了该策略,包括一种对常见免疫疗法抵抗性较强的顽固类型。在每种情况下,将β‑葡聚糖训练与疫苗联合使用比任一单独治疗更能有效减缓肿瘤生长。重要的是,他们还将研究扩展到了人类。暴露于β‑葡聚糖的人类血细胞在对结直肠癌疫苗肽的反应中表现更好,产生更多免疫刺激性细胞因子。当这些受训的免疫细胞被扩增并与来自患者的微型结直肠肿瘤(类器官)共同培养时,它们比未经训练的细胞杀死了更多癌细胞。去除体系中的人单核细胞和巨噬细胞会抹去这一益处,证实这些受训细胞是关键的协调者而非仅仅是直接的肿瘤杀手。
这对未来癌症疫苗意味着什么
简而言之,这项工作表明一种安全的酵母来源多糖可以“指导”固有免疫细胞,支持更有效的结直肠癌疫苗接种。通过重编程巨噬细胞的能量利用方式以及它们保持待命的基因,β‑葡聚糖训练引发多米诺效应:巨噬细胞招募NK细胞、NK细胞召集专业树突状细胞,三者共同打造更强大的记忆CD8 T细胞群。尽管仍需在临床试验中检验许多问题——包括安全性、给药时机与最佳疫苗组合——训练免疫在这里展现出作为佐剂策略的潜力,或能将更多“冷”性、免疫抑制的结直肠肿瘤转化为可被免疫系统识别和控制的目标。
引用: Hamdan, F., Gandolfi, S., D’Alessio, F. et al. Leveraging glucan-induced trained immunity for the epigenetic and metabolic rewiring of macrophages to enhance colorectal cancer vaccine response. Nat Commun 17, 1757 (2026). https://doi.org/10.1038/s41467-026-68466-5
关键词: 结直肠癌免疫治疗, 训练免疫, β-葡聚糖, 巨噬细胞与NK细胞, 癌症疫苗