Clear Sky Science · zh
体内 CRISPR 筛选鉴定出 SAGA 复合体成员作为造血的关键调控因子
为何维持血液生成平衡很重要
每天,你的身体在不为人知中制造数千亿个新的血细胞,它们负责运输氧气、抵抗感染并止血。这种持续不断的生成依赖于骨髓中罕见的“母”细胞,即造血干细胞。当控制这些细胞的机制出现问题时,人们可能会出现贫血、免疫力下降或白血病等癌症。本研究提出了一个简单却有力的问题:在我们基因组中的数千个基因里,哪些基因对于维持健康和平衡的血细胞生成确实是必不可少的?
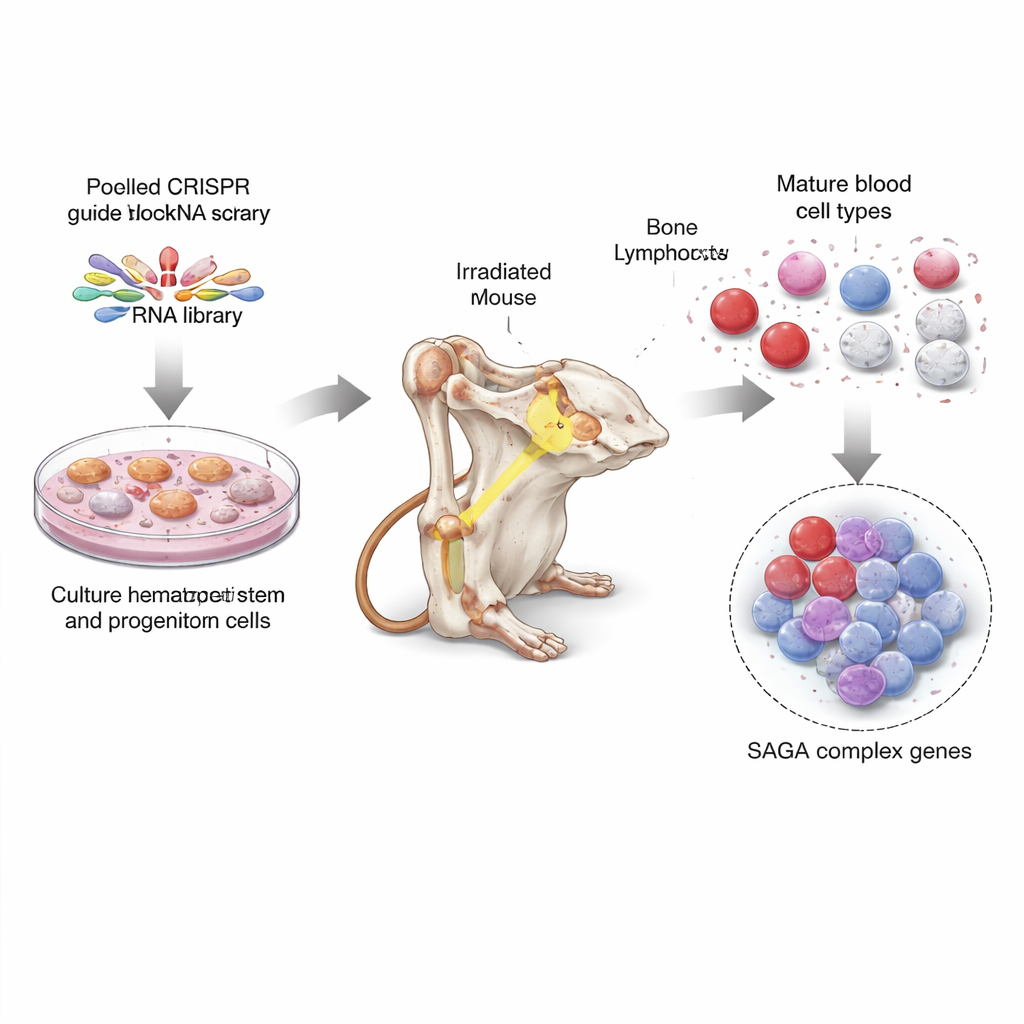
在小鼠干细胞中进行的全基因组寻宝
为了解答这一问题,研究人员使用 CRISPR——常被比作分子剪刀的基因编辑工具——关闭小鼠基因组中几乎每一个基因,每个基因设计十个向导序列。他们首先在特定培养条件下大量扩增骨髓干细胞与祖细胞,然后用混合的 CRISPR 向导感染这些细胞,使得每个细胞带有针对不同基因的敲除。随后,他们将这些混合并编辑过的细胞移植到数十只接受过照射的鼠体内,允许编辑细胞重建动物的血液系统。几个月后,研究人员从骨髓中纯化出各种成熟血细胞类型和类干细胞,测定哪些 CRISPR 向导被过度或不足地代表。由此揭示出哪些基因缺失有利于未成熟细胞积累,哪些则支持成熟血细胞的生成。
一个名为 SAGA 的隐秘控制枢纽浮出水面
在许多已知的造血调控因子中,出现了一组令人惊讶的命中:多个属于大型蛋白复合体 SAGA 的结构组件,包括名为 Tada2b、Taf5l 和 Tada1 的基因。SAGA 本身并不直接制造血细胞;相反,它通过化学修饰一种称为组蛋白的 DNA 包装蛋白来帮助开启或关闭其他基因。当团队单独敲除这些 SAGA 组分并将编辑后的细胞移植到小鼠体内时,观察到一致的模式:未成熟的骨髓细胞大量积累,但它们分化为循环白细胞、红细胞和某些免疫细胞的能力显著下降。实质上,干细胞和祖细胞被卡在了一个瓶颈中,无法完成向功能性血细胞的转变。
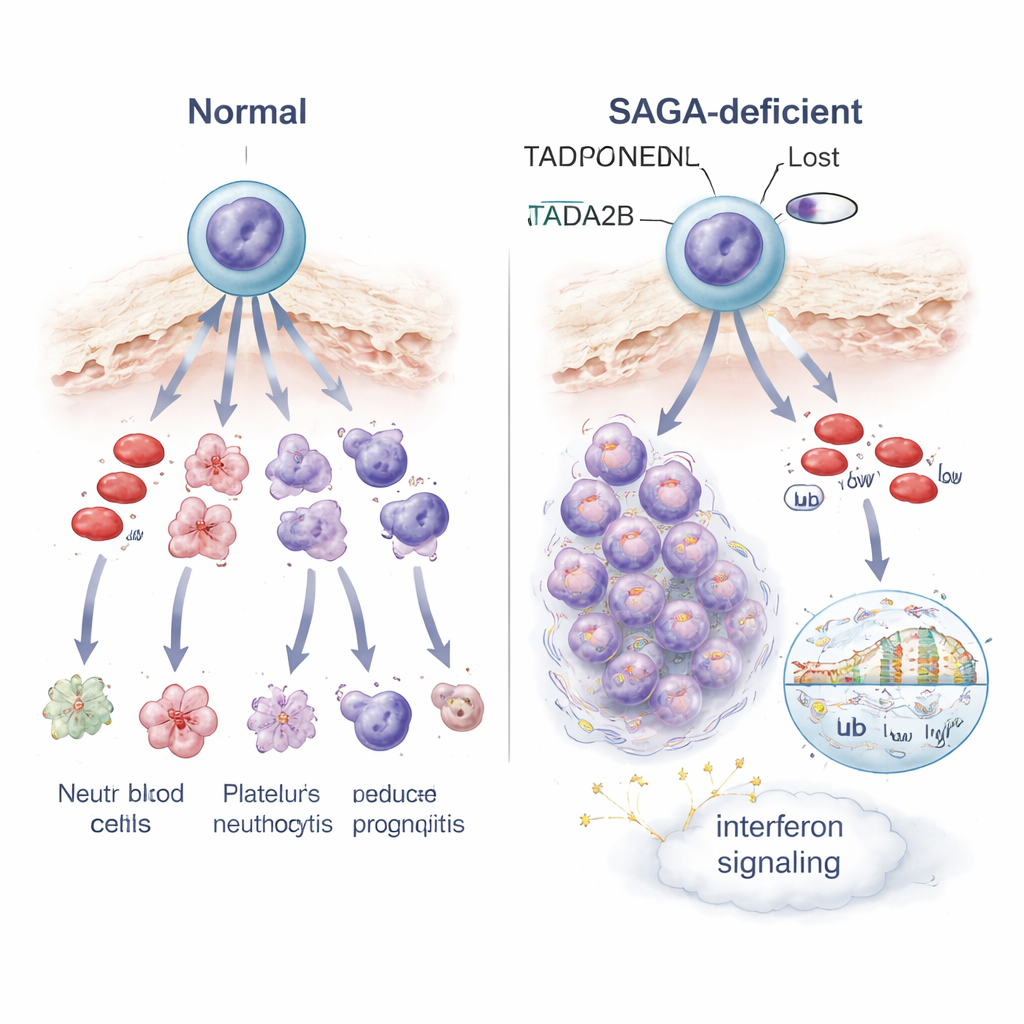
基因控制紊乱如何改变细胞命运与应激信号
为了解这些受阻细胞内部发生了什么,科学家们对单细胞和群体水平的基因活性进行了分析。失去 Tada2b 或 Taf5l 会在干细胞中重编程许多基因的活性,呈现两个显著主题。首先,参与干扰素信号的基因——通常属于机体抗病毒防御的一部分——被激活,表明细胞处于内部警报或应激状态。其次,细胞的线粒体(为细胞工作提供能量的微小发电站)活动下降,且这些改变的细胞对一种靶向线粒体能量产生的药物更为敏感。在 DNA 包装层面,缺失 Tada2b 的细胞显示出与开放、活跃染色质相关的组蛋白标记水平降低,以及与基因读取方式相关的另一种标记发生变化。这些染色质化学性质的转变可能有助于解释为何包括指导正常血液成熟的基因在内的许多基因变得失调。
从基础机制到疾病模型
研究团队随后检验了提高或降低 SAGA 活性是否能逆转这些效应。促使细胞过表达 Tada2b 会降低与干扰素相关的基因活性,并减少类干细胞的比例,这与敲除的表型正好相反。用抑制 SAGA 关键酶亚基的药物处理正常干细胞可以再现大部分 Tada2b 丧失的分子特征,进一步支持 SAGA 的染色质修饰活性在其功能中的核心地位。最后,研究者转向人类骨髓增生异常综合征的细胞模型,这是一种前白血病性疾病,血液生成受损且干扰素通路常被上调。当他们在这些人类细胞中敲除 SAGA 组分并将其移植到免疫缺陷小鼠中时,编辑细胞获得了增殖优势,并再次激活了干扰素和髓系基因程序,提示该调控枢纽也影响疾病行为。
这对血液健康和未来疗法意味着什么
对一般读者而言,核心信息是:这项研究揭示了一个强大的控制中心——SAGA 复合体——它帮助造血干细胞决定何时保持未成熟、何时分化以及如何避免有害的应激反应。当关键的 SAGA 成员缺失时,干细胞积累但无法产生足够的功能性血细胞,同时应激和类抗病毒信号上升,线粒体功能衰退。这些发现不仅深化了我们对终生维持健康血液生成机制的理解,也暗示 SAGA 活性的微小变化可能促成与年龄相关的血液问题和骨髓增生异常综合征等疾病。长期来看,描绘这一调控电路可能帮助科学家设计出能够将有缺陷的干细胞重新引导回平衡且有弹性的血液生成的疗法。
引用: Shankar, A., Olender, L., Hsu, I. et al. In vivo CRISPR screening identifies SAGA complex members as key regulators of hematopoiesis. Nat Commun 17, 1756 (2026). https://doi.org/10.1038/s41467-026-68465-6
关键词: 造血干细胞, CRISPR 筛选, SAGA 复合体, 干扰素信号, 骨髓增生异常综合征