Clear Sky Science · zh
来源于神经嵴细胞的 DKK1 和 NEDD4 在第二心场调节 Wnt 信号以协调心输出道发育
为何微小的“心脏建造者”至关重要
早期胚胎的心脏起初是一个简单的管状结构,但它必须迅速重塑为一个能同时向全身和肺部输送血液的复杂器官。这个建造过程中的细微失误可导致严重的出生缺陷,有些情况需要在出生后不久进行手术。该研究揭示了两类细胞在塑造心脏主要出口通道时如何互相通讯,并发现了一种可能导致小鼠和人类先天性心脏病的分子错误。
共同构建心脏出口斜坡的两支队伍
将血液从心室送出的那部分心脏——心输出道——来自一个称为第二心场的区域。此处的细胞必须在加入不断增长的输出道之前保持为灵活的“祖细胞”状态,并在恰当时机转化为成熟的心肌。紧邻它们迁行的是神经嵴细胞,这是一类游走的细胞群,参与构建大血管和瓣膜。早期工作表明神经嵴细胞以某种方式影响第二心场,但这种相互作用的机制尚不清楚。 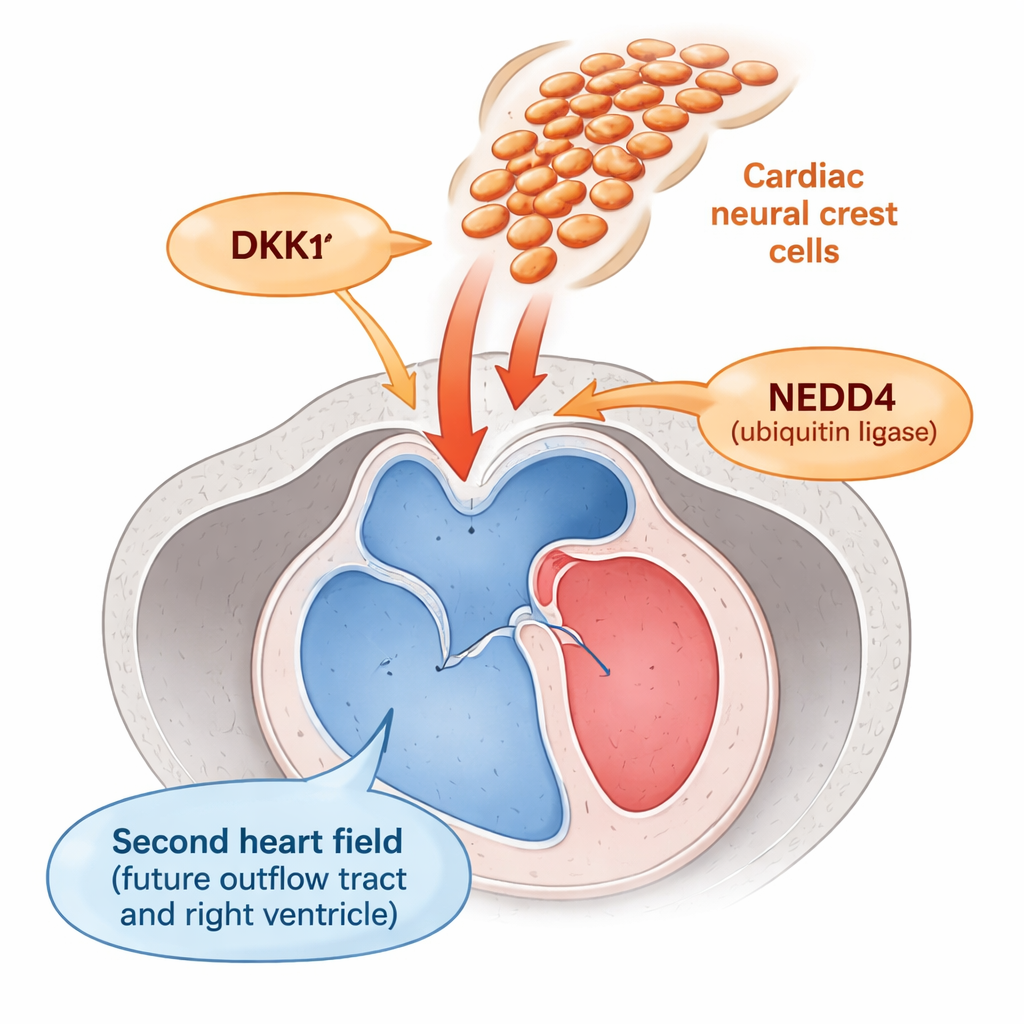
生长信号的分子调光器
作者发现神经嵴细胞像调光开关一样调节一种关键的生长信号 Wnt,Wnt 可维持祖细胞分裂并延迟其成熟。他们发现神经嵴细胞是 DKK1 的主要来源,DKK1 是一种分泌的小蛋白,能在邻近细胞中抑制 Wnt 信号。DKK1 本身通常受 NEDD4 的调控,NEDD4 是一种将 DKK1 标记并送往降解的蛋白。在小鼠胚胎中,如果在神经嵴细胞中缺失 Nedd4,DKK1 会异常积累。过量的 DKK1 降低了邻近第二心场的 Wnt 活性——通过核内 β-连环蛋白减少(Wnt 信号的标准读数)以及多种 Wnt 响应基因表达下调可以看出这一点。
时机出错时,心脏结构失衡
过多的 DKK1 和不足的 Wnt 带来了明确后果:第二心场细胞过早转变为心肌。成熟肌肉的标志在这一祖细胞区提前出现,可用于延长输出道的未分化细胞数量减少。通过追踪分裂细胞随时间的变化,研究团队显示突变体中进入输出道的第二心场细胞数量减少。因此,输出道变短并旋转异常,导致大血管与心室之间错位。这些结构性错误类似于人类锥-动脉干畸形(conotruncal defects),例如双出口右心室,以及在完全敲除 Nedd4 小鼠中观察到的相关畸形。
验证信号的作用并与人类疾病建立联系
为确认改变的 Wnt 信号是否确实导致这些问题,研究者在孕鼠中用药物微调该通路。在原本健康的胚胎中抑制 Wnt,会促使它们出现与丢失 Nedd4 时相同的过早分化和旋转缺陷;而在缺失 Nedd4 的背景下减少 Dkk1 基因剂量,能部分挽救输出道的大小和旋转问题。最后,团队发现一名患有法洛四联症的儿童携带一个罕见的遗传性 NEDD4 变体,该变体削弱了其标记 DKK1 以促降解的能力。工程改造携带相同 Nedd4 变体的小鼠出现右侧心壁和隔缺损,支持了错误的 NEDD4–DKK1 调控可以促成人类先天性心脏病的观点。 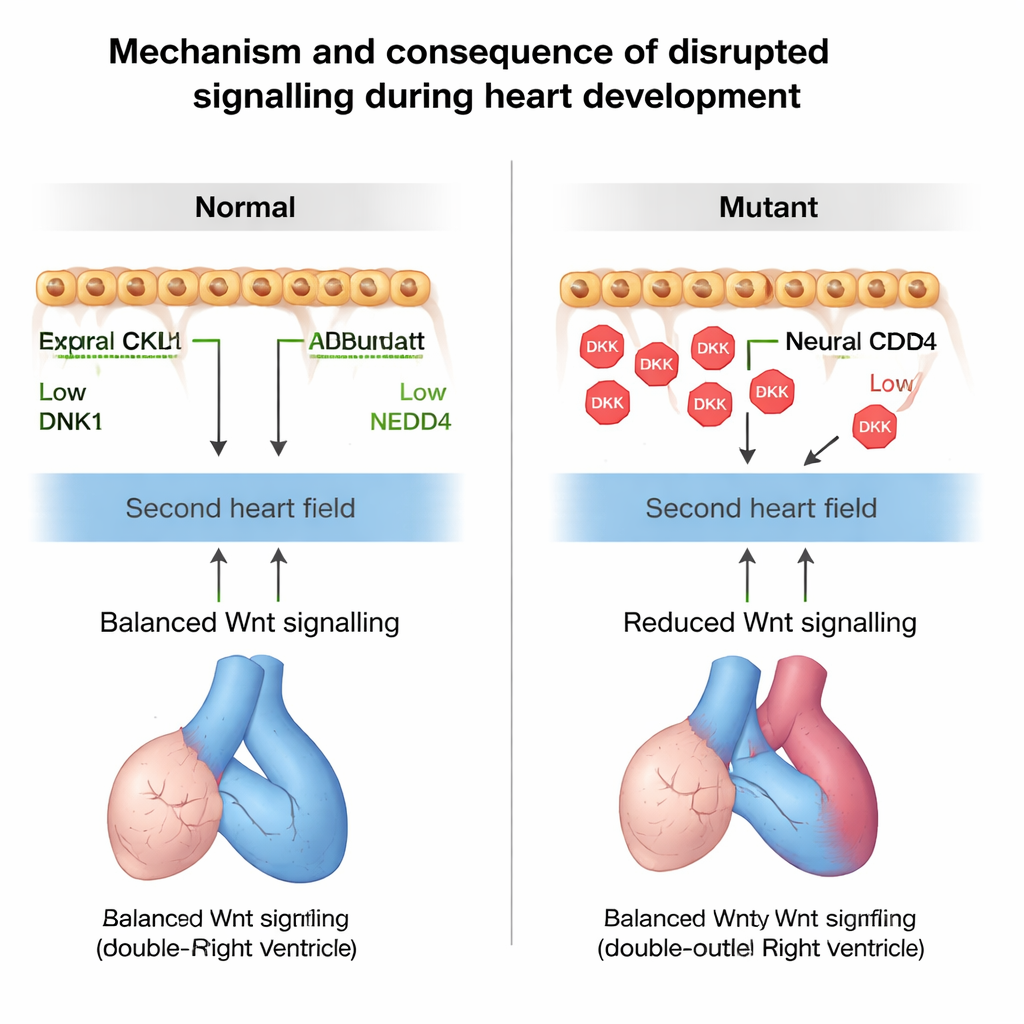
这对理解心脏缺陷意味着什么
对非专业读者而言,核心信息是:心脏的“出口斜坡”依赖于其构建单元何时停止增殖并开始成为心肌这一时机的精确把握。这个时机不仅由心脏组织自身控制,也受到邻近神经嵴细胞通过 NEDD4–DKK1 对生长信号的微调影响。当这一分子调光器被压得过低时,输出道会发育不足并错位,导致严重的出生缺陷。通过绘制这一路径并将其与人类基因变体相联系,该研究为某些先天性心脏病的成因提供了新线索,并强调了未来诊断或干预的潜在分子靶点。
引用: Wiszniak, S., Alankarage, D., Lohraseb, I. et al. Neural crest cell-derived DKK1 and NEDD4 modulate Wnt signalling in the second heart field to orchestrate outflow tract development. Nat Commun 17, 1751 (2026). https://doi.org/10.1038/s41467-026-68459-4
关键词: 先天性心脏病, 心脏发育, 神经嵴细胞, Wnt 信号, 心脏输出道