Clear Sky Science · zh
通过电化学钴催化不对称脱对称构建远程双立体中心
为更好的药物塑造分子形状
化学家早已知道,分子的三维形状决定着药物在体内的效应。许多成功的药物和催化剂之所以有效,正是因为某些原子在空中指向恰当的方向。然而,要在一步反应中精确布置两个相隔较远的“控制点”一直极为困难。本研究提出了一种电力驱动的方法,利用单一钴基催化剂来雕塑含有两个相距较远立体中心的分子——这些是关键的三维特征——为设计药物和专用化学工具打开了新途径。
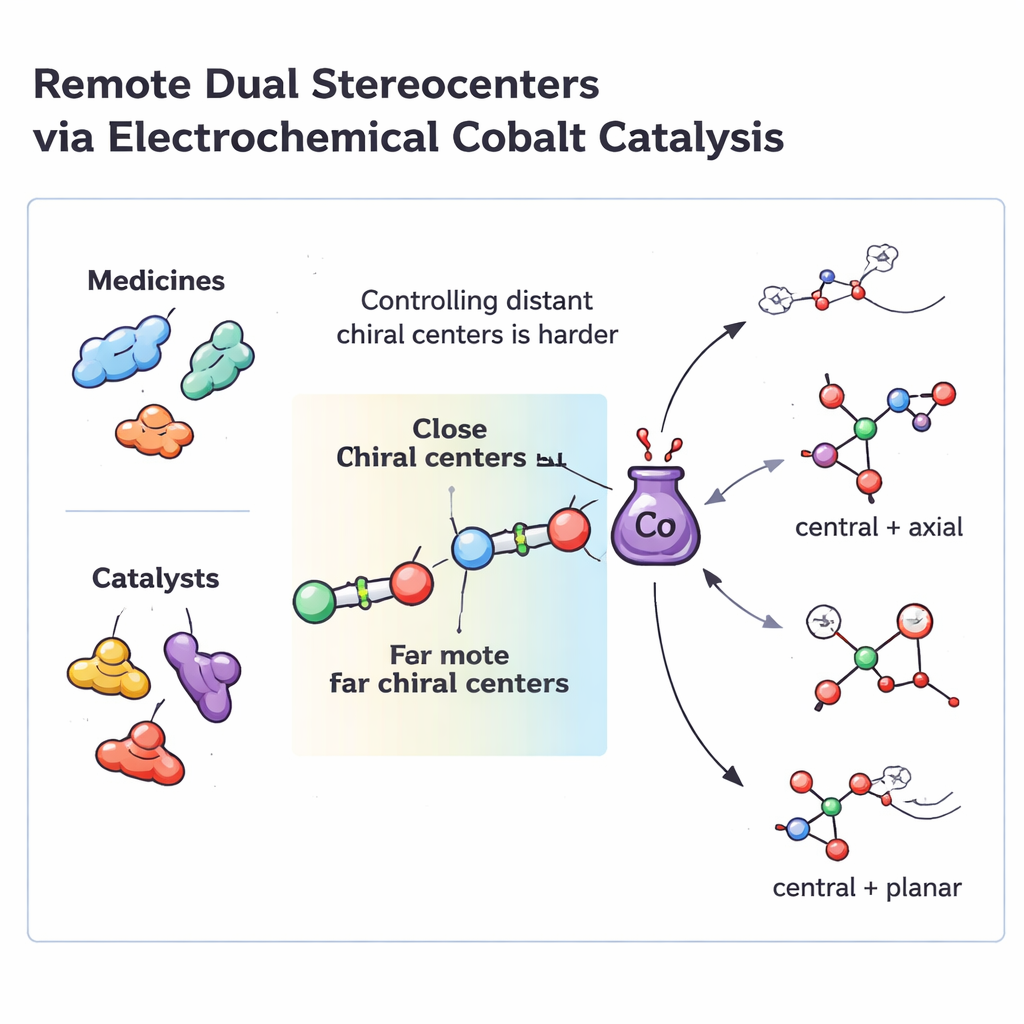
为什么远程控制点很重要
许多现代药物和高性能催化剂都包含两个非邻近的立体中心——即可以存在左旋或右旋的特定原子排列。这些远程控制点常常决定分子如何契合生物靶标或催化剂中的金属位点。传统的不对称方法擅长构建相邻的立体中心,即两个控制点彼此相邻。但当这些点相隔五个或更多原子时,常用的“引导”模型就失效,化学家通常需要多步路线或由两个不同催化剂协同完成。这样的多催化剂体系难以调整、易发生不相容性,且通常只适用于起始物种的狭窄家族。
一种单催化、电力辅助的捷径
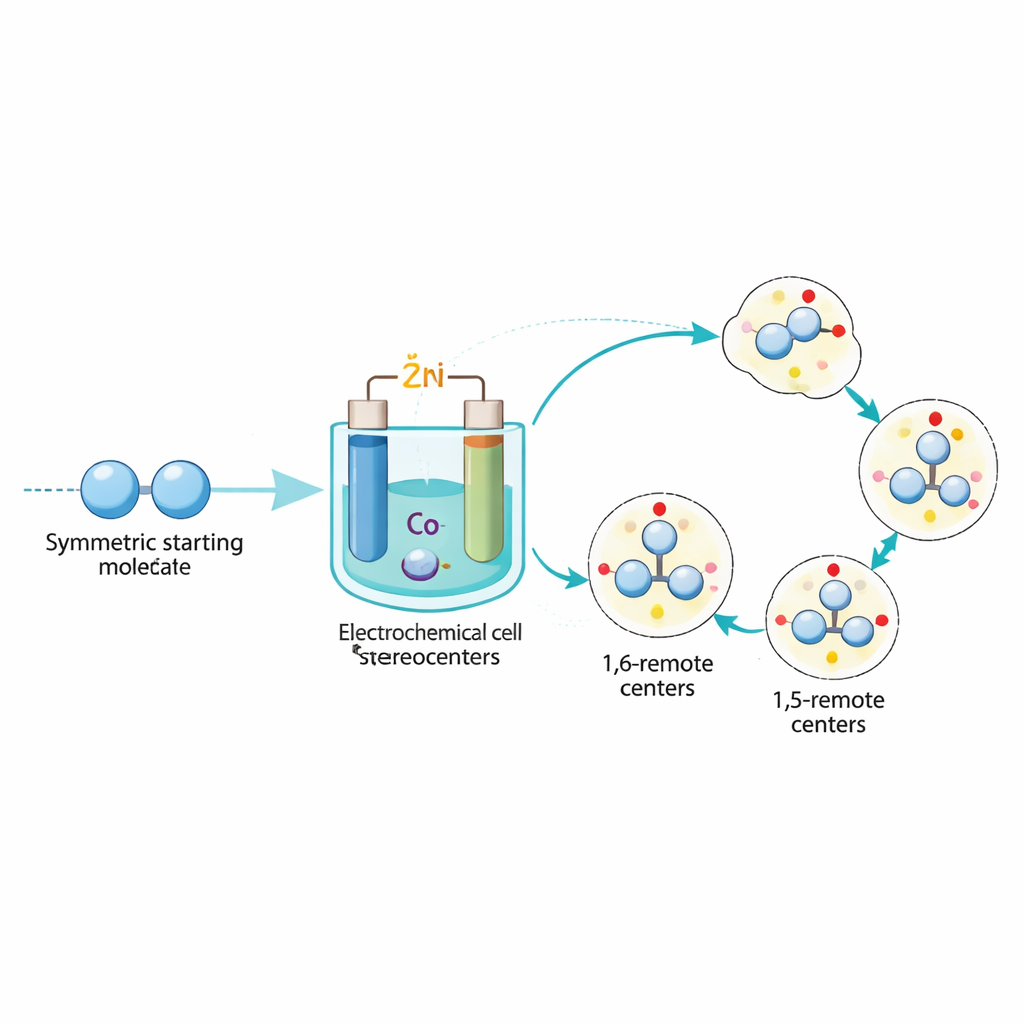
作者通过将电化学与手性钴催化剂结合来应对这一挑战。他们不使用化学还原剂,而是在配有锌和镍电极的简单电池中施加小电流。该电流将带有手性配体的钴络合物还原成低价的活性物种,能够结合并重塑简单的起始物:对称二醛和所谓的烯炔(同时含有双键和三键)。核心思想是脱对称:从具有两个等价“末端”的分子出发,利用手性钴有控制地打破这种对称,使每一端成为明确的三维结构的一部分。
把对称性变为多样性
在优化条件下,这一电化学过程能可靠地将各种二醛和烯炔转化为在远端位置同时包含两种不同手性元素的产物。根据起始骨架的不同,团队可以在同一统一体系中生成四类不同的三维排列:一个中心立体中心与扭曲的C–C轴结合,一个中心立体中心与扭曲的C–O轴结合,以及基于[2.2]对位环烯烃和铁烷(ferrocene)骨架的两种平面手性。在实践中,这意味着他们可以制造出空间构型在多年内保持锁定的分子族,且对单一三维构型具有极高的选择性,同时芳香环上可容忍多种取代基。
窥探反应机理
为理解该过程的工作原理,研究者进行了标记实验和机理探测。通过将某些氢原子替换为氘(氢的较重同位素),他们证明这些原子最终位于产物中预期的位置,且不同分子间没有发生混掺。这排除了某些竞争反应路径,并支持一种逐步机理:钴催化剂首先与烯炔形成类似环状的中间体,从而建立第一个立体中心。随后二醛插入该中间体以生成第二个立体中心,接着发生释放产物并再生活性钴物种的步骤。团队还展示了产物可以进一步被氧化、耦合或转化为配体,而不会丧失其精细控制的三维构型。
从实验室方法到有用的分子构件
通俗地说,这项工作展示了如何用电力和单一钴催化剂,在原本简单且对称的起始分子上刻画出高度特异的三维形状。与其为每种手性结构设计不同的催化体系,不如用同一电化学平台直接生成多类具有两个远程控制点的手性产物。由于此类结构在畅销药物和先进催化剂中很常见,该策略为化学家提供了一种更直接、更高效且灵活的方式来构建复杂且对形状敏感的分子。
引用: Li, Y., Liu, S., Yuan, B. et al. Construction of remote dual stereocenters by electrochemical cobalt-catalyzed enantioselective desymmetrization. Nat Commun 17, 743 (2026). https://doi.org/10.1038/s41467-026-68437-w
关键词: 不对称催化, 电化学, 钴催化, 手性分子, 远程立体中心