Clear Sky Science · zh
使用多重Cas12a sgRNA在体内实现高特异性的改进基因敲除
更可靠的基因编辑
基因编辑为研究生物学、治疗疾病甚至控制害虫提供了新途径,但在真实动物体内,它往往没有头条报道那样干净利落。许多细胞逃避了编辑或仅被部分改变,这会模糊实验结果并限制实际应用。本文描述了一种在果蝇中基于CRISPR的新方法,使基因敲除更为完整且更精确,为在复杂生物体中实现更可靠的基因组编辑提供了蓝图。
为何传统CRISPR常常力不从心
传统的CRISPR工具如Cas9通常使用单个或少量导RNA在选定位点切割DNA。在活体动物中,这种方法面临若干障碍:有些导RNA本身效果差;有些靶位点酶难以接近;细胞的修复机制常常以微小改变“修复”断裂,但这些改变并未使基因失活。结果产生镶嵌现象:同一组织中相邻细胞可能携带不同的突变,或根本未被编辑。这种斑片式的编辑使得在基因真正被完全关闭时观察其作用变得困难,也给需在大多数细胞中高效发挥作用的应用(如基因疗法或基因驱动)带来挑战。
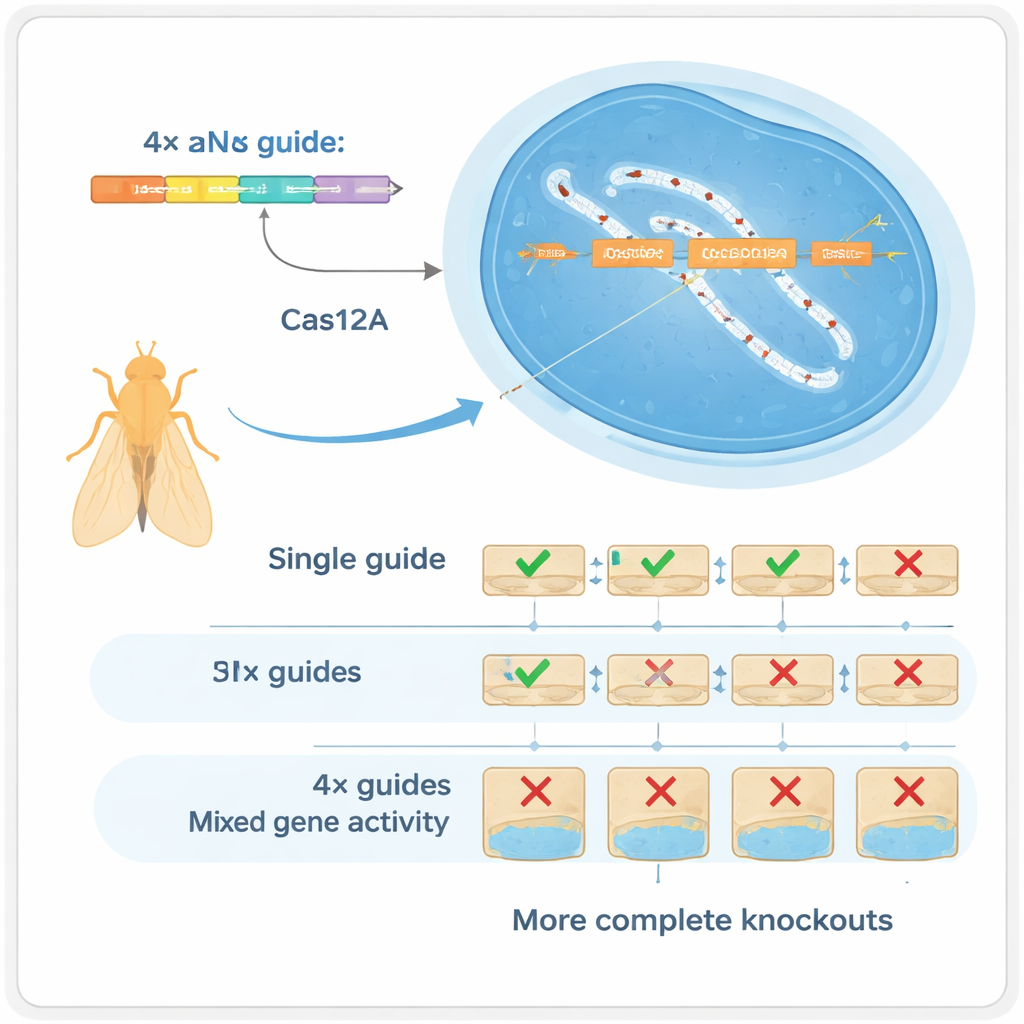
四个导向优于一个
作者转向了另一种CRISPR酶Cas12a,它比Cas9更容易处理紧凑的导向阵列。他们建立了一个果蝇工具箱,其中每个基因由一组四个导向RNA针对,所有导向都编码在单个可大量生产的小DNA片段上。在严控的测试中,他们显示每个基因使用四个导向会显著改变产生的DNA变体类型:系统不再主要产生单个位点的微小插入或缺失,而是频繁产生位点间的大型缺失,这些缺失几乎总是破坏基因功能。这种“多重化”通过两种方式发挥作用:若某个导向失败,其他导向可补位(冗余);若多个导向同时切割,则可移除基因更大片段(协同)。
高效性未伴随额外的附带损害
更多的DNA断裂显然带来安全方面的疑问:在一个区域内的多次切割会不会意外抹去邻近基因?导向在基因组其它部位误切的概率会不会增加?为此,研究者们测量了细胞死亡情况,调查了对邻近基因的影响,并设计了一种巧妙的测定方法来可视化染色体修复事件,即跨大范围DNA的杂合性丧失(loss of heterozygosity)。他们发现,在单个基因内聚集四处切口是可耐受的:与传统Cas9方法相比并未增加细胞死亡,且很少扰动邻近基因,除非导向非常靠近某个调控元件。对覆盖约三分之一果蝇基因组、超过2000个导向的大规模筛选显示,99%以上的导向阵列在预定靶点处是活性的,而可复现的脱靶活性低于1%,表明即便在多重化设置下也具有很高的特异性。
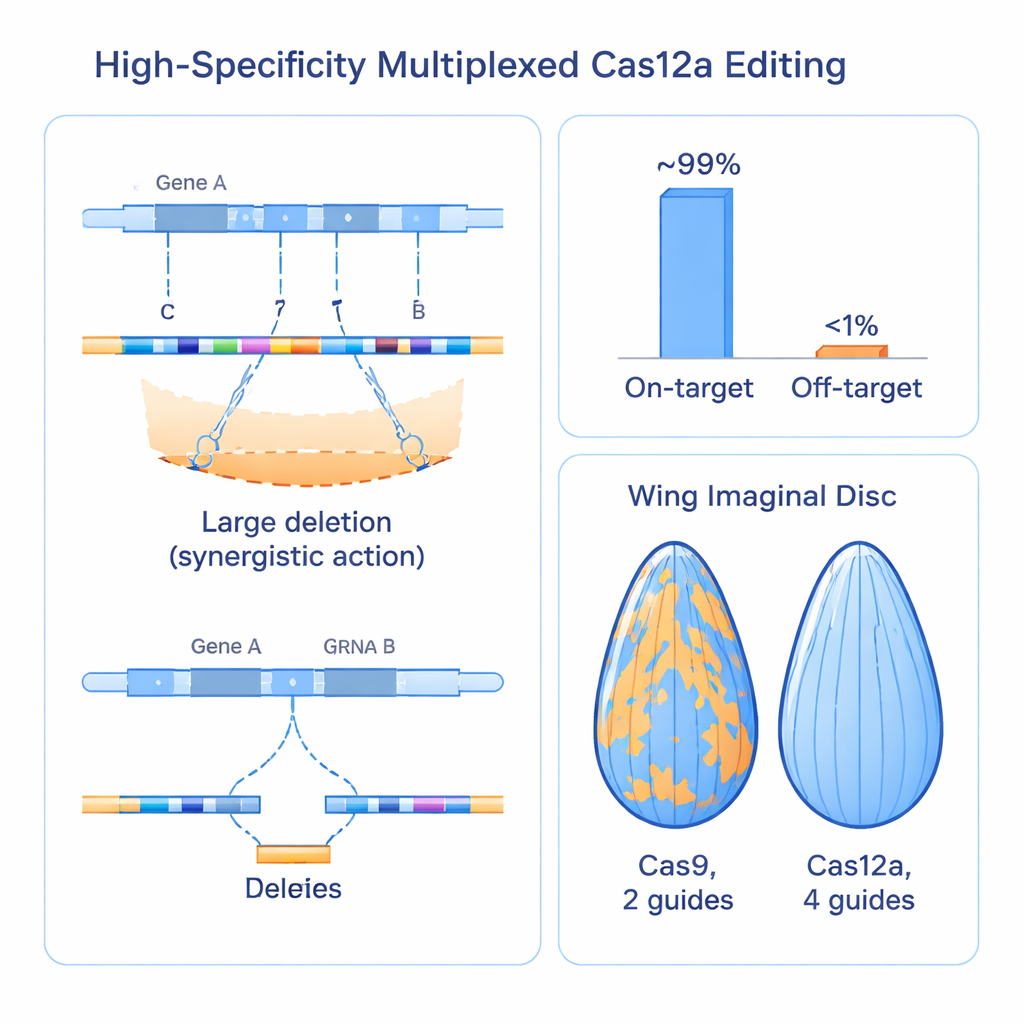
在真实组织中优于既有Cas9系统
为了检验这些分子学改进是否能转化为更清晰的生物学表型,团队将其Cas12a-四导向系统与广泛使用的Cas9资源直接比较,目标涵盖100多个基因。在眼、肠和发育中的翅等组织中,Cas12a方法产生了比Cas9更强、更均一的功能丧失效应,而Cas9常留下明显的未编辑正常组织斑块。以翅膀大小作为定量读数时,新系统持续地对已知调控基因产生更大且更可重复的生长缺陷,表明一些先前被评为微弱或非必需的基因,实际上是被旧工具未充分灭活而被漏检的。该方法的增强能力甚至揭示了名为trade embargo的基因在翅膀发育和生存中先前未知的必需作用。
对未来基因编辑的意义
简言之,这项工作展示了如何把CRISPR从有时杂乱的手术刀,转变为在活体动物中更果断地关闭基因的开关。通过将Cas12a与每基因四个导向结合,作者实现了几近完全的敲除且未观察到大量非预期效应,且该格式在规模化覆盖数百个基因时具有可行性。虽然该方法在果蝇中开发,但其基本原理——使用多个导向以获得冗余与协同,并仔细检测染色体副作用——具有广泛适用性。该策略可改进基础研究、提升基因筛选的分辨率,并为未来医学与生态学中基因编辑的更安全设计提供参考。
引用: Port, F., Buhmann, M.A., Zhou, J. et al. Improved in vivo gene knockout with high specificity using multiplexed Cas12a sgRNAs. Nat Commun 17, 877 (2026). https://doi.org/10.1038/s41467-026-68434-z
关键词: CRISPR, Cas12a, 基因敲除, 果蝇, 基因组编辑特异性