Clear Sky Science · zh
福氏志贺菌通过蛋白质ADP-吡咯烷化逃避由septin介导的细胞自主免疫
某些肠道细菌如何绕过我们的内部安保系统
由志贺菌引起的严重腹泻在全球仍是一个重大问题,尤以幼儿为甚。我们的细胞并非毫无防御:它们具有内置的工具,可以捕获并销毁入侵的微生物。本研究揭示了致痢性志贺菌福氏志贺菌如何利用精巧的分子手段拆解其中一项防御,从而帮助细菌在肠道内细胞间传播。
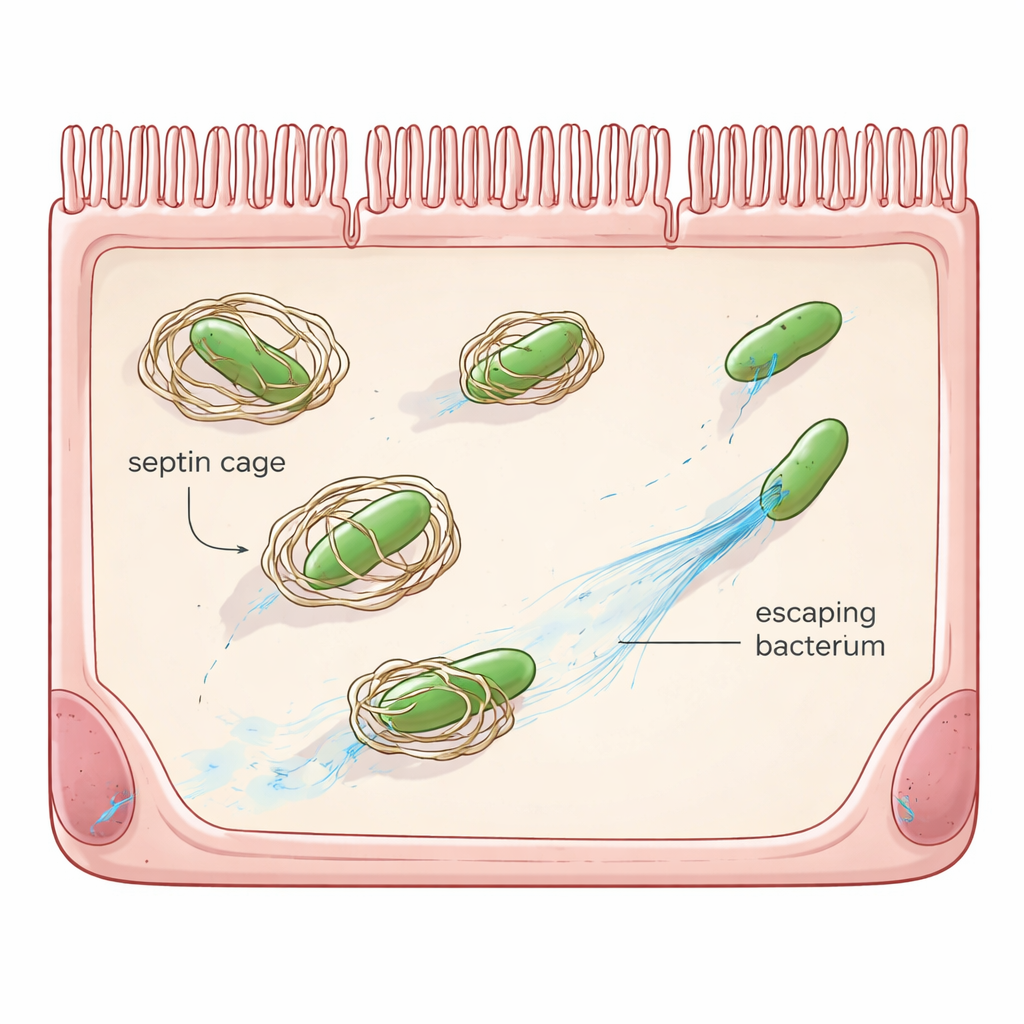
细胞的“自助”防御
除白细胞和抗体外,许多普通细胞还携带自身的应急安保系统,称为细胞自主免疫。其中一类系统依赖于septin——一组形成环状和笼状构架的支架蛋白。当志贺菌进入细胞并逃入细胞质时,septin可以在细菌周围组装,遏制其运动能力并将其标记以便被细胞回收途径销毁。先前的工作表明,志贺菌已有一种反制手段——一种名为OspG的蛋白,可将septin标记以促其降解。然而即便缺失OspG,大多数细菌仍能避免被困,这暗示志贺菌可能还有其他伎俩。
揭示第二种细菌破坏因子
作者将注意力转向志贺菌的另一组蛋白,即OspC家族。他们在人体细胞中采用全局蛋白图谱方法,寻找在OspC蛋白存在时发生化学修饰的宿主蛋白。除了已知的与蛋白质合成相关的靶点外,他们发现若干septin,尤其是名为SEPT9的蛋白,一直被标记。详细的生化测试表明,三种OspC蛋白可以直接将源自NAD的能量富集小标签附加到septin的多个位点上。这种化学变化称为ADP-吡咯烷化(ADP-riboxanation),是对更常见蛋白修饰的一种特殊且不可逆的变体。
从内部破坏蛋白质支架
为弄清这一化学标签如何削弱细胞防御,研究团队聚焦于SEPT9。septin通常形成由八个亚基有序连接的链,随后排列成丝状并最终在细菌周围形成功能完整的笼。研究者发现,在感染过程中,SEPT9上的一个特定位点——名为精氨酸561(arginine 561)的氨基酸,是ADP-吡咯烷化的主要位点。结构学研究和用纯化蛋白重建的实验显示,该位点位于两个SEPT9亚基相互锁定的关键接触面。当该精氨酸被化学修饰,或被替换成模拟所增加负电荷的残基时,八聚体链会解体为更小的片段,无法再构建稳定的丝状结构。
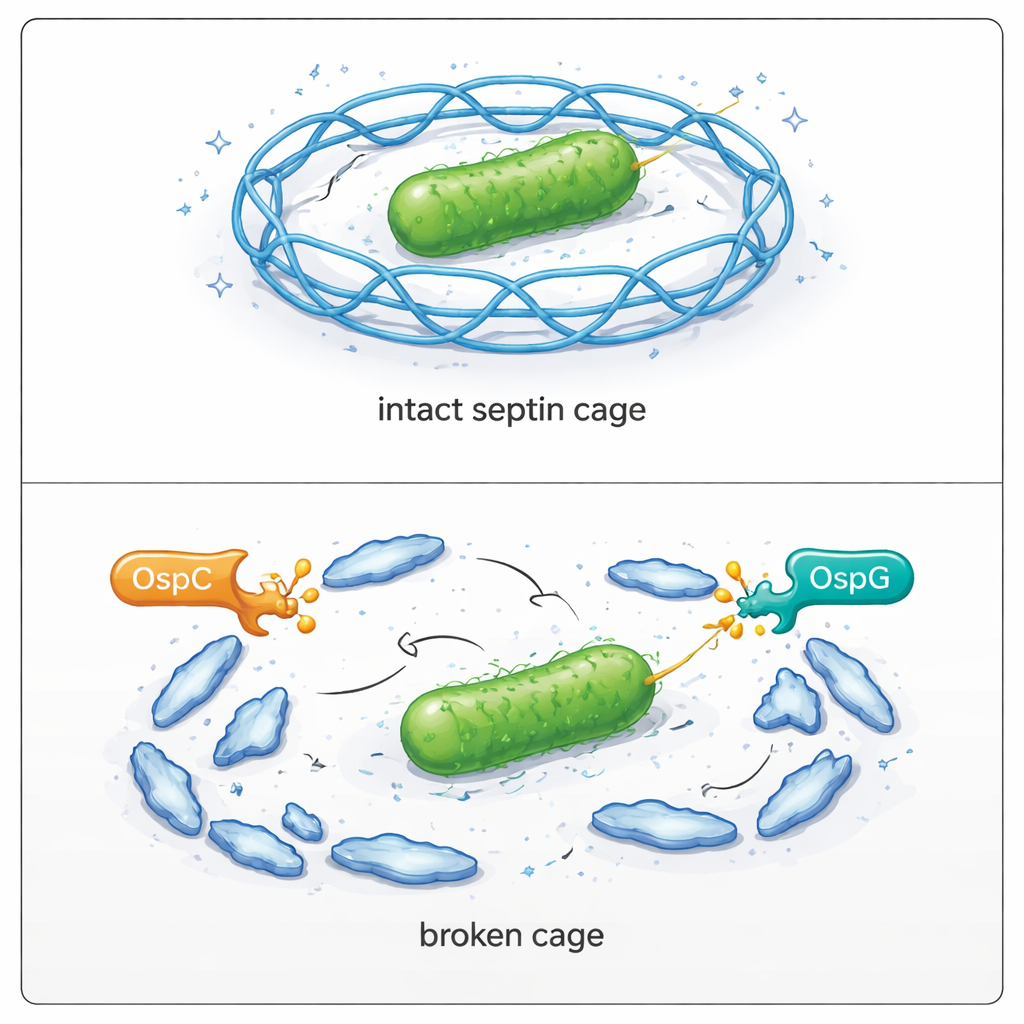
在被感染细胞内观察笼的崩溃
随后团队回到活细胞中观察其后果。在被野生型志贺菌感染的人类细胞里,只有少数细菌被septin笼困住。当所有OspC蛋白被基因删除时,被困细菌的比例几乎翻倍。移除OspG也产生了类似效果,而同时删除OspC和OspG则进一步提高了笼的形成,并严重削弱了细菌穿越细胞层扩散的能力。将活性OspC蛋白重新导入突变株后,这些菌株恢复了逃逸笼和复制形成大片病斑的能力。显微镜观察证实:当SEPT9在精氨酸561处不能被修饰时,它能有效参与笼的形成;而被OspC修饰时,细菌周围的笼形成显著下降。
这对抗志贺菌意味着什么
用通俗的话说,这项工作表明志贺菌携带一对配套的分子工具,专门用来撬开细胞内“监狱”的牢栏。OspC直接削弱构建septin笼所需的蛋白构件,而OspG则通过另一条化学途径促进其降解。两者协同使细菌得以逃脱、在细胞内移动并入侵邻近细胞。理解这些精确的逃逸机制不仅深化了我们对细胞内在免疫如何运作的认识,也指向了新的治疗思路:抑制OspC或保护关键septin接触面的药物,或可帮助恢复细胞捕获并清除这一危险病原体的天然能力。
引用: Tang, Z., Xian, W., Özbaykal Güler, G. et al. Shigella flexneri evades septin-mediated cell-autonomous immunity via protein ADP-riboxanation. Nat Commun 17, 1727 (2026). https://doi.org/10.1038/s41467-026-68425-0
关键词: 志贺菌, septin笼, 细胞自主免疫, 细菌毒力因子, ADP-核糖基化