Clear Sky Science · zh
使用 e2MPRA 同时进行表观基因组谱系分析与调控活性测量
读取细胞的隐秘开关
你体内的每个细胞几乎携带相同的 DNA,但脑细胞与肝细胞的行为却大相径庭。秘密在于短小的 DNA 片段,它们像基因的调光开关,能够将基因打开、调低或关闭。本研究引入了一种强大的新工具,称为 e2MPRA,允许科学家同时测试成千上万这样的开关,同时观察 DNA 在细胞内如何被包装和标记——这些都是理解发育、疾病风险以及为何某些遗传变体有影响而另一些没有的关键步骤。
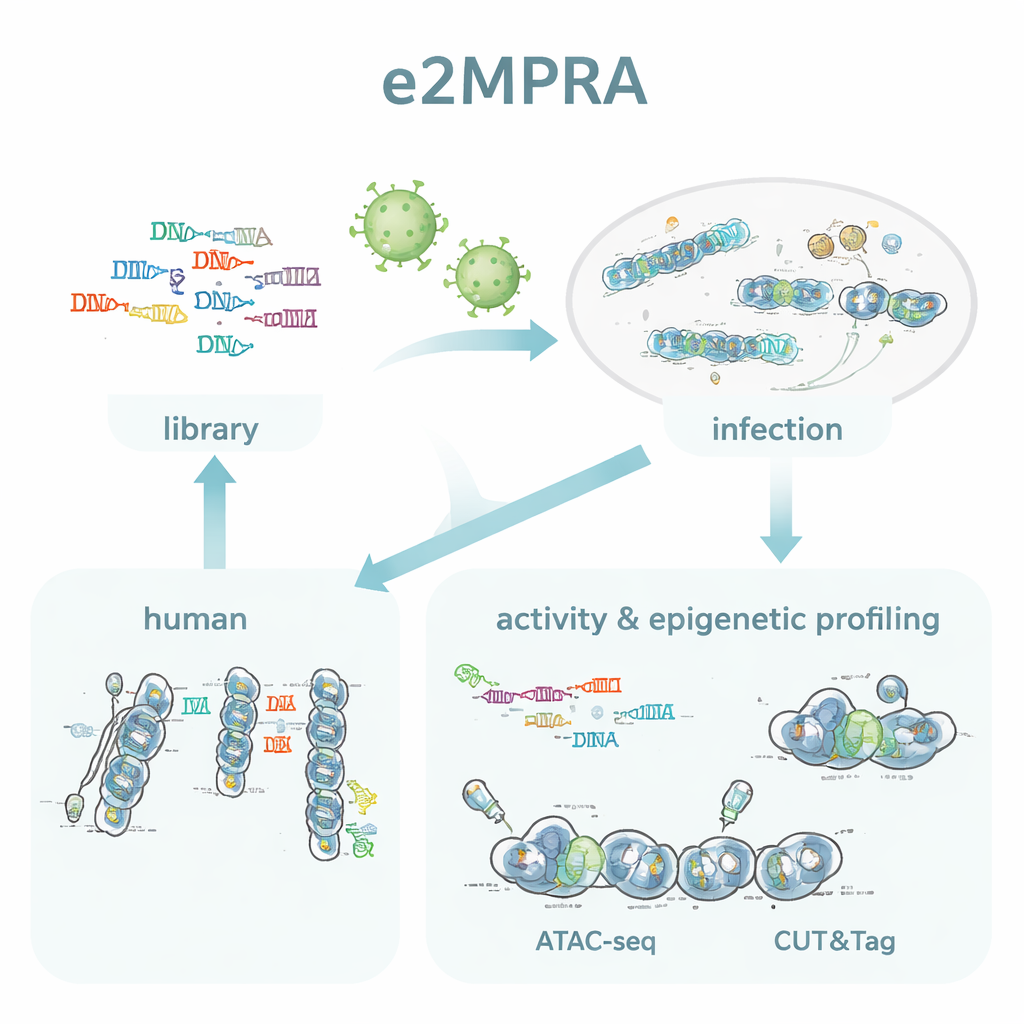
从 DNA 地图到 DNA 功能
过去十年,研究者绘制了大量“候选”调控开关的地图,也就是顺式调控元件(cis-regulatory elements)。他们使用的方法显示了 DNA 在何处松散(开放染色质)、哪些蛋白结合以及周围 DNA 上有哪些组蛋白修饰。这些地图很有价值,但大多是描述性的:蛋白结合或标记的出现并不能证明该序列真正控制基因活性。传统的大规模并行报告子测定(MPRAs)可以测试成千上万段 DNA 片段是否增强或抑制报告基因,但并不能告诉我们哪些蛋白在那里结合或伴随该活性发生了哪些表观遗传学变化。
一项兼具活性与表观标记的双重检测法
作者通过将慢病毒载体 MPRA 与两种表观基因组技术(ATAC-seq 和 CUT&Tag)结合,构建了 e2MPRA。首先,他们构建一个 DNA 文库,每个候选调控序列都连有一个短条形码,并置于一个最小启动子和报告基因旁。该文库随后被包装进慢病毒并多次整合到培养的人类细胞基因组中。从同一批细胞中,他们读取 RNA 中的条形码来测量调控活性,并使用 ATAC-seq 与 CUT&Tag 测量插入序列处的染色质可及性和一个关键的组蛋白标记(H3K27ac)。通过将这些信号标准化为每个序列实际整合的频率,他们在单次实验中获得了数千个元件的“开/关强度”和表观遗传状态的并列测量。
解码转录因子基序如何协同工作
为展示该技术的发现能力,团队从肝细胞中已知的转录因子基序构建了合成增强子。他们在中性 DNA 模板上以不同的数量和排列顺序布置这些基序。部分因子,如 HNF1A 和 XBP1,表现为典型激活子:增加拷贝数会提升报告子输出。另一些,如 HNF1A 与 ONECUT1,主要增强染色质可及性,符合其作为“先锋”因子打开闭合 DNA 的角色。PPARA 则显示不同的模式,单独强烈改变染色质与组蛋白标记但自身并不激活转录,然而它能与其他因子协同提升基因活性。已知的抑制因子 REST 在置于激活子旁时会抑制活性。值得注意的是,仅仅重新排列四个基序就能显著改变增强子强度,且激活子通常在更靠近启动子的位置发挥最佳作用,这揭示了这些基序排列中存在一种类似语法的结构。
精确定位多能性增强子中的敏感碱基
研究者随后转向对干细胞身份重要的增强子,聚焦于由多能性因子 POU5F1(也称 OCT4)和 SOX2 结合的区域。他们构建了密集突变文库,对 100 碱基对的增强子中的每个碱基进行系统性改变,并对大小为六碱基的小窗口进行随机重排。在诱导多能干细胞中使用 e2MPRA,他们能够观察哪些突变削弱或增强报告子活性,以及这些突变如何影响染色质可及性和乙酰化。破坏 POU5F1::SOX2 结合基序常常同时降低基因活性和表观标记,证实了其核心作用。在 POU5F1 基因附近一个研究透彻的增强子中,他们还发现改变 YY1 基序会增加转录但降低染色质开放性,这提示某些因子可能一方面促进开放状态,另一方面仍限制表达。
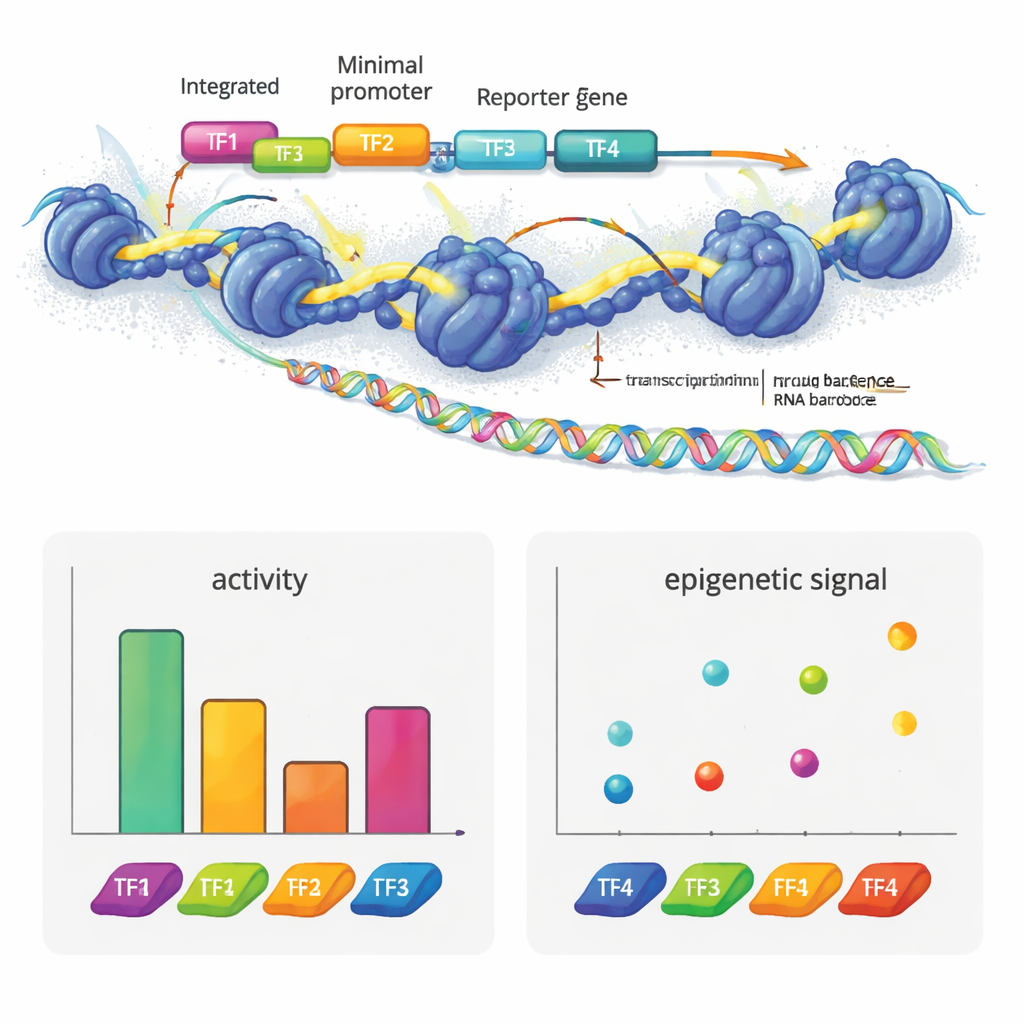
这对基因与疾病意味着什么
e2MPRA 并不能完美再现基因组天然三维连线的所有细节,但它提供了一种实用的方法,在相同条件下比较成千上万条调控序列与变体。通过将功能性读数(DNA 片段驱动基因的强度)与表观遗传读数(该 DNA 如何被包装和标记)耦合,该方法有助于揭示为何某些转录因子基序、组合与位置如此关键。长期来看,像 e2MPRA 这样的工具可使解读与疾病相关的非编码遗传变体更容易,设计用于基因疗法的合成增强子更可行,并建立一个更完整的“调控代码”,将 DNA 序列与细胞行为连接起来。
引用: Zhang, Z., Georgakopoulos-Soares, I., Bourque, G. et al. Simultaneous epigenomic profiling and regulatory activity measurement using e2MPRA. Nat Commun 17, 1724 (2026). https://doi.org/10.1038/s41467-026-68422-3
关键词: 基因调控, 增强子, 表观遗传学, 转录因子, 功能基因组学