Clear Sky Science · zh
DNA 末端构型决定 NHEJ 介导的末端桥接过程中突触复合体的形成
当 DNA 断裂时,细胞必须迅速决策
我们的细胞中,DNA 每天都会因正常代谢和环境应激而出现划伤、切割和损伤。其中最危险的损伤之一是双链断裂,即 DNA 双螺旋的两条链同时断开。如果这些断裂不能快速且准确地修复,细胞可能死亡,或更糟的是走向癌变。该研究探讨了断裂 DNA 末端的精确形状和化学性质如何影响一个关键修复途径——非同源末端连接(NHEJ)——是否能高效且尽量少出错地将这些末端牵引在一起。
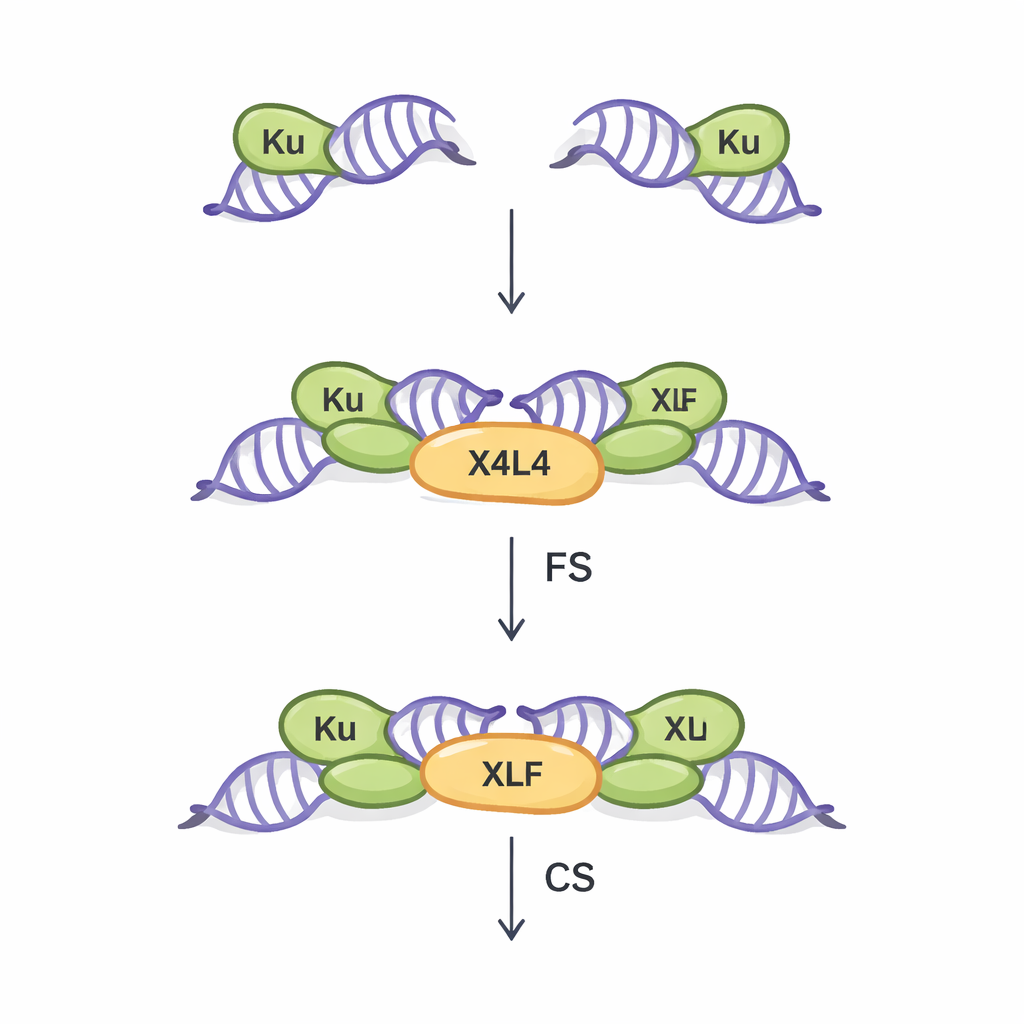
把断裂的 DNA 拉到一起的两种方式
NHEJ 是大多数体细胞修复双链断裂的主要途径。它不依赖匹配的 DNA 模板,因此速度快但有一定错误概率。该途径的第一个关键步骤称为突触(synapsis):将两端断裂的 DNA 物理性地桥接起来,以便随后连接。先前的研究主要使用理想化的钝端 DNA,揭示出两种突触装配形式。在“可变突触”(flexible synaptic,FS)状态中,末端被保持在彼此附近并可相对移动,探寻配对方式。在“紧密突触”(close synaptic,CS)状态中,末端端对端对齐,已准备好被连接酶封合。三个核心蛋白——Ku、XRCC4–Ligase IV(合称 X4L4)和 XLF——已知协调该过程,但真实世界中不规则的 DNA 末端如何影响哪种突触状态形成仍不清楚。
末端形状与短片段配对引导修复路径
研究人员使用单分子 FRET,一种基于荧光的纳米尺度距离追踪技术,观察单个 DNA 分子在 NHEJ 蛋白作用下被牵引到一起的过程。他们将简单的钝端与更现实的具有短单链悬垂(即可配对的小尾巴)的末端进行了比较。结果发现,当悬垂互补时,即使只有几个碱基,也会大幅提高形成紧密突触复合体的几率。事实上,仅三对“微同源”配对碱基就足以使 Ku 和 X4L4 单独构建出稳定的 CS 复合体,而无需 XLF。这表明 DNA 本身可以提供部分能量和方向性,通常由辅助蛋白提供。
微小 DNA 翻瓣如何帮助稳定桥接
通过分析不同的 FRET 特征,团队发现对于有悬垂的末端,紧密突触状态至少存在两种结构形式。在一种形式中,悬垂的最顶端彼此配对,形成带缺口或断裂的接头。在另一种形式中,双链 DNA 与单链悬垂的交界处沿轴线紧贴,而悬垂向外翻折成小翻瓣。这些翻瓣仍然允许碱基配对并将末端保持在极近的距离,从而可能稳定复合体,并为酶在最终封合前修剪或延长 DNA 留出空间。有趣的是,悬垂中常见的氧化损伤(如 8-氧代鸟嘌呤)对该过程影响有限,突显了 NHEJ 对某些损伤形式的稳健性。
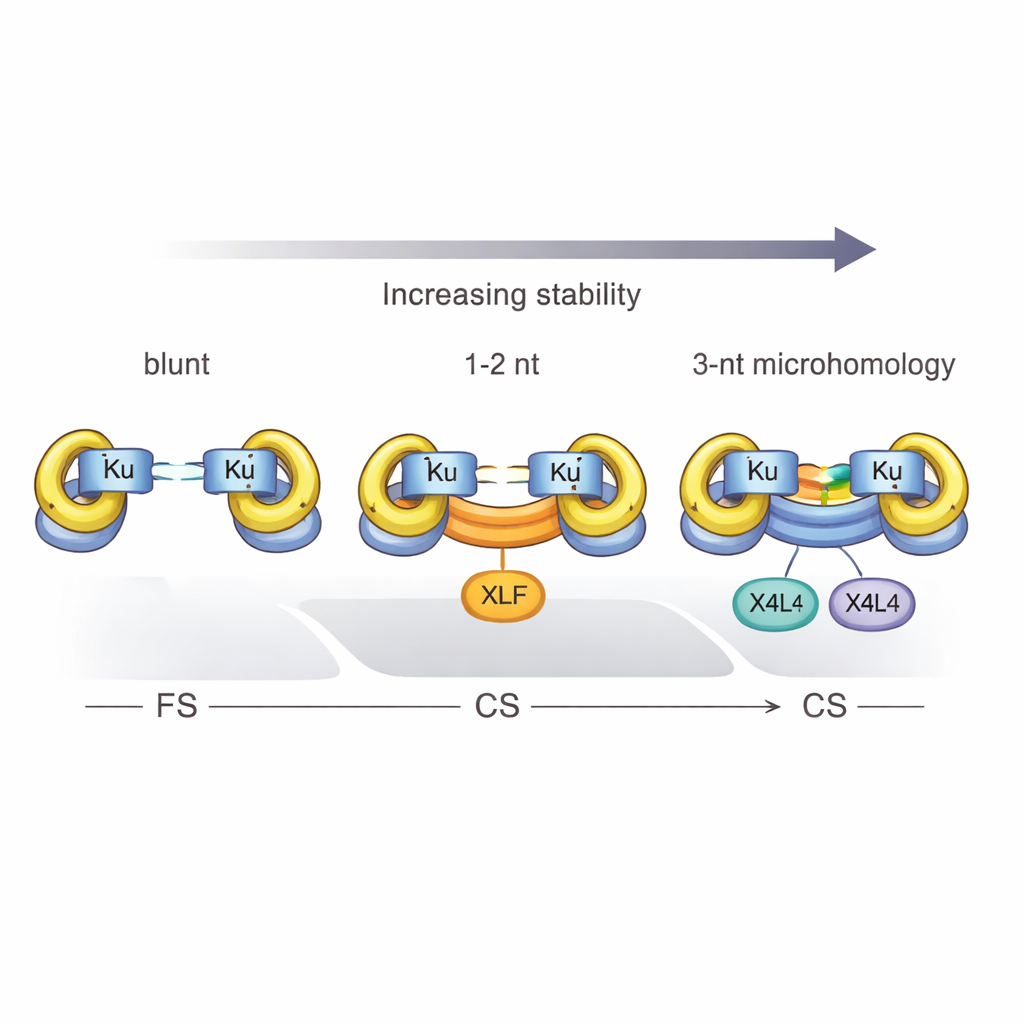
蛋白、磷酸和“三”的力量
研究还确定了一个明确阈值:至少需要三个互补碱基,Ku 和 X4L4 才能可靠地将可变复合体转换为紧密复合体。如果只有一对或两对匹配,系统大多停留在可变状态,除非 XLF 参与进来帮助夹紧末端。化学细节也很重要。当断裂 DNA 带有 5′ 磷酸基——许多生理性断裂的常见特征时,突触效率提高,紧密复合体更可能被真正连接,使暂时的桥接转为永久修复。然而,这种磷酸的促进作用无法完全替代断裂处碱基配对带来的稳定作用。
这对健康与基因组编辑意味着什么
通俗地说,这项工作表明断裂的 DNA 末端并非被动等待修复的对象。其精确的形状、微小的匹配序列片段和化学标记会积极引导修复蛋白如何抓取、对齐并重新连接它们。当存在三个或更多匹配碱基时,DNA 末端自身有助于将断裂锁定在可修复的配置中,有时使某些辅助蛋白变得可有可无。当此类匹配稀少时,额外的蛋白因子就变得必不可少。这些发现有助于解释为何有些断裂能被整洁修复,而另一些会导致小的突变或重排。它们也为改进 CRISPR 等基因组编辑工具提供线索:这些工具故意制造的断裂由相同的 NHEJ 机器修复。通过调控这些断裂的末端,科学家或可更好地控制基因组被重塑的方式。
引用: Zhang, C., Jin, W., Jiang, Y. et al. DNA end configurations dictate synaptic complex formation during NHEJ-mediated end bridging. Nat Commun 17, 1720 (2026). https://doi.org/10.1038/s41467-026-68417-0
关键词: DNA 双链断裂修复, 非同源末端连接, DNA 同步连接(synapsis), 微同源序列, 基因组稳定性