Clear Sky Science · zh
用于机会性筛查、分期和进展风险分层的多模态脂肪性肝病人工智能
为什么肝脏脂肪与瘢痕对所有人都重要
脂肪性肝病已不再罕见或小众:全球约三分之一的成年人肝脏有过多脂肪,而且这一比例还在上升。对许多人来说它无声无息,但对另一些人则会导致危险的瘢痕(纤维化)、肝硬化、肝癌和心血管问题。与此同时,数以百万计的人因胸痛、肿瘤随访或常规体检等原因已经接受 CT 扫描,但没人仔细查看他们的肝脏。本研究提出了一个简单而有力的问题:人工智能(AI)是否可以在现有影像中默默扫描、标出隐匿的肝脏疾病,并帮助医生在严重损害出现前采取干预?
基于真实医院数据构建的新型 AI 助手
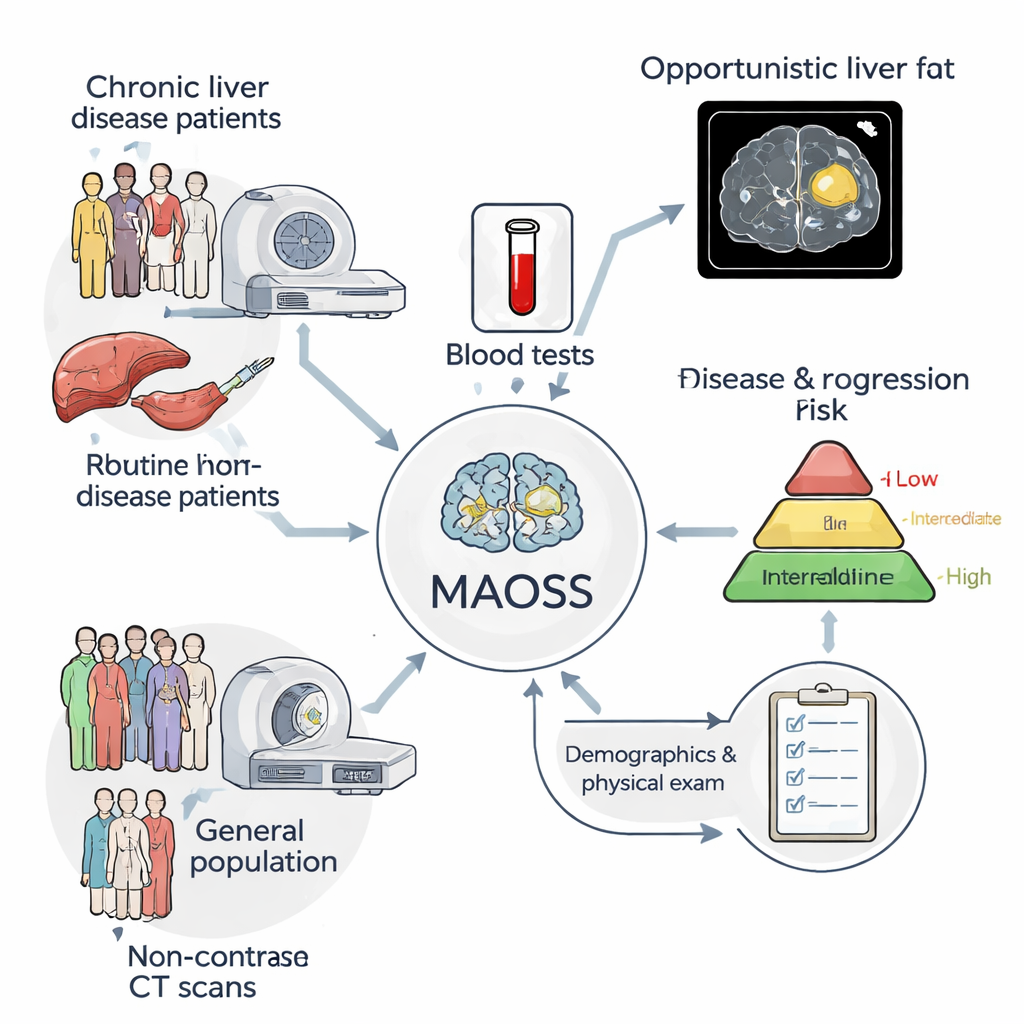
研究者开发了一个名为 MAOSS(多模态机会性肝脏脂肪筛查人工智能)的多模态 AI 系统。它不依赖单一信息源,而是结合三类数据:肝脏的三维非增强 CT 影像、常规血液化验结果以及年龄和体型等基础临床信息。团队用来自一家大型中国医院的 2000 多例患者数据训练该系统,其中近 1000 例具有显微镜下的肝组织检查(即金标准),另有超过 1100 例具有详尽的放射学报告。这种混合标签让 AI 能同时从最精确的活检标签和临床日常中更易获得的放射报告中学习。
教 AI 识别脂肪与瘢痕
MAOSS 的设计旨在从每次 CT 扫描中回答两个关键问题:肝脏中有多少脂肪(脂肪变性),以及任何纤维化发展到何种程度。为此,模型将疾病分期视为有序阶梯——从无、轻度、中度到重度——并学习把每位患者放在正确的梯阶上。其特殊的“多模态”结构能够灵活处理缺失信息;例如在部分血检缺失时仍能运行并更依赖影像数据。研究者还加入了一种基于“综合梯度”的解释工具,能突出影像中最强影响 AI 决策的肝脏区域和密度,向临床医生提供可疑脂肪改变的热图。
MAOSS 与现有工具的性能比较
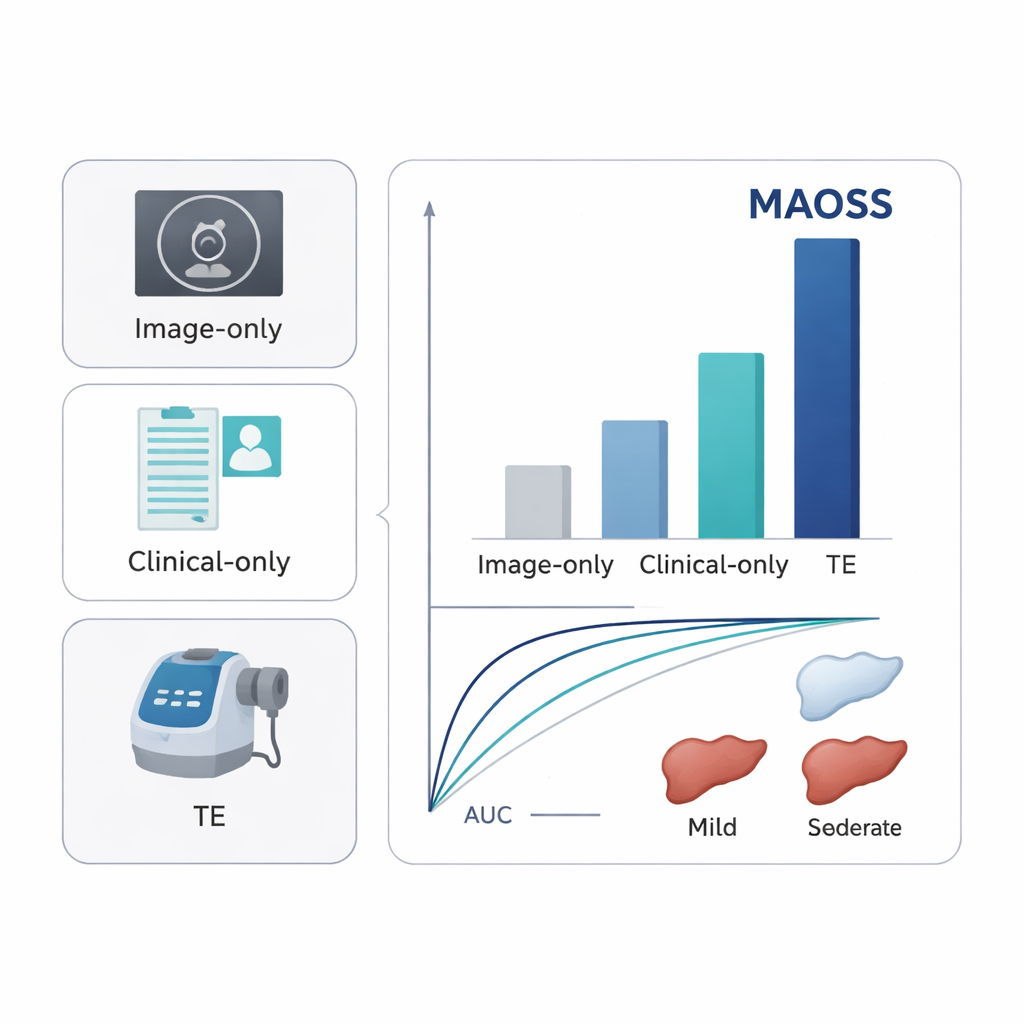
在来自多家医院的独立患者队列(包括外部队列和一组基于 MRI 的肝脏脂肪测量队列)上测试时,MAOSS 在检测即便是轻度肝脂肪方面表现出高准确性,受试者工作特征曲线下面积(AUC)约为 0.90–0.93。它在识别临床重要纤维化方面也表现良好,AUC 约为 0.82–0.89。这些分数持续优于仅用影像、仅用临床数据或标准超声相关测量(如瞬时弹性成像)的模型。在一项包含 11 位放射科医生的读片研究中,MAOSS 作为辅助工具:当医生在查看 CT 的同时看到 AI 评分时,他们识别早期脂肪肝的能力明显提高,尤其是在区分正常肝脏与轻微病变方面。
将常规扫描变为早期预警网络
团队接着考察 MAOSS 在日常医疗混乱现实中的可行性。他们将系统应用于来自急诊、住院、门诊和体检中心的超过 18,000 例真实 CT 扫描,其中大部分最初并非因肝脏问题而下单。MAOSS 对“脂肪肝”与“非脂肪肝”的评估与放射科报告高度一致,尤其在大型体检人群中更为接近。随后,他们将 MAOSS 接入一条既定的临床指南,以决定哪些脂肪肝患者应转诊专科。在一组 1192 人的活检确证人群中,MAOSS 增强的路径比单纯基于超声测量的标准方法多识别出约三分之一有进展为脂肪性肝炎或晚期纤维化风险的患者,同时仍能安全地排除低风险个体。
这对患者和未来医疗意味着什么
对非专业读者而言,关键结论是:现有为其他健康问题而做的 CT 扫描可以兼作肝病的无声筛查系统,无需额外就诊或侵入性操作。通过自动同时读取 CT 影像与常规血检,MAOSS 能比传统方法更早发现脂肪肝和令人担忧的纤维化,帮助放射科医生看到他们可能会忽视的细微病变,并更准确地将患者分为低、中、高三档进展风险。作者也指出需要更大规模、长期随访的研究且该 AI 并非完美,但结果表明多模态 AI 有望成为在病情无声恶化前预防严重肝病的重要工具。
引用: Gao, Y., Li, C., Chang, W. et al. Multi-modal AI for opportunistic screening, staging and progression risk stratification of steatotic liver disease. Nat Commun 17, 1562 (2026). https://doi.org/10.1038/s41467-026-68414-3
关键词: 脂肪性肝病, 医疗人工智能, CT 成像, 肝纤维化, 机会性筛查