Clear Sky Science · zh
分层机制控制因 DNA 损伤阻滞的 RNA 聚合酶 II 的清除
当基因复制机器遇到障碍
每一秒,数以百万计的微小分子机器——RNA 聚合酶 II——在我们的 DNA 上穿行,将基因信息转录为 RNA。但当 DNA 受损时,例如被阳光中的紫外线照射,这些机器可能会停转。如果被阻滞的聚合酶堆积,细胞将无法正常读取基因,这对脑细胞尤其危险,可能导致像库肯海纳综合征这样的罕见疾病。本研究详细揭示了细胞如何感知这些被阻滞的机器,并在它们造成持久危害之前选择重新启动或将其移除。
观察细胞“交通堵塞”的新方法
为了解细胞如何清除被阻滞的聚合酶,研究人员构建了一个时间分辨的转录“摄像头”。他们使用一种药物,让现有的 RNA 聚合酶 II 可以继续前进但阻止新的聚合酶起始,并在每个细胞核内制造一个微小的紫外损伤斑点。通过追踪活性形式聚合酶上的特定化学标记,他们可以观察该标记在受损区域相对基因组其它部分消失的速度。同时,他们开发了一个配套检测,用来测定细胞提取物中活性聚合酶的总量,这不仅显示聚合酶何时离开 DNA,还显示何时被细胞的降解系统拆解。
为被阻滞的机器标记以便移除
团队聚焦于转录耦合修复,这是一种专门修复正在被读取基因上的损伤的修复系统。他们使用一组相匹配的人类细胞系,每个细胞系缺失不同的修复因子。两个蛋白——CSB 和 CSA——被发现是决定性的把关者。当任一蛋白缺失时,RNA 聚合酶 II 在损伤位点累积并顽固地滞留,细胞无法降解它。在生化层面上,这些细胞也不能在聚合酶的关键位点连接小型的泛素标签。相比之下,缺失后期修复蛋白(那些切除并替换受损 DNA 的蛋白)的细胞仍能正常清除聚合酶。这表明,对被阻滞聚合酶的初始泛素标记是决定其命运的关键触发信号。
两支清理队:一支快速,一支备用
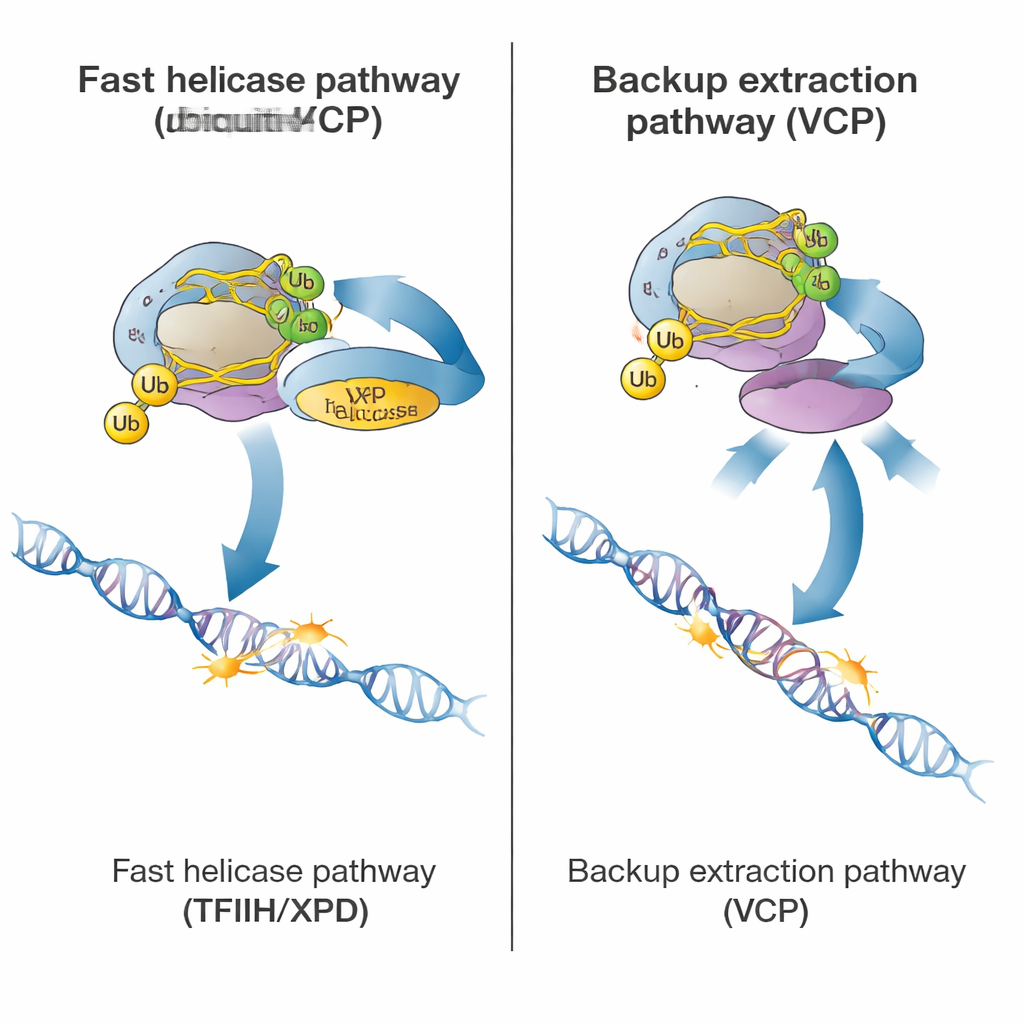
一旦聚合酶被标记,细胞可以在两种清除方式之间选择。主要的快速途径依赖于一个大型修复复合物 TFIIH,尤其是其 XPD 解旋酶亚基,后者利用能量来解开 DNA。辅助蛋白,包括 ELOF1、UVSSA 和 STK19,将 TFIIH 带到被阻滞的聚合酶处,并将 XPD 定位在其前方的 DNA 上。通过在携带解旋酶失活型 XPD 突变的患者细胞中使用新检测,作者表明当 XPD 无法解旋 DNA 时,聚合酶的清除显著变慢,尽管其余修复机器仍在位。这表明 XPD 的机械拉动作用通常是将聚合酶从损伤处“震”松,以便修复酶能接近并处理受损位点。
缓慢但至关重要的备用方案
研究还揭示了一条更慢的应急清除途径。该途径依赖于 VCP(又名 p97),一种识别泛素标签并能强行从染色质中提取蛋白的蛋白质。在 TFIIH 完全正常的健康细胞中,阻断 VCP 只有轻微影响。但在 TFIIH 缺失、定位异常或解旋酶失活的细胞中,聚合酶的清除几乎完全依赖于 VCP。在这些情况下,即使正常修复无法继续,VCP 仍能将被标记的聚合酶从 DNA 上拉走并送去降解。关键是,这条备用途径仍然需要一定的泛素标记,这也解释了为什么缺失 CSB 或 CSA 的细胞——因此缺少泛素标记——在主路径和备用路径中都会失败。
这对健康和疾病意味着什么
综合起来,这项工作勾勒出当 RNA 聚合酶 II 遇到 DNA 损伤时细胞采用的一套分层安全程序。首先,CSB 和 CSA 用泛素标记被阻滞的机器。如果一切正常,TFIIH 及其 XPD 解旋酶会迅速将聚合酶移开,以便切除并修复损伤。若 TFIIH 无法完成其工作,VCP 会介入,提取聚合酶并将其送去降解,从而防止其阻塞基因表达,尽管 DNA 损伤本身仍然存在。该框架有助于解释为何 CSB 或 CSA 的遗传缺陷会导致特别严重的神经系统问题:缺乏泛素标记会使细胞失去主要的修复驱动通路和备用的提取通路,导致被阻滞的聚合酶卡在受损基因上,转录长期受阻。
引用: van der Meer, P.J., Yakoub, G., Tsukada, K. et al. Hierarchical mechanisms control the clearance of DNA lesion–stalled RNA polymerase II. Nat Commun 17, 1647 (2026). https://doi.org/10.1038/s41467-026-68413-4
关键词: 转录耦合 DNA 修复, RNA 聚合酶 II, 紫外线诱导的 DNA 损伤, 蛋白质泛素化, 库肯海纳综合征