Clear Sky Science · zh
在原位可视化艰难梭菌在肠道感染过程中表现型异质性与单细胞形态
为什么肠道细菌的行为各不相同
艰难梭菌(通常称为C. diff)是医院中臭名昭著的病原体,在抗生素扰乱肠道正常微生物后可引起严重、甚至危及生命的腹泻。然而即便这些细菌遗传上相同并处于相同环境,单个细胞的行为仍可以大相径庭。这项研究以前所未有的细节显示了单个C. diff细胞在感染小鼠肠道过程中如何开启或关闭毒素产生,甚至改变形态,为解释该疾病为何顽固难治提供了线索。
实时追踪危险的肠道入侵者
为了解体内单个C. diff细胞的行为,研究人员需要在密集且多样的肠道微生物群中清晰地看到它们。他们构建了持续在显微镜下发出鲜亮颜色的C. diff菌株,使用不会干扰细菌生长或致病能力的特殊荧光蛋白。通过用这些发光菌株感染经抗生素处理的小鼠,然后切片并染色结肠,他们能够在完整的肠组织中精确定位并观察数千个单个细菌细胞的位置和行为。 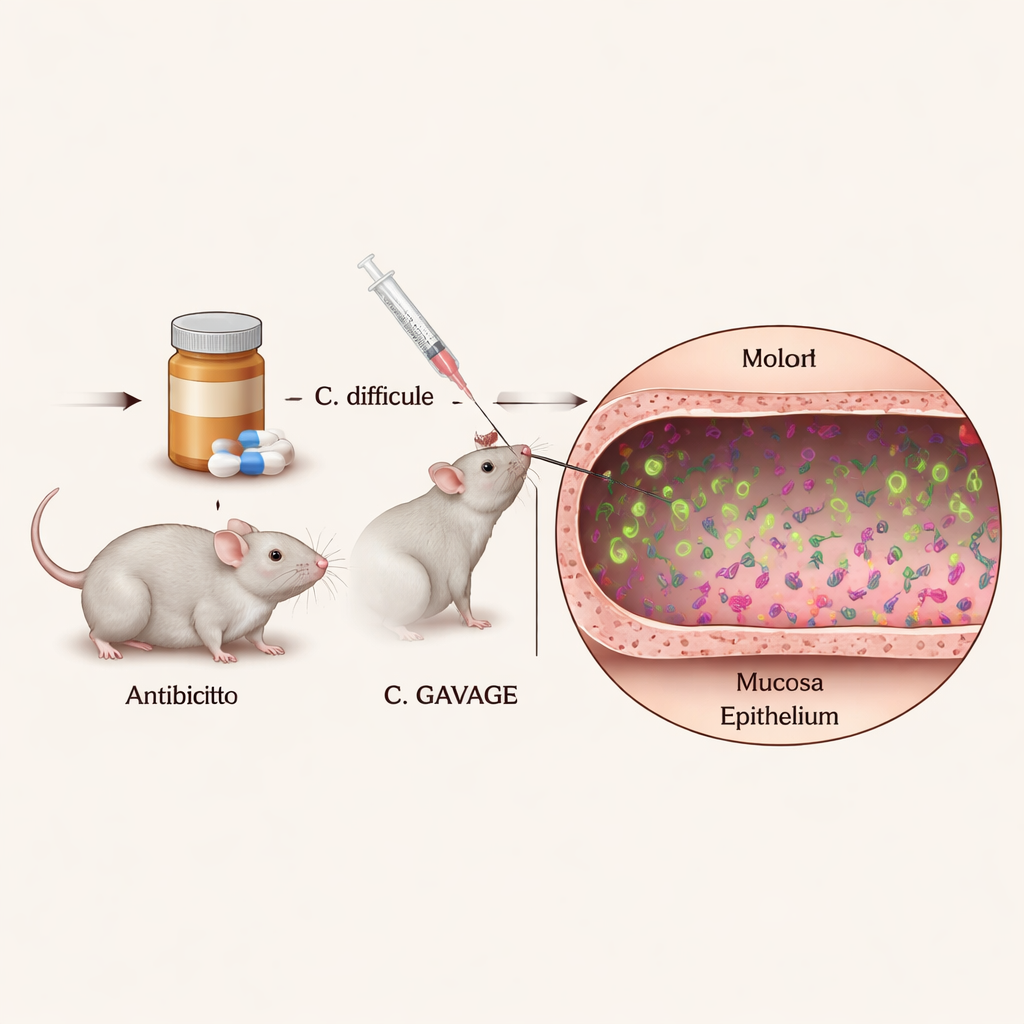
细菌在结肠中的居所
图像显示大多数C. diff细胞位于结肠内容物的中心,即腔内,证实该生物主要是一种自由漂浮的“腔内”病原体。然而,一小部分细胞持续出现在粘液层附近并紧贴上皮表面——上皮是覆盖结肠并作为与外界隔离的薄细胞层。在免疫系统正常的常规小鼠中,这种近接接触的亚群之前并不明显。重要的是,工程化的荧光标签在动物体内并未明显削弱细菌,这意味着这些图像很可能反映了C. diff在真实感染中的行为。
谁产生毒素,在哪里产生?
研究组随后加入了第二种荧光信号,只有在C. diff启动其毒素基因时才会亮起。毒素是损伤肠道黏膜并驱动疾病症状的有害蛋白,也是医生在粪便检测中用于诊断感染的指标。令人意外的是,细菌并非同时全部产生毒素。相反,在感染的早期和晚期,只有一部分细胞在任何时点显示“毒素开启”。在一个被遗传改造为过度产生毒素的突变株中,这一比例更高,但即便如此也并非所有细胞都参与。另外显著的是,细胞的位置——漂浮在腔内、停留在粘液中或接触上皮——并未强烈改变毒素产生的频率或这些基因的表达强度。 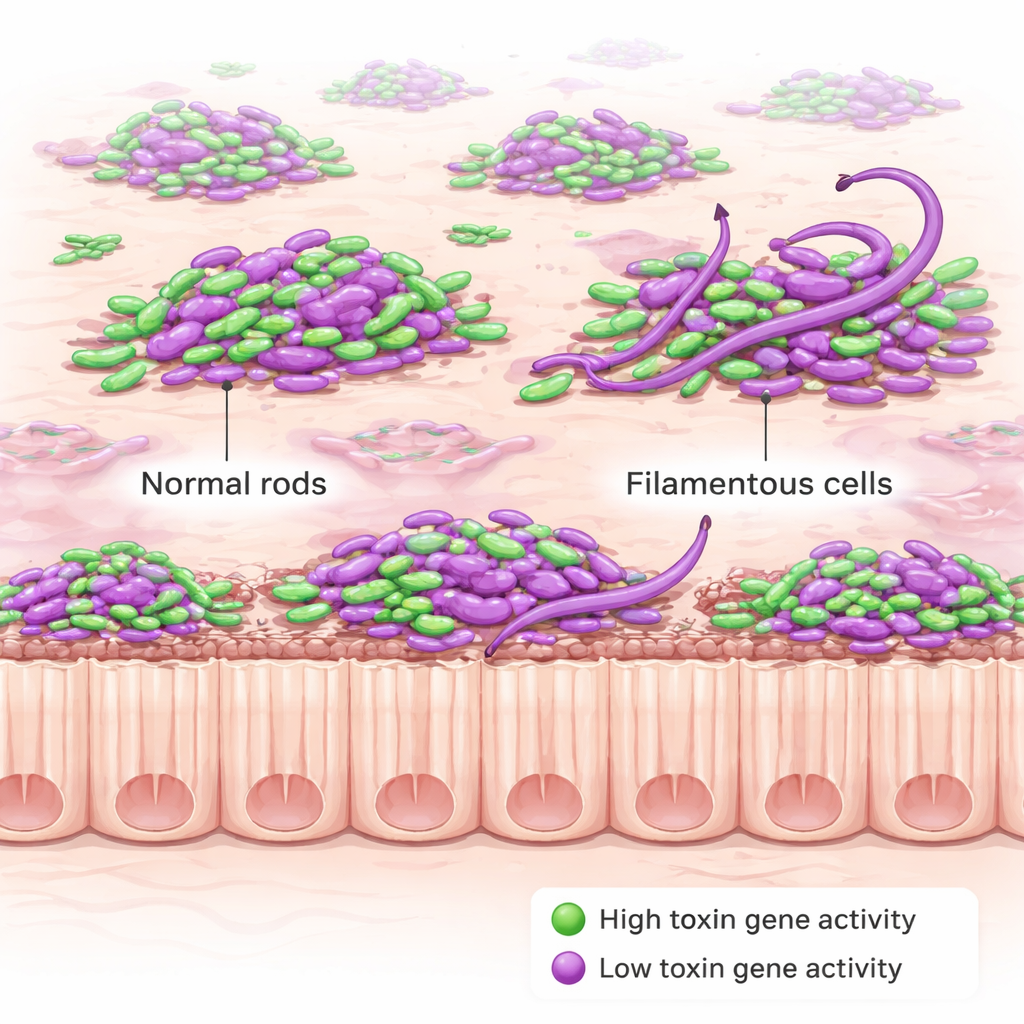
受压下的形态转换细胞
在绘制毒素产生的同时,研究人员意外发现了一种新的行为。在被毒素过度表达突变株感染的小鼠中,急性期许多C. diff细胞变成异常长的弯曲丝状体,有些长度超过正常短杆形的十倍以上。这种“线状”形态主要出现在早期的严重感染期,并在后期减弱;在同一菌株的实验室培养基中并未出现。这提示是发炎肠道内的压力条件——而非仅仅遗传改变本身——触发了这种剧烈的重塑。后续实验显示,丧失一种称为RstA的调控蛋白(它同时控制毒素基因和其他应激反应)会促成这种丝状形成。
这对艰难梭菌疾病意味着什么
对非专业读者来说,关键结论是即便是单一菌株的C. diff也像一支分工的队伍。有些细胞承担能量成本去产生毒素并破坏肠道,释放出的养分可以被不产生毒素的邻近细胞利用。这种共同的“分工”可能帮助感染持续并反弹,因为并非每个细胞对针对毒素或针对快速生长细菌的治疗同样敏感。新开发的发光报告系统为科学家提供了一种强有力的方法,可逐细胞观察C. diff及相关肠道微生物随时间和空间在体内的适应方式。这一洞见最终可能指导出不仅仅杀死细菌的治疗策略,而是针对驱动疾病和复发的特定亚群的有害作用进行干预。
引用: DiBenedetto, N.V., Donnelly-Morell, M.L., Kumamoto, C.A. et al. In situ visualization of Clostridioides difficile phenotypic heterogeneity and single-cell morphology during gut infection. Nat Commun 17, 1716 (2026). https://doi.org/10.1038/s41467-026-68411-6
关键词: 艰难梭菌, 肠道微生物组, 细菌毒素, 表现型异质性, 荧光成像