Clear Sky Science · zh
一种纳米系统靶向基质金属蛋白酶组织抑制因子‑1以实现持续时空特异性特发性肺纤维化疗法
为什么顽固的肺部瘢痕很重要
特发性肺纤维化(IPF)是一种进展性肺病,正常的多孔肺组织逐渐被僵硬的瘢痕组织取代。患有IPF的人在日常活动中会出现气短,确诊后多数患者只能存活几年。现有药物能在一定程度上放缓病情进展,但很少能逆转既有瘢痕,而且常伴随副作用。本研究探索了一种智能吸入式“纳米治疗”策略,目标不仅是减缓IPF,还要主动清除瘢痕组织并促进肺组织自我修复。
问题所在:粘性的瘢痕和化学应激
在IPF中,氧气进入血液的空间被过量蛋白质如胶原蛋白填满,使本应柔软的气囊变成僵硬的斑块。作者把注意力集中在一种名为TIMP‑1的蛋白上,它像刹车一样抑制能够分解过量胶原的天然酶。通过分析患者及经诱导产生肺纤维化的小鼠肺样本,他们发现TIMP‑1水平比健康肺高出数倍,并且随着胶原沉积增加而上升。同时,受损肺组织显示活性氧(ROS)水平激增——这些化学“火花”会损伤细胞——并伴随健康气囊上皮细胞关键标志物的丧失。综合来看,这些发现指向一个恶性循环:过多的TIMP‑1减慢了瘢痕分解,而氧化应激进一步破坏肺组织结构。
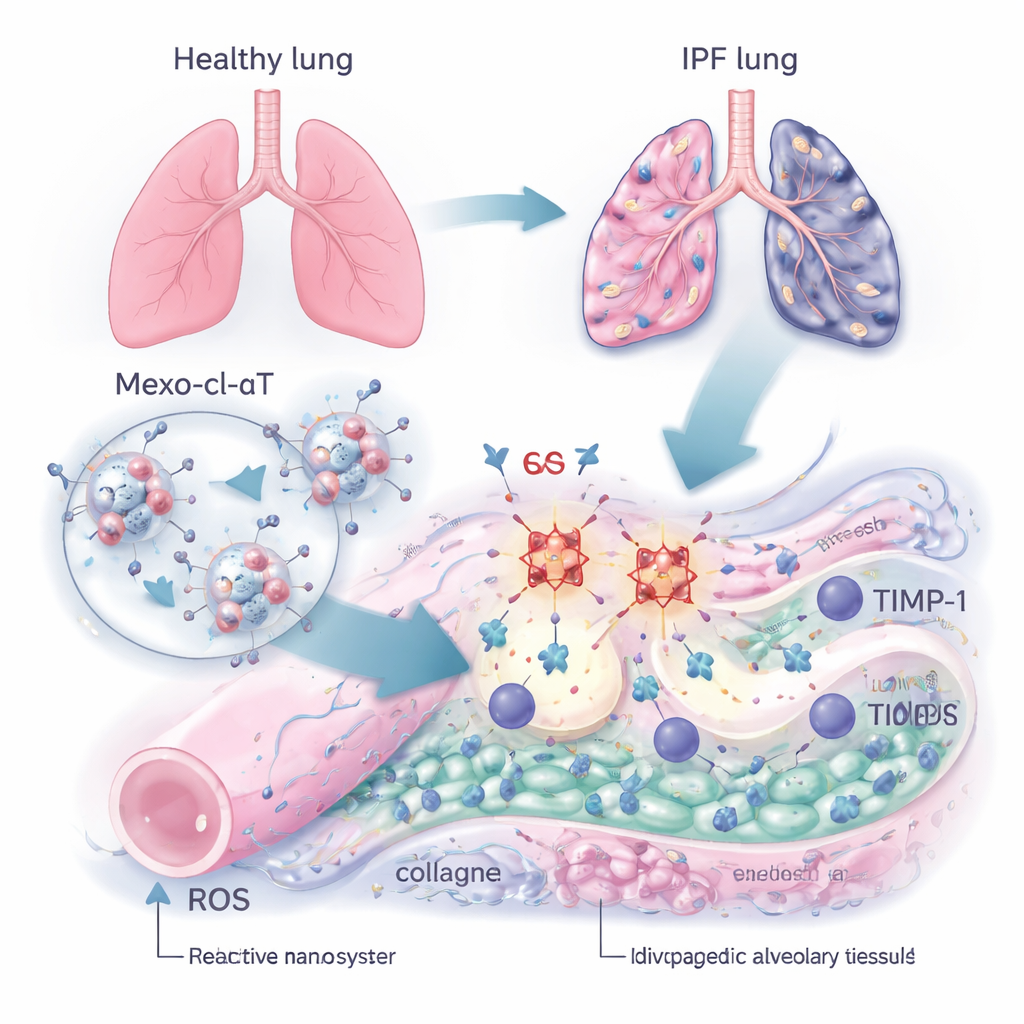
智能递送载体:微小的修复包
为打破这一循环,研究团队构建了一种名为Mexo‑cl‑aT的纳米疗法。他们以外泌体为起点——外泌体是干细胞释放的天然囊泡,已知能定位受损组织并支持修复。在这些外泌体表面,他们连接了能特异性结合TIMP‑1的抗体。外泌体与抗体之间的连接采用了一种可被ROS切断的化学连接子。换言之,瘢痕肺的恶劣化学环境被用作信号:当外泌体到达富含ROS的受损区域时,连接子断裂,部分吸收ROS并在TIMP‑1富集处释放抗体,同时外泌体本身继续促进组织修复。
纳米系统的行为与作用机制
在细胞研究中,研究者表明Mexo‑cl‑aT在液体中保持稳定,但在暴露于与患病肺相似的过氧化氢水平时会迅速释放其抗体。与此同时,它显著降低了存在的过氧化氢量,证实了其清除ROS的作用。在类瘢痕细胞模型中,释放的抗体降低了TIMP‑1水平,使能够分解胶原的酶恢复活性;而外泌体成分则减少细胞死亡、促进细胞增殖并加快肺细胞与血管细胞的伤口愈合。与不可切断连接子的版本相比,该ROS响应型设计更有效地去除了胶原并减轻了化学应激,突出了可控释放的重要性。
在重度肺瘢痕模型中的测试
随后,团队在由博莱霉素诱导的晚期肺纤维化小鼠模型中测试了该疗法,该模型用于模拟晚期IPF。一次吸入给药的Mexo‑cl‑aT在肺内停留数日,并且比其各成分的简单混合物保留了更多抗体。经治疗的肺肉眼及显微镜下看起来更健康:气腔重新打开,瘢痕厚度下降,总胶原含量几乎恢复正常。活化的致瘢痕细胞标志物下降,而与健康气囊和血管内皮细胞相关的蛋白上升。化学测定显示治疗显著降低了TIMP‑1水平,恢复了清除胶原酶的平衡,并去除了约四分之三的过量ROS。重要的是,炎症指标下降,血液检测和器官检查未见明显毒性。
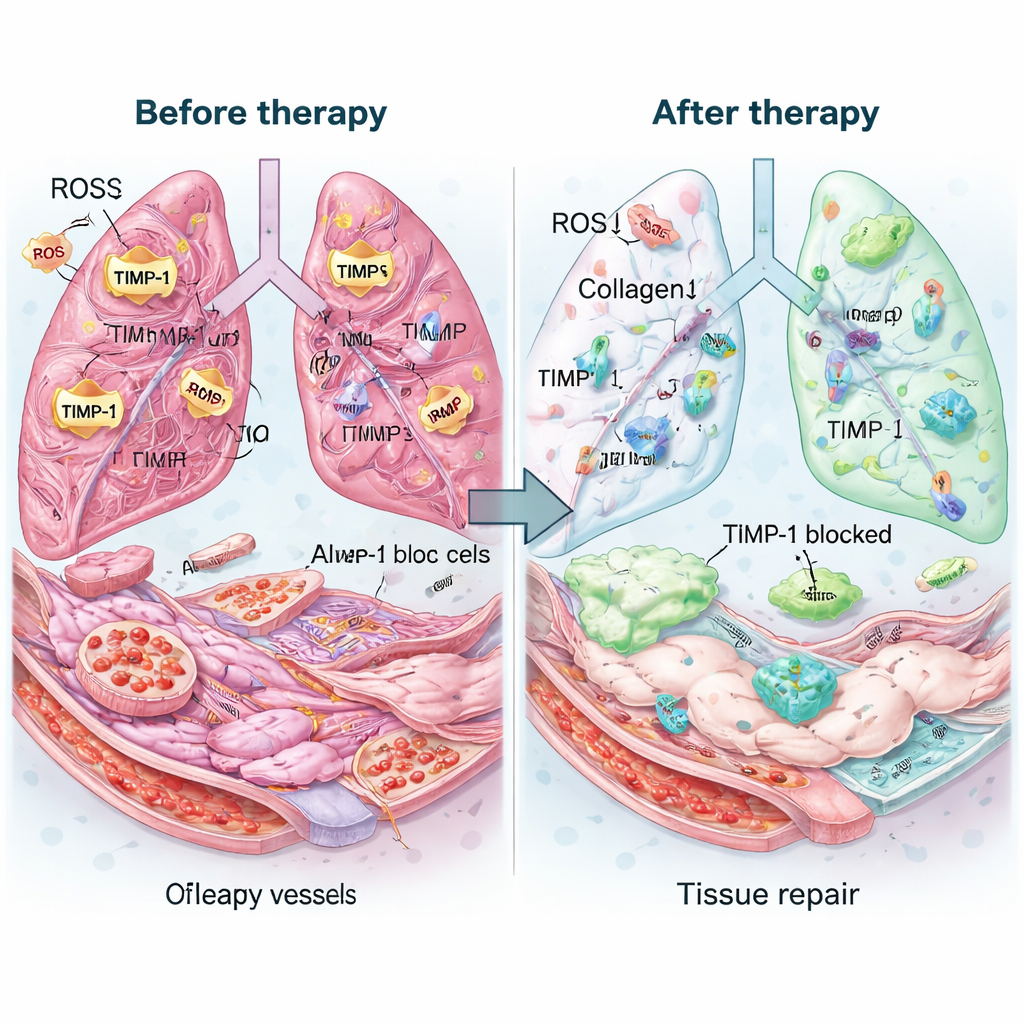
这对患者可能意味着什么
对于患有IPF的人来说,这项工作尚不能立即带来治愈,但它提出了一种有前景的策略。Mexo‑cl‑aT纳米系统的目标不是仅仅减缓新损伤,而是主动逆转既有瘢痕、缓解有害的化学应激并支持脆弱肺组织的重建——所有这些通过靶向吸入的方式将治疗集中在最需要的部位。尽管大规模外泌体生产和人体试验等挑战仍然存在,该研究表明,针对病变环境调谐的精准纳米疗法有朝一日可能改变顽固性肺纤维化乃至其他纤维化疾病的治疗方式。
引用: Li, C., Lu, G., Chen, H. et al. A nanosystem targeting tissue inhibitor of metalloproteinase-1 for continuous spatiotemporal idiopathic pulmonary fibrosis therapy. Nat Commun 17, 1694 (2026). https://doi.org/10.1038/s41467-026-68398-0
关键词: 特发性肺纤维化, 肺部瘢痕化, 纳米医学, 外泌体疗法, TIMP-1