Clear Sky Science · zh
受损上皮细胞状态影响T细胞介导排斥后肾移植存活率
这项肾脏研究对患者的重要性
肾移植能挽救生命,但即便医生似乎控制了被称为T细胞介导的排斥反应,移植肾在手术多年后仍常出现失败。本研究提出了一个简单但关键的问题:当显微镜下的免疫反应看起来“已被治疗”时,为何有些移植肾仍会过早衰竭?通过对来自小鼠和人类的移植肾逐细胞放大观察,研究者揭示了肾脏滤过小管内存在的一层隐蔽性损伤,这有助于解释哪些移植物能存活、哪些不能。
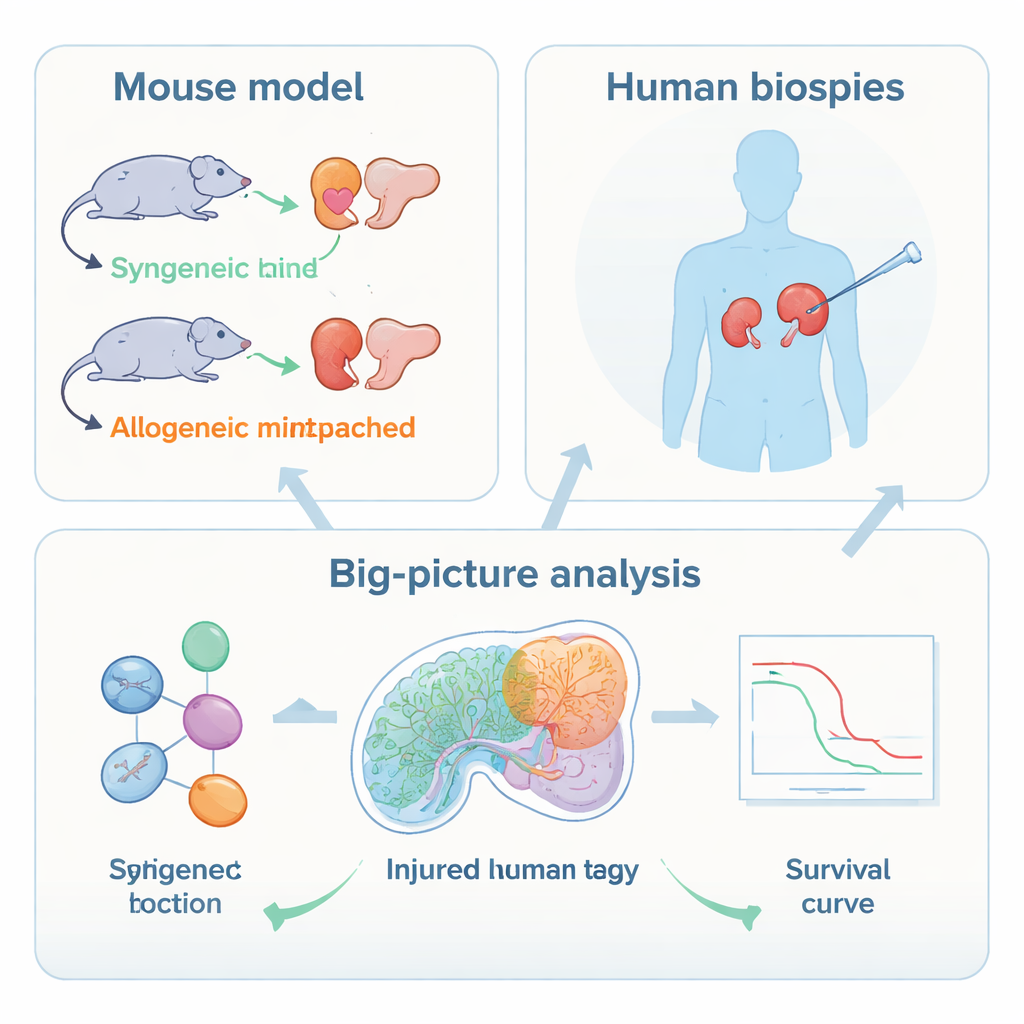
超越经典排斥征象的视角
医生通常通过观察白细胞侵入肾脏并攻击处理尿液的微小小管来诊断T细胞介导的排斥。强效的抗排斥药物常能驱散这些免疫细胞,使活检结果看起来好转。然而,患有这种排斥形式的患者仍面临较高的移植失败风险。早期的大规模基因研究提示,肾细胞内的组织损伤信号比免疫细胞数量更能预测结局。作者旨在以单细胞分辨率定义这些损伤信号,并检验它们与长期移植存活的关联程度。
逐细胞剖析排斥
研究小组首先使用受控的小鼠模型,将肾脏在遗传上相同的鼠之间移植,或在不匹配的菌系之间移植以诱发排斥。随后他们采用单核RNA测序以读取单个细胞中数千个基因的活性,并使用空间转录组学来显示这些细胞在组织切片中的位置。这些工具揭示,在排斥过程中,分子层面变化最强烈的并非免疫细胞,而是肾脏自身的上皮细胞,主要位于近端小管和称为粗升支的段落。在这些区域,细胞启动了损伤与应激基因、炎症信号以及更原始、去分化状态的标志,同时降低了维持正常滤过所需的转运功能。
隐匿的严重受损小管细胞斑块
通过对基因活性相似的细胞进行聚类,研究者在小鼠肾脏中发现了几种不同的“小管细胞损伤状态”。有些反映早期应激反应,另一些则代表严重受损、发生重大变化的细胞,这些细胞失去正常身份并产生大量炎症和纤维化相关分子。空间定位显示,这些细胞状态并不均匀分布:某些严重损伤状态在肾皮质和外髓质形成斑片状聚集,并与T细胞、巨噬细胞及成纤维细胞等复杂邻里共存。相比之下,位于较深区域的一些受损细胞却出人意料地与免疫细胞隔离,暗示损伤产生和持续存在的路径可能不同。
将小鼠损伤状态与人类移植对照
作者随后考察这些细胞状态在人类中是否存在。他们分析了来自有活动性T细胞介导排斥的人类肾移植活检样本与稳定移植物样本。单细胞数据再次显示,近端小管和粗升支的受损细胞的基因模式与小鼠中最严重的受损细胞状态高度相符。利用这些人类特征图谱,研究团队对数千份既往的整体组织基因表达谱进行了“解卷积”,发现严重受损的小管状态在T细胞介导的排斥和混合性排斥中更为常见,而在仅抗体介导的排斥或无排斥时则较少。重要的是,他们构建了代表每种受损状态的紧凑基因集,并在一个具有详细随访的大队列中对其进行了评分。
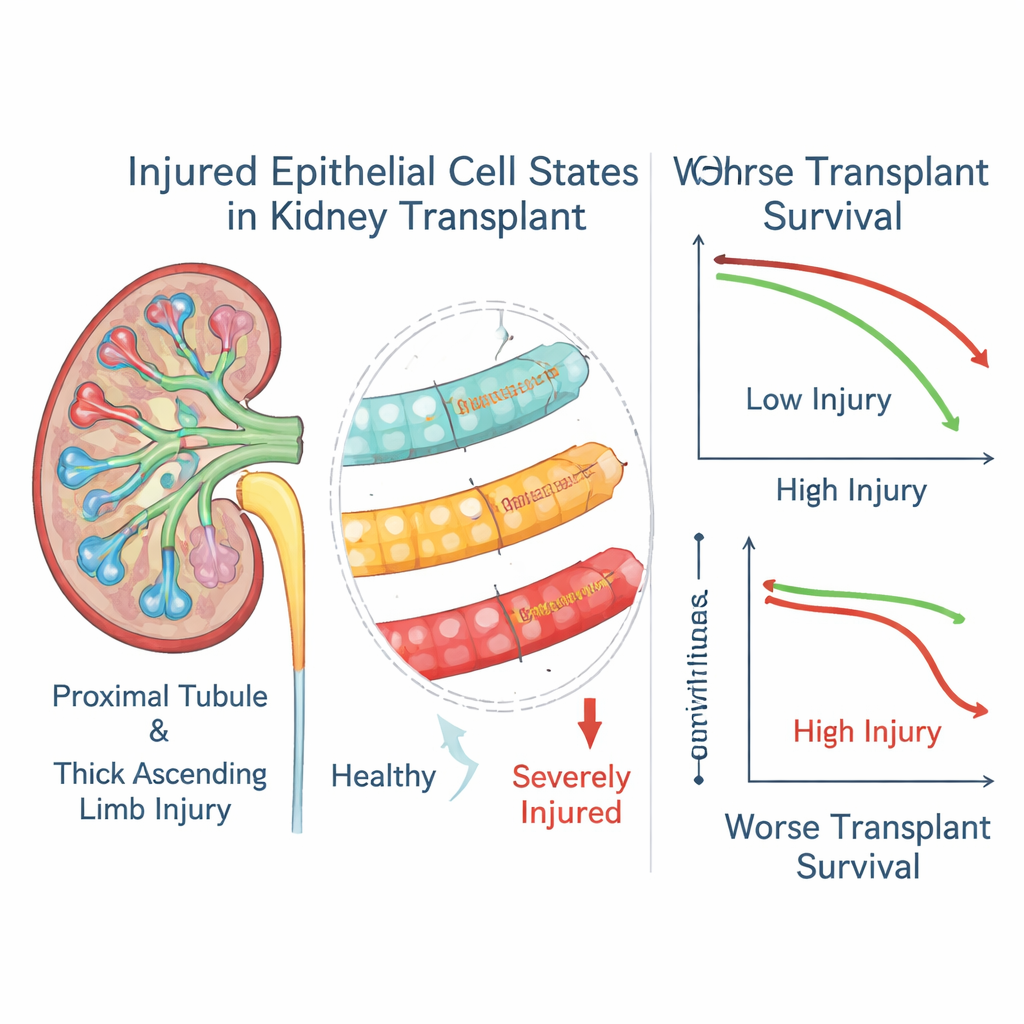
受损小管细胞作为移植物命运的预测因子
当作者将这些基因评分与超过一千名移植受者的三年结局相关联时,出现了清晰的模式。在近端小管和粗升支中,最严重上皮细胞损伤状态的标志物水平高,与移植物丢失的风险显著相关,即便这些患者的活检在其它方面被归类为已治疗的排斥。较轻的小管损伤状态则呈相反趋势,与更好的存活相关,提示其可能代表一种更成功的修复程序。在一部分接受重复活检的患者中,“严重损伤”评分在排斥表面上已消退很久之后仍常保持升高,暗示这些改变的细胞可以长期存在并继续影响疾病进程。
对移植护理的意义
对于非专业读者,关键的信息是:被排斥肾脏中的损伤并非全部直接来自免疫细胞,当免疫攻击平息时,并非所有损伤都会消失。本研究表明,顽固的严重受损小管细胞斑块可作为未来移植失败的早期预警。长期来看,基于这些损伤基因特征的简单检测——甚至可能通过检测排泄到尿液中的细胞——可帮助医生识别高风险患者、量身定制治疗并监测肾脏是否真正恢复。该研究亦提示,可将这些受损上皮细胞本身作为新的治疗靶点,以在常规免疫抑制之外保护移植肾脏。
引用: Pfefferkorn, A.M., Jahn, L., Gauthier, P.T. et al. Injured epithelial cell states impact kidney allograft survival after T-cell-mediated rejection. Nat Commun 17, 1060 (2026). https://doi.org/10.1038/s41467-026-68397-1
关键词: 肾移植排斥, 小管细胞损伤, 单细胞测序, 移植存活率, 上皮细胞状态