Clear Sky Science · zh
CD39 多态性使镰状细胞病患者发生肺部血栓
这对镰状细胞病患者为何重要
镰状细胞病影响全球数百万人,常常损害肺部,有时会导致猝发且危及生命的血栓。但并非所有患者都会出现这种危险的肺部血栓,尽管他们都有共同的血液基础问题。本研究揭示了许多镰状细胞病患者体内存在的一种内在保护机制——同时解释了为何某种遗传变体会使一部分高危患者失去这层保护。
镰状血液中的拉锯战
在镰状细胞病中,红细胞比正常更容易破裂。破裂时,它们向血流中释放一种称为 ADP 的小分子。ADP 像警报一样激活血小板,血小板是形成血栓的细胞。肺部过量的 ADP 会触发血小板聚集,堵塞微小肺动脉,导致疼痛且有时致命的呼吸衰竭发作。问题在于,尽管所有患者都持续发生红细胞损伤,为什么这种情况并非发生在每个人身上。
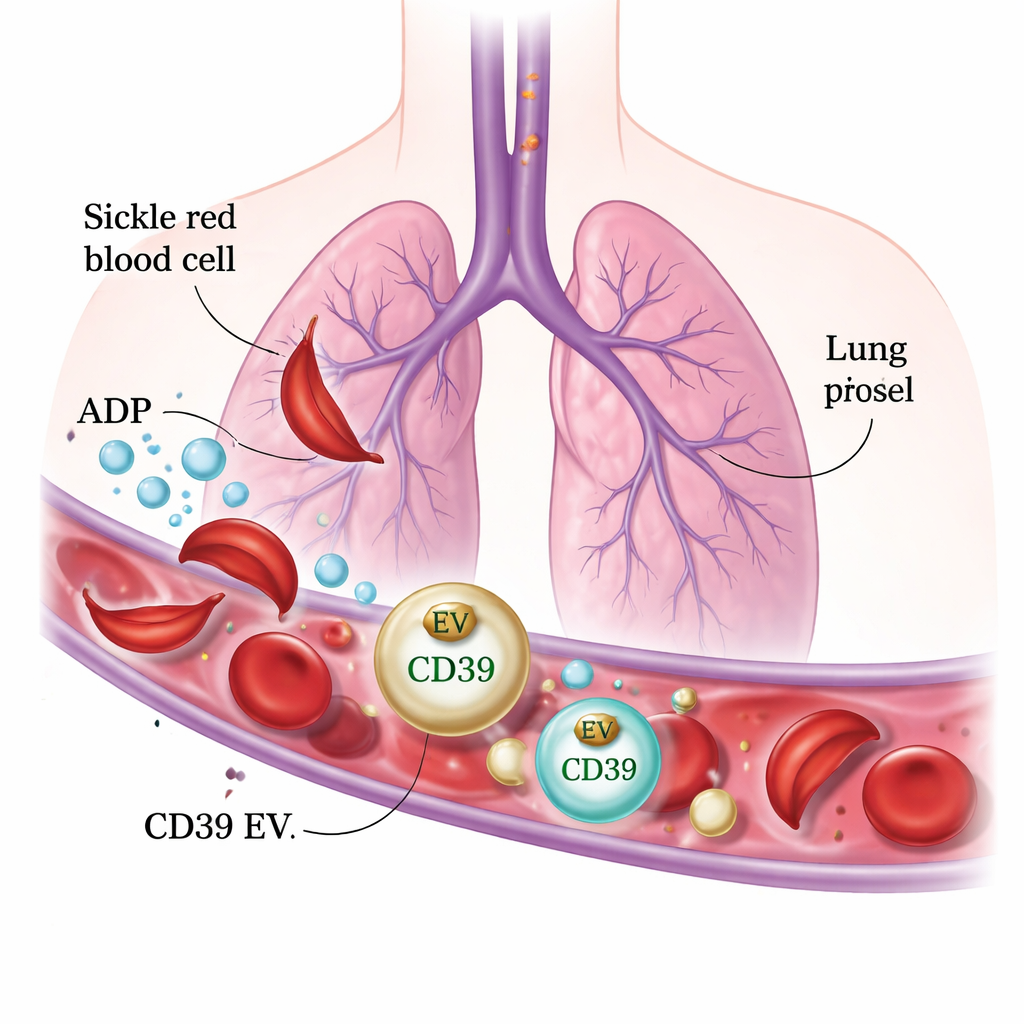
来自肺壁的微小保护囊泡
研究者使用携带人体镰状血红蛋白的专门培育小鼠,并借助活体高分辨率成像观察在将 ADP 注入血流后肺内发生的变化。在正常小鼠中,ADP 会迅速引发富含血小板的血栓形成并暂时阻塞小肺血管。相反,镰状小鼠意外地受到保护:它们的肺血管保持通畅,血小板对 ADP 并不聚集。对血液的进一步检查显示,镰状小鼠血中比对照组存在更多微小的膜“气泡”,即细胞外囊泡。这些囊泡携带大量表面酶 CD39,CD39 能将 ADP 分解为活性较低的形式。在体外实验中,来自镰状小鼠的囊泡能强力降解 ADP 并阻止血小板聚集。
关闭保护机制揭示 CD39 的作用
为了证明 CD39 对这种保护的责任,研究人员在镰状小鼠中使用化学抑制剂阻断了 CD39 的活性。一旦 CD39 被关闭,ADP 就像预期那样:它触发了强烈的血小板聚集和肺血管阻塞,同时循环血小板计数下降,显示出活跃的血栓形成迹象。同样,在来自镰状小鼠的血样中抑制 CD39 后,血小板对 ADP 的反应恢复到正常强度。这些实验表明,循环中携带 CD39 的囊泡在镰状细胞病的肺部充当了对抗凝血信号的强有力刹车。
削弱屏障的遗传变体
研究者随后转向生活在世的镰状细胞病患者。他们发现许多患者的血液中也富含携带 CD39 的囊泡,且其血小板对 ADP 的反应较弱,这与自然保护效应一致。然而,对 400 多名患者的遗传分析显示,携带名为 rs3176891 G 的 CD39 基因特定版本的患者更可能有肺部血栓的病史。在这一遗传亚组中,患者血液中 CD39 阳性囊泡更少、CD39 活性更低,血小板对 ADP 的反应更强。重要的是,同一遗传变体在一大群没有镰状细胞病的非裔背景人群中并未增加血栓风险,这表明这种危险主要在持续的红细胞破坏存在时才显现。
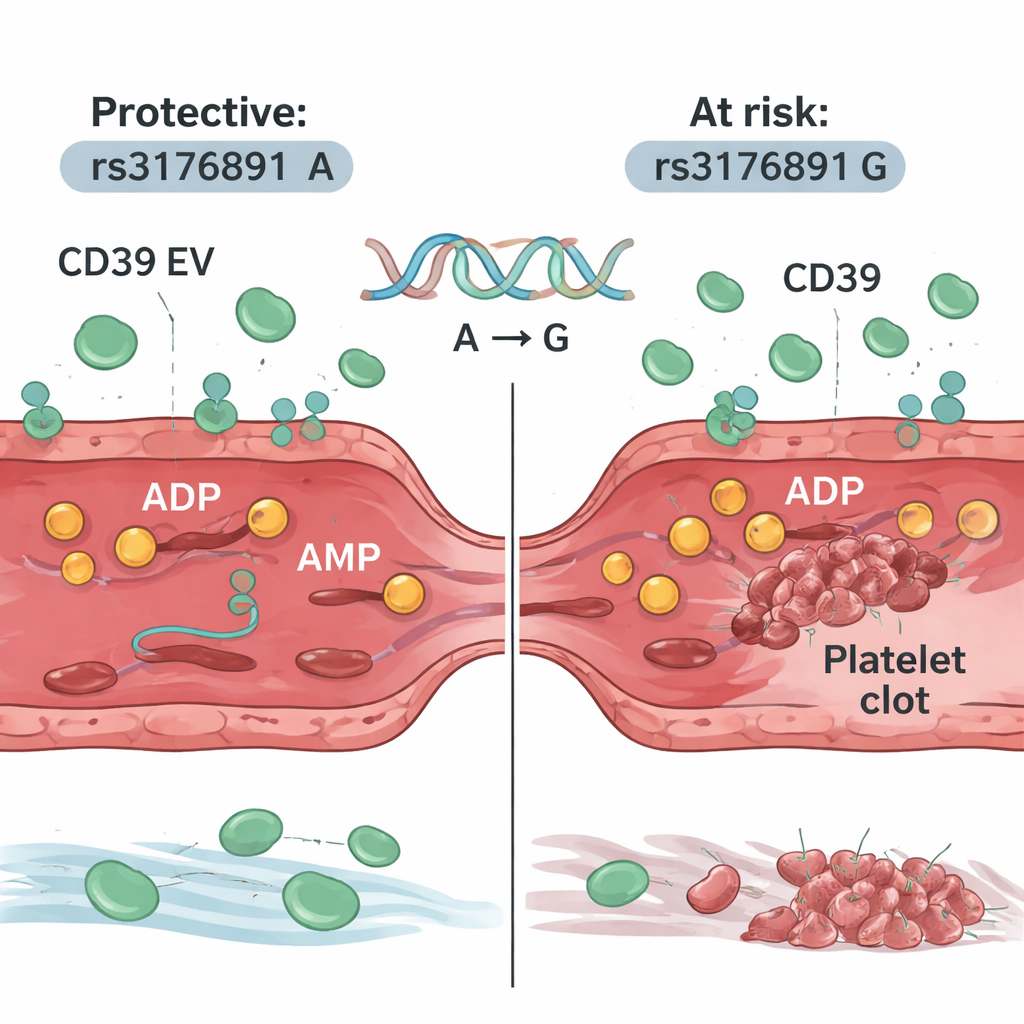
对患者与未来护理的意义
对镰状细胞病患者而言,这些发现强调体内并非单纯被促凝信号所淹没——它也会部署自身的应对措施。在许多患者中,肺血管细胞释放富含 CD39 的囊泡,吸收多余的 ADP,帮助防止血小板堵塞脆弱的肺动脉。但那些继承了 rs3176891 G 版本 CD39 基因的人,其保护屏障可能较弱,使他们更易发生肺栓塞。未来,检测该遗传变体并测量携带 CD39 的囊泡水平,可能有助于识别高风险患者并定制针对血小板信号的更精确治疗,将对这种天然防御机制的新认识转化为对镰状细胞病最严重并发症之一的更好防护。
引用: Brzoska, T., Kaminski, T.W., Katoch, O. et al. CD39 polymorphism enables lung thrombosis in sickle cell disease. Nat Commun 17, 1693 (2026). https://doi.org/10.1038/s41467-026-68396-2
关键词: 镰状细胞病, 肺部血栓, 血小板, 细胞外囊泡, CD39 多态性