Clear Sky Science · zh
OTX2抑制人类多能干细胞向8细胞样和桑椹胚样状态的重编程
揭示人类细胞中被隐藏的早期潜能
每个人都是从一个单细胞开始,很快分裂成一小团早期细胞,每个细胞都有可能形成机体的各种组织以及诸如胎盘之类的支持结构。科学家们渴望在实验室中重现这种罕见的早期“全能”状态,因为它可能改变再生医学并加深我们对不孕与早期妊娠丢失的理解。本研究揭示了一个关键的遗传制动器——名为OTX2的基因,它阻止人类干细胞回退到这种强大的8细胞样状态——并展示了当该制动被解除时会发生什么。 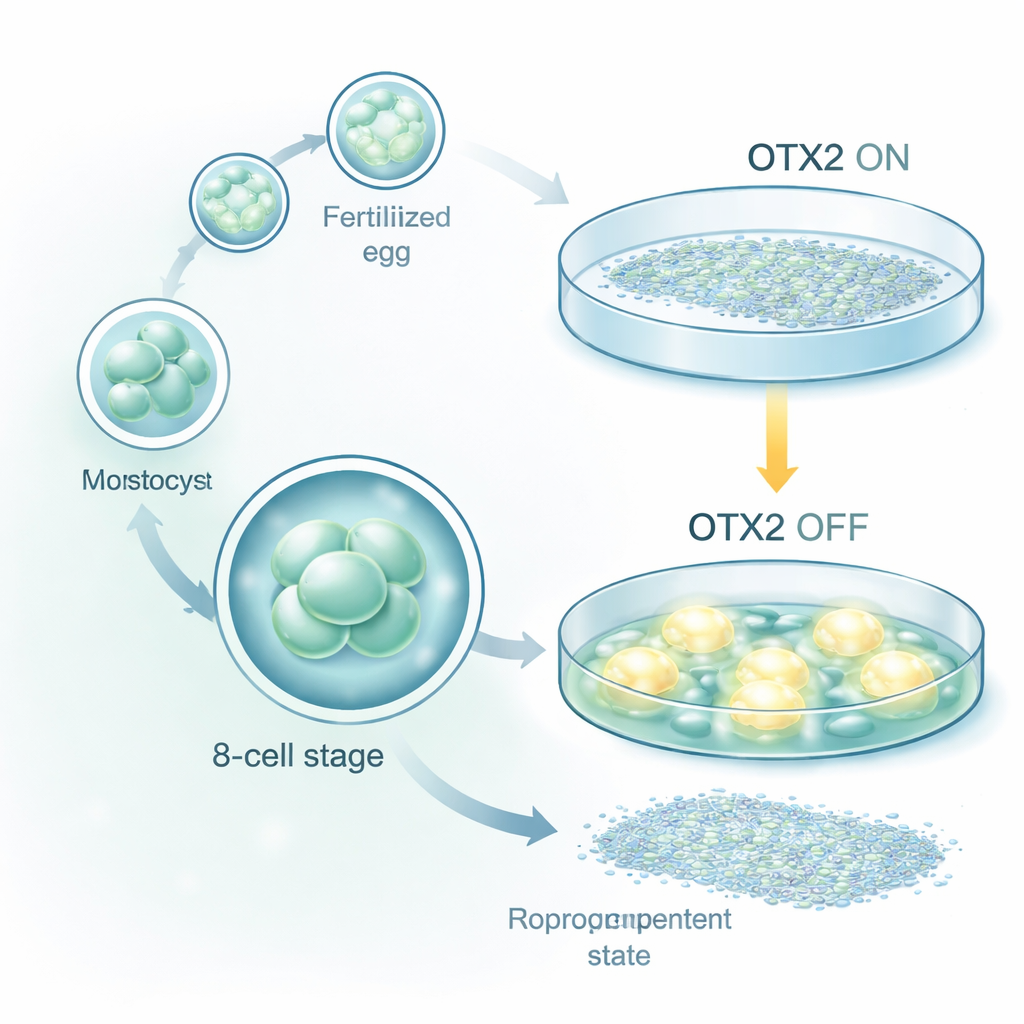
细胞几乎能做任何事的短暂窗口
在人类胚胎中,在8细胞阶段发生一次戏剧性的控制权交接。控制权从卵子中储存的分子转交给胚胎自身的基因组,这一过程称为合子基因组激活。在这一刻,细胞最接近真正的“全能性”:原则上,每个细胞不仅能形成胎儿,还能形成诸如胎盘的外胚层支持组织。由于人类胚胎样本稀缺且伦理敏感,研究者通过将普通的人类多能干细胞重编程,构建了称为8细胞样细胞(8CLCs)的实验室模型。这些干细胞已经具有多能性,但通常只能生成机体组织,而不能同时生成机体与额外胚外组织。本文的核心问题是:是什么阻止多能干细胞重新进入这一更早、更强大的状态?
OTX2作为遗传守门人的出现
研究团队首先梳理了现有的人胚数据集,寻找在8细胞阶段活动发生变化的转录因子——即调控其他基因的基因。一个候选者脱颖而出:OTX2,长期以来因其在脑发育中的作用以及推动干细胞向更成熟“启动态”(primed)转变而为人所知。他们发现OTX2在最早期阶段(包括合子、2细胞和4细胞胚胎)中含量丰富,但在8细胞阶段后其水平急剧下降。在被逐步驱动向8细胞样身份的体外干细胞模型中,OTX2呈现与一个关键8细胞标志TPRX1相反的变化:随着TPRX1上升,OTX2下降。这种相反的关系暗示OTX2可能在阻碍回到8细胞样状态的重编程中发挥屏障作用。
移除制动再现早期胚胎特征
为检验这一想法,研究者工程化改造了人类多能干细胞,使其携带一个荧光报告器:当TPRX1(即8细胞样身份)被激活时会发光。利用逐步的化学方案,他们将“启动态”干细胞经中间的“天真态”转化为8CLCs。在标准条件下,只有一小部分细胞变为TPRX1阳性。当他们使用CRISPR删除OTX2基因时,8CLCs的比例几乎翻倍,达到约28%。这些缺失OTX2的细胞开启了许多8细胞期基因和通常仅在胚胎该阶段活跃的特定可动位点DNA元素。其整体基因表达模式和DNA可及性与天然8细胞及稍晚的桑椹胚(morula)胚胎高度吻合。关键的是,当这些细胞被引入早期小鼠胚胎时,它们不仅贡献于胎体组织,还参与了如胎盘等胚外结构,这是类全能潜能的标志。 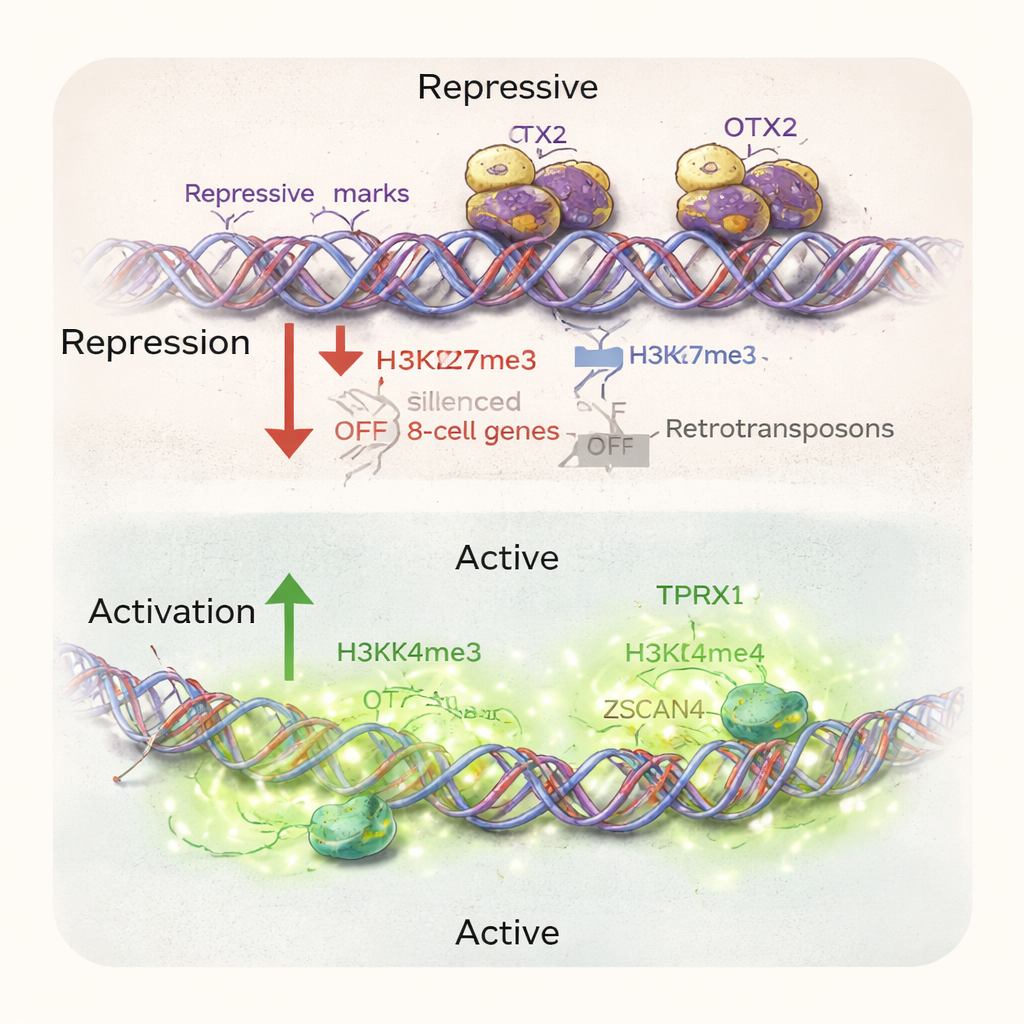
OTX2如何沉默最早期的胚胎程序
进一步挖掘时,作者绘制了OTX2在这些重编程细胞中结合DNA的位置。他们发现OTX2直接结合在许多8细胞特异性基因及其相关重复元件附近的DNA片段上。在OTX2存在的地方,周围的染色质携带分子“关闭”标记并且相对致密;在OTX2缺失的地方,这些区域打开并获得与基因激活相关的“开启”标记。过表达OTX2产生的效果与删除相反:抑制8细胞样基因并减少8CLCs数量。有趣的是,这种作用在很大程度上独立于另一个著名的早期胚胎基因DUX4。尽管两者影响许多相同的靶点,OTX2并不只是简单地开关DUX4;相反,它作为上游抑制因子,帮助将8细胞程序保持封存状态。
从早期胚胎到未来的治疗
综上所述,这项研究表明OTX2充当分子守门人,阻止人类多能干细胞回归到8细胞样、类全能的状态。移除OTX2打开了这道门,使相当比例的细胞更忠实地模拟真实8细胞和桑椹胚胎的基因活动、表观遗传景观和发育范围。对非专业读者来说,这意味着科学家们已识别出一个关键开关,决定细胞是保持灵活但受限的状态,还是重新获得人类生命最早期阶段的更广泛潜能。从长远看,学会如何安全地控制这一开关,可能带来为研究生成细胞的新方法、改进与克隆相关的技术,并且或许有朝一日通过从头重建受损组织来治疗疾病。
引用: Kong, X., Jiang, N., Chen, S. et al. OTX2 inhibits human pluripotent stem cell reprogramming toward 8-cell-like and morula-like states. Nat Commun 17, 1685 (2026). https://doi.org/10.1038/s41467-026-68388-2
关键词: 全能干细胞, 合子基因组激活, OTX2, 早期人胚, 细胞重编程