Clear Sky Science · zh
通过 CRISPR/Cas9 精准切除 NOTCH2NLC 中扩增的 GGC 重复以治疗细胞核内包涵体病
用 DNA 编辑应对一种神秘的脑部疾病
细胞核内包涵体病(NIID)是一种罕见但毁灭性的脑疾病,可导致痴呆、运动障碍,甚至早逝。目前尚无治愈方法。本研究探讨是否可以利用一种强大的基因编辑工具 CRISPR,将驱动 NIID 的一小段但具有毒性的 DNA 片段切除,从而展示未来可能通过改写基因来对抗脑疾病的治疗思路。 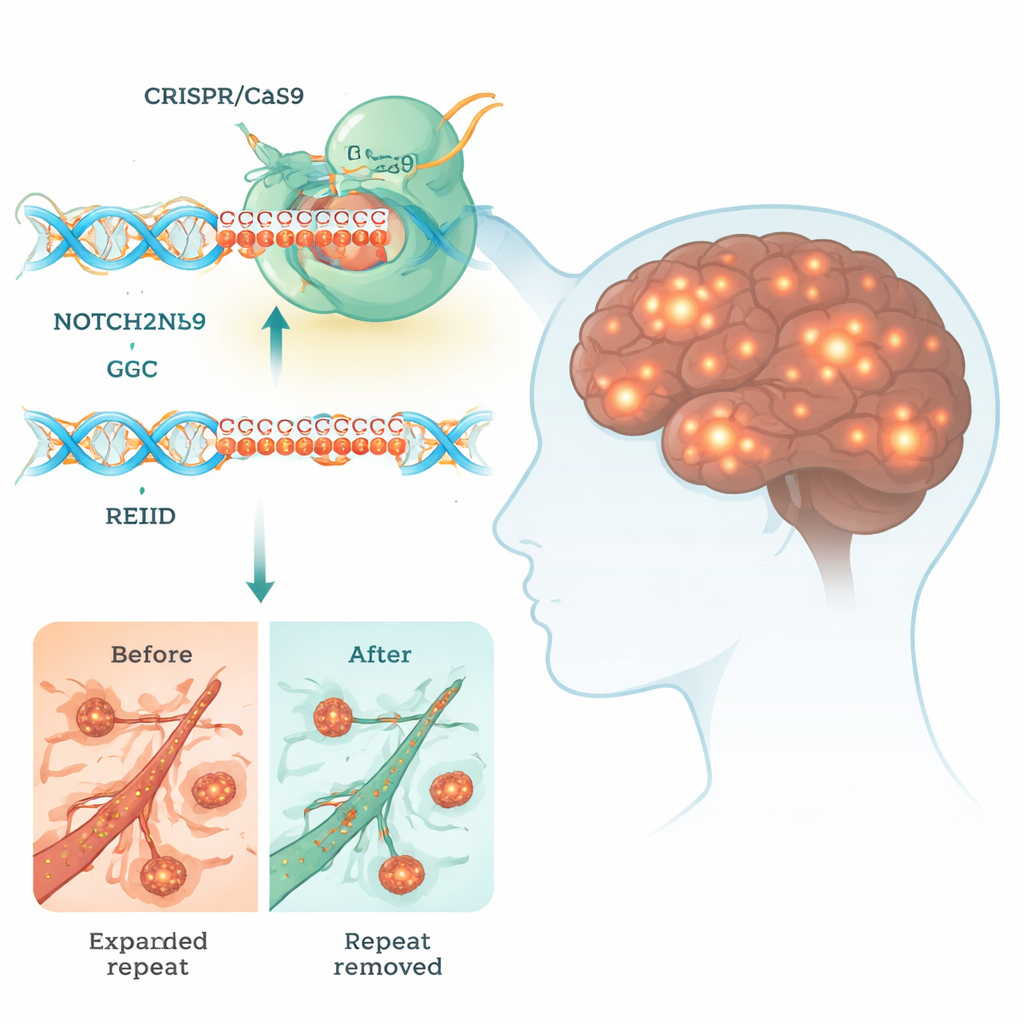
隐藏的遗传罪魁
许多遗传性脑疾病是由短的 DNA 序列异常扩增引起的。在 NIID 中,问题是位于名为 NOTCH2NLC 基因的一段三核苷酸“GGC”重复序列过度扩展。虽然这段序列位于非经典编码区,但细胞的翻译机制仍可能读取它,产生异常的多甘氨酸(polyG)链。这些黏性的多甘氨酸链在神经细胞和其他组织的细胞核内凝聚成团,干扰能量产生、RNA 加工以及核质间分子运输等关键过程。
精准“基因外科手术”的挑战
为 NIID 设计基因编辑治疗尤其困难,因为 NOTCH2NLC 有若干几乎相同的姊妹基因,这些基因对人类大脑发育非常重要。如果 CRISPR 错误切割到这些近亲基因,可能弊大于利。研究人员仔细扫描了 GGC 重复周围的 DNA,发现了能够将 NOTCH2NLC 与其近亲区分开的微小序列差异。随后他们设计了成对的 CRISPR 引导 RNA,使 Cas9 这把“分子剪刀”能在扩增重复的前后精确切割。这种双切割策略利用细胞自身的修复机制去除有毒片段,同时尽量不影响该基因家族的其余部分。
从培养皿中的细胞到患者来源的神经元
研究团队首先在标准人类细胞和携带大量 NOTCH2NLC 重复的工程化细胞中测试他们的 CRISPR 设计。在这些模型中,编辑器有效地切除了重复片段,多甘氨酸包涵体的水平下降了大约一半或更多。随后他们在来自一名 NIID 患者的诱导多能干细胞(iPSCs)上开展实验,并将这些细胞分化为神经前体细胞(一种早期脑细胞)。使用 CRISPR,他们要么删除了扩增的重复,要么将其替换为正常长度的版本。详尽的 DNA 及全基因组测序显示编辑高度准确,几乎没有不良切割的证据,且被编辑的细胞仍能正常分裂和成熟。 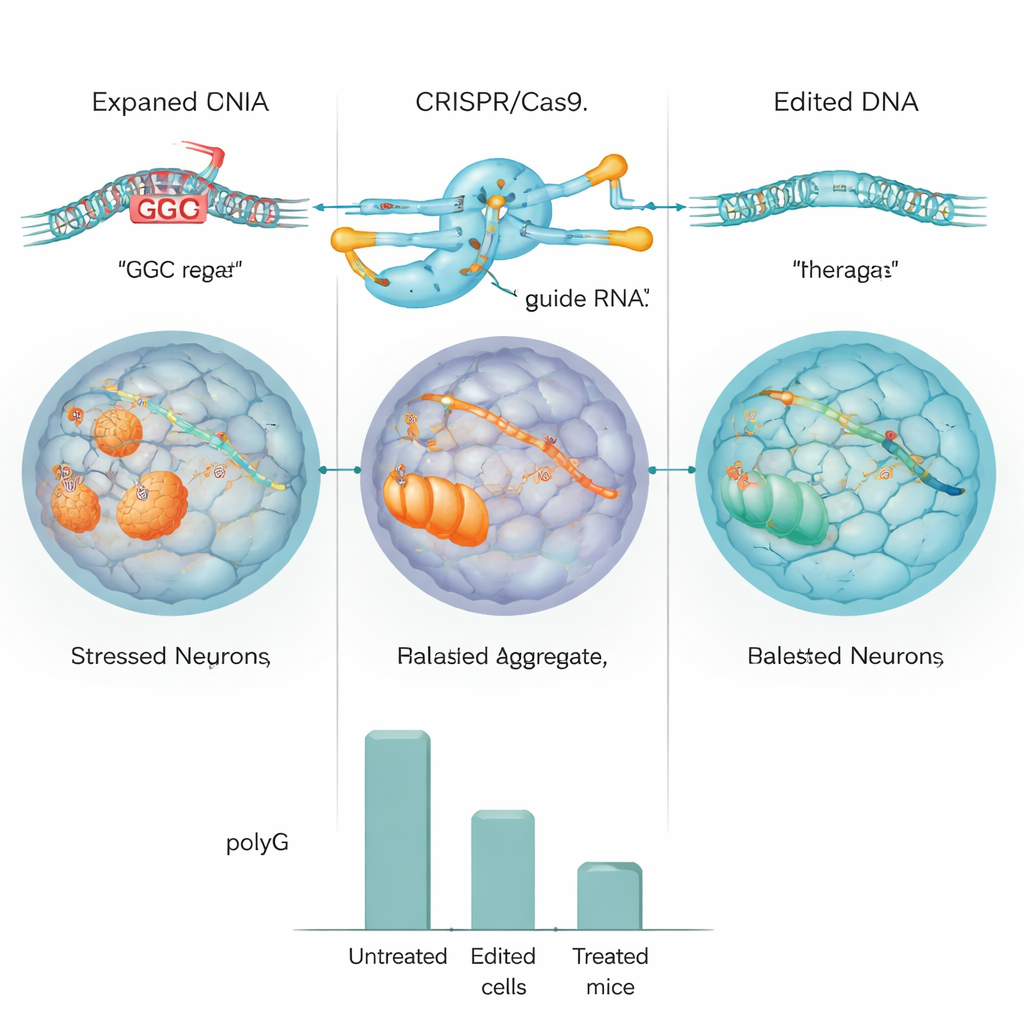
在小鼠模型中拯救大脑和全身功能
为检验该方法是否能实际改善疾病,研究人员使用了携带人类 NOTCH2NLC 重复并表现出 NIID 样特征的小鼠模型,这些小鼠出现细胞核内包涵体、运动障碍和寿命缩短等症状。他们将 CRISPR 系统封装入一种改造病毒,通过新生小鼠静脉注射后在全脑传播。在接受治疗的动物中,脑组织内成功去除了扩增的重复。因此,有毒的 polyG 水平显著下降,神经元健康相关的标志物改善,支持性脑细胞的异常激活也减轻。行为学测试显示,接受治疗的小鼠活动更多、平衡性更好、存活时间比未治疗的同窝鼠更长。在心脏这一在该模型中也会积累 polyG 的器官中,观察到类似的益处。
这对未来治疗意味着什么
对普通读者而言,主要信息是 NIID 很大程度上由一段特定的过度扩增 DNA 重复驱动,精确去除该重复能在细胞和小鼠中逆转许多疾病表型。这项工作尚未直接转化为可用于人类的现成疗法:研究人员仍需完善长期安全性、改进递送方法,并在更大、更接近人类的动物中进行测试。但该研究提供了有力的概念验证,表明经过精心设计的基因编辑可以在保护密切相关基因的同时安全地沉默有毒重复。这一策略未来不仅可能用于 NIID,也可能推广到由类似重复扩增引发的其他脑肌疾病。
引用: Xie, N., Pan, Y., Tong, H. et al. Precise excision of expanded GGC repeats in NOTCH2NLC via CRISPR/Cas9 for treating neuronal intranuclear inclusion disease. Nat Commun 17, 1683 (2026). https://doi.org/10.1038/s41467-026-68385-5
关键词: CRISPR 基因编辑, 细胞核内包涵体病, 重复扩增性疾病, NOTCH2NLC, 神经退行性疾病