Clear Sky Science · zh
Tmem110 调节 TRPML1 构象以维持内体溶酶体稳态并防止线粒体 DNA 泄漏与病理性自体 DNA 加工
为什么受伤后泄漏的 DNA 很重要
当我们遭受严重创伤,例如头部受重击时,损伤并不会仅局限于受伤部位。许多患者随后会发展为一种危险的全身反应,其中肺、肝、肾等器官开始衰竭。本研究揭示了细胞内微小结构——溶酶体、线粒体与免疫感应器——如何相互对话以决定机体是悄然清理碎片还是陷入自我攻击式的免疫风暴。理解这一隐蔽的清理系统,可能为预防创伤后器官衰竭以及治疗自身免疫和炎症性疾病开辟新路径。
从头部损伤到全身危机
创伤性脑损伤(TBI)可触发一种强烈的炎症风暴,称为多器官功能障碍综合征(MODS),但脑内损伤如何扩散至远端器官尚不清楚。作者将注意力集中在单核细胞和巨噬细胞上——在血液和组织中巡逻、承担“垃圾清理”任务的免疫细胞。TBI 后,细胞以失控的方式死亡并释放出完整的线粒体——这些携带自身 DNA 的微小能量工厂进入循环。线粒体 DNA(mtDNA)在免疫系统看来酷似细菌 DNA,如果不能被快速清除,就会启动类似抗病毒的强烈防御反应。通常,细胞会将这些流浪的线粒体吞入酸性隔室——溶酶体,酶在其中降解 DNA,防止其泄入细胞质。 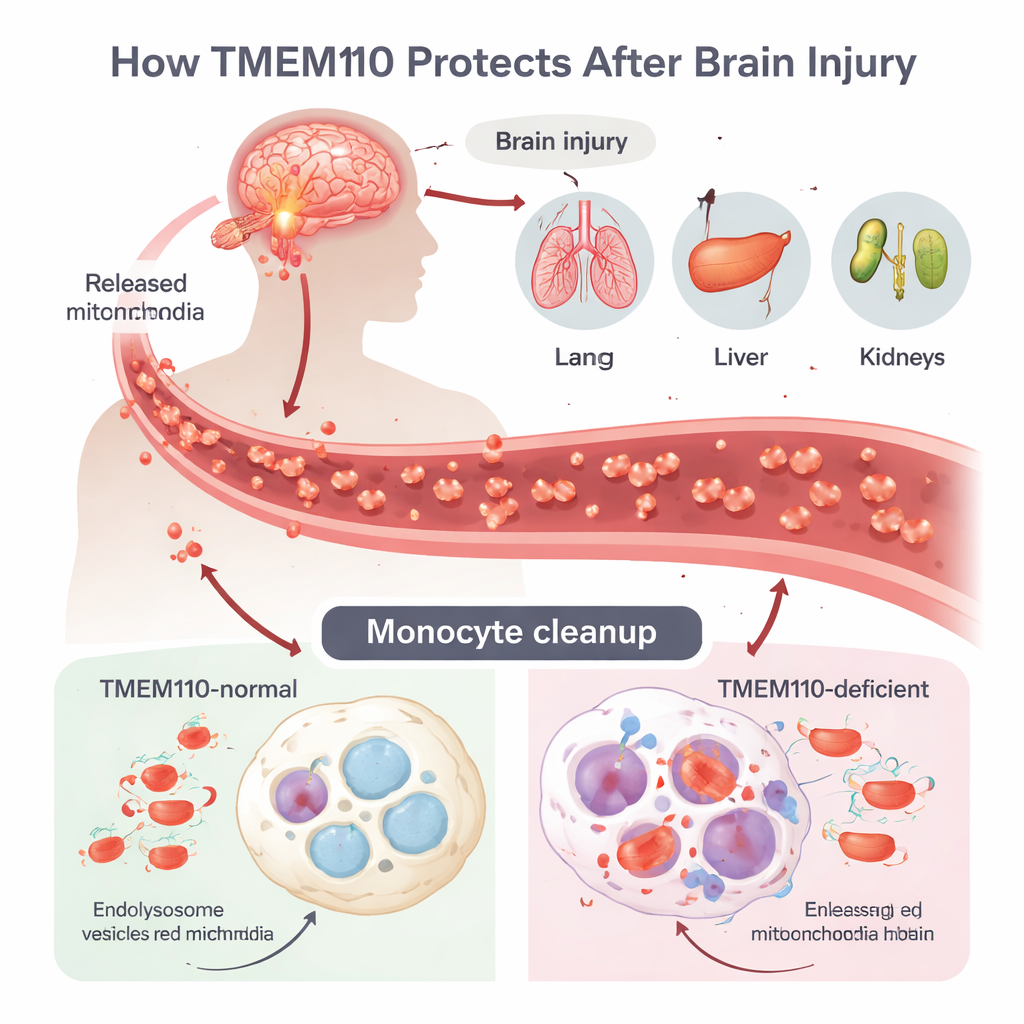
维持溶酶体稳定的守门蛋白
研究小组鉴定出 TMEM110,一种跨越内质网膜(主要的细胞内膜网络)的蛋白,在该过程中起关键守门角色。借助仅在单核细胞和巨噬细胞中缺失 TMEM110 的基因工程小鼠,他们建立了可控的脑损伤模型。与正常小鼠相比,缺失 TMEM110 的动物血液和脑脊液中的 I 型干扰素——强效的抗病毒信号分子——水平显著升高。其肺、肝、肾和淋巴结的损伤更为严重,TBI 后长期存活率明显下降。当研究者阻断 I 型干扰素受体,或用正常细胞替换突变的骨髓时,器官损伤和死亡率都下降,说明外周单核细胞过度的干扰素信号是该情形下 MODS 的关键驱动因素。
离子处理异常如何导致 DNA 逃逸
深入研究这些免疫细胞,作者发现缺失 TMEM110 的溶酶体在化学上失衡:酸性降低且钙离子过载。在这种条件下,通常在溶酶体内切割 DNA 的酶 DNase II 活性丧失,溶酶体膜变得脆弱,mtDNA 因而泄入周围的细胞质。人体单核细胞吞噬标记的供体线粒体的体外实验证实:没有 TMEM110 时,更多的 mtDNA 泄入细胞液并触发干扰素刺激基因的激增。研究显示 TMEM110 通过调控另一种蛋白——溶酶体离子通道 TRPML1 来发挥作用。当 TMEM110 存在时,它与 TRPML1 发生物理接触,并将其推向“开放”构象,在溶酶体表面产生微小的钙释放热点。这些受控的钙外流有助于维持适当的酸性、支持膜修复,并将 mtDNA 限于内部并予以降解。 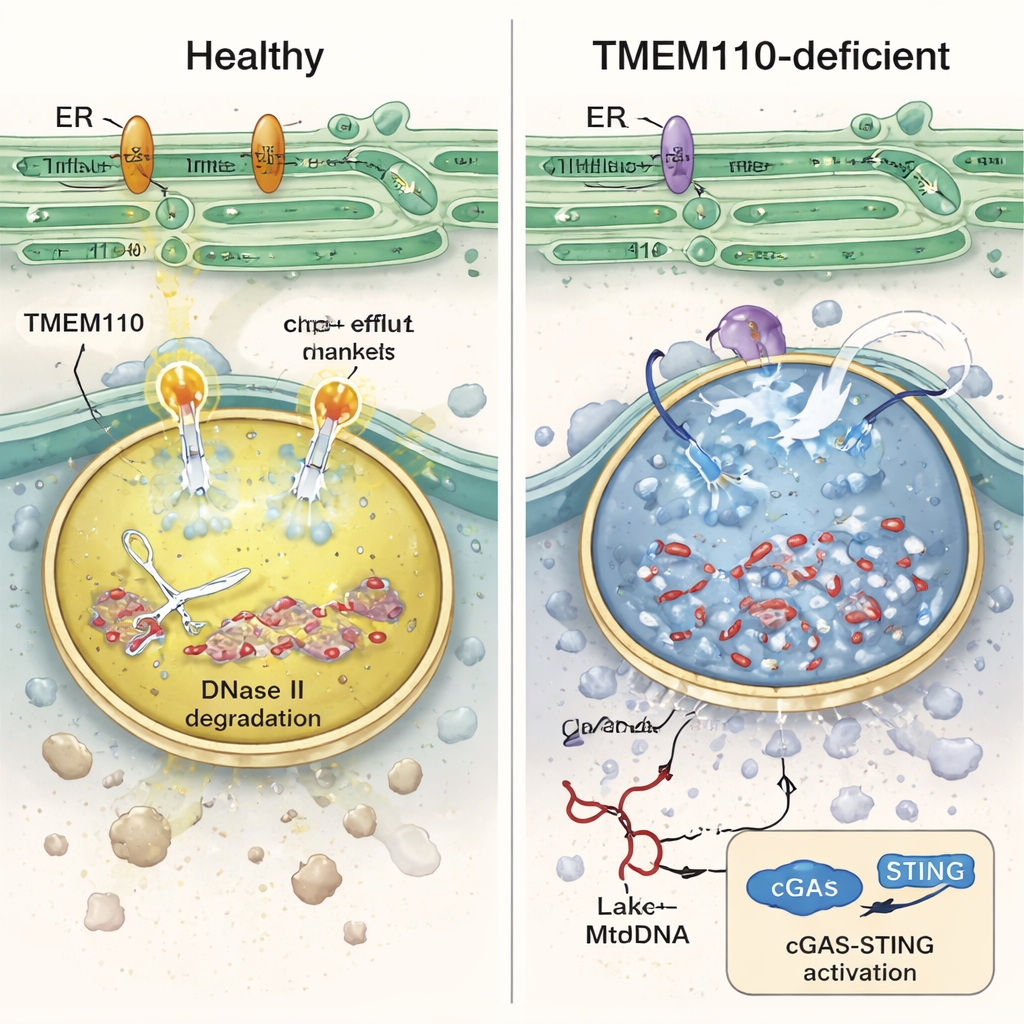
与细胞 DNA 报警系统的反馈回路
一旦 mtDNA 溢入细胞质,它会被 cGAS–STING 通路识别,这是细胞检测游离 DNA 的主要报警系统。有趣的是,TMEM110 在静息状态下也与 STING 结合并将其隔离在内质网,防止不必要的警报。当细胞质 DNA 积累时,STING 被激活并放松对 TMEM110 的束缚。反过来,这暴露了 TMEM110 的另一片段,促使其与 TRPML1 相互作用并增强溶酶体钙外流,形成一个反馈回路:感知到自体 DNA 激活了增强 DNA 清除的机制。人类自炎性综合征中发现的与疾病相关的 STING 突变会破坏这一交接过程,使 TMEM110 滞留于抑制状态,助长慢性干扰素激活。在携带此类 STING 突变的小鼠中,TBI 导致更严重的器官损伤和更高的死亡率,但通过 mRNA–脂质纳米颗粒疗法向溶酶体递送一小段 TMEM110 片段,部分恢复了对 mtDNA 的控制并改善了存活率。
来自患者的线索与新治疗路径
随后作者转向一组包含 143 名创伤相关脑损伤并伴 MODS 的临床队列。受伤早期其单核细胞中 TMEM110 水平较高的患者更可能恢复器官功能并存活。TMEM110 较低的患者表现出更多循环 mtDNA 与脱细胞线粒体、更强的干扰素反应、更高的器官衰竭评分以及更广泛的自身抗体谱,包括针对 DNA 与核蛋白的抗体。这些模式与小鼠研究发现高度一致,支持 TMEM110 驱动的溶酶体稳定性与 mtDNA 清除在人体疾病中为通用机制的观点。
这对严重创伤患者意味着什么
通俗地说,这项工作表明,在重大创伤后,我们的免疫系统面临一个微妙的选择:是默默消化来自死亡细胞的大量自体 DNA,还是将其误判为病毒入侵并发动全面攻击,从而损害自身器官。TMEM110 通过调节溶酶体离子通道并与 DNA 传感器 STING 协同,帮助细胞选择更安全的路径。当该系统失灵——无论是因为 TMEM110 缺失、STING 突变或溶酶体不堪重负——mtDNA 逃逸,警报持续响起,随之而来的是多器官损害。针对 TMEM110–TRPML1–STING 轴的干预,例如定向溶酶体的 mRNA 疗法,可能为预防或治疗严重创伤后的器官衰竭和类自身免疫并发症提供新途径。
引用: Feng, Z., Pan, Y., Zhou, J. et al. Tmem110 regulates the conformation of TRPML1 to maintain endolysosomal homeostasis and prevent mitochondrial DNA leakage and pathological self-DNA processing. Nat Commun 17, 1678 (2026). https://doi.org/10.1038/s41467-026-68382-8
关键词: 创伤性脑损伤, 线粒体 DNA, 溶酶体, I 型干扰素, cGAS-STING 通路