Clear Sky Science · zh
人类 COP1–DET1 泛素连接酶复合体的冷冻电镜结构
细胞如何决定要摧毁哪些蛋白
在每个细胞内,成千上万的蛋白必须在适当的时间不断被合成、改造或降解。本文研究了细胞的关键“质量控制”机器之一——一种分子碎纸机,它决定何时去除与癌症和发育相关的强效基因调节因子。通过以近原子分辨率揭示其三维结构,作者展示了这台机器如何在一种不活跃的堆叠态与一种活跃的底物加工态之间切换——这些见解最终可能有助于设计调节其活性的药物。
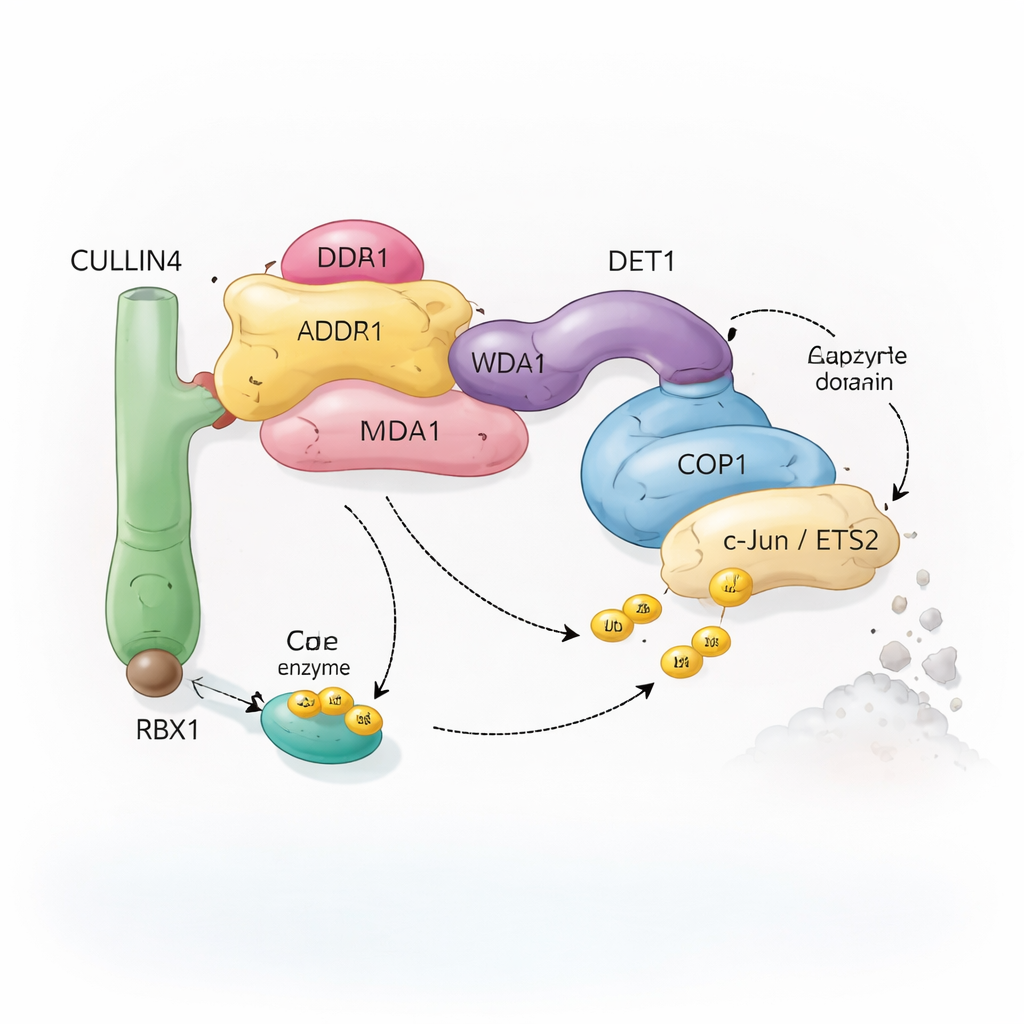
由多部分组成的分子回收队
细胞依靠一种称为泛素化的系统来标记待回收的蛋白。小分子泛素像可移除的旗帜,告诉细胞某个蛋白应被修饰、重新定位或销毁。称为泛素连接酶的特殊酶复合体会把这些旗帜附加到选定的靶蛋白上。本研究的复合体以 COP1 为中心,这是一种从植物到人类都存在的蛋白,帮助标记重要的转录因子——这些蛋白控制哪些基因被开启或关闭。COP1 并不单独工作:它可以插入到围绕骨架蛋白 CULLIN4 构建的更大装配体中,另有多个适配子如 DDB1、DDA1 和 DET1。共同组成的这些成分形成了一个灵活的“回收队”,识别诸如 c‑Jun 和 ETS2 等特定转录因子,这些因子在细胞生长和癌症中经常起作用。
捕捉复合体的三维结构
为了理解这个回收队如何运作,研究人员使用了单颗粒冷冻电子显微镜,这种技术可成像快速冷冻的蛋白并重构出高分辨率形态。他们在培养细胞中重建了人类 COP1–DET1 系统,纯化复合体并可视化出几种不同的结构状态。首先,他们解析了作为中心枢纽的 DDB1–DDA1–DET1 模块结构。DET1 呈现出一种不寻常的、部分柔性的形状,而不是刚性的盘状结构,并带有一个突出“爪状”结构可以抓握配对酶。随后,通过加入 COP1 与一类称为 E2 的辅助酶,他们捕获到更大的装配体,展示了各部分如何配合,揭示了既有紧凑堆叠态也有更开放的二聚(两个 COP1)排列。
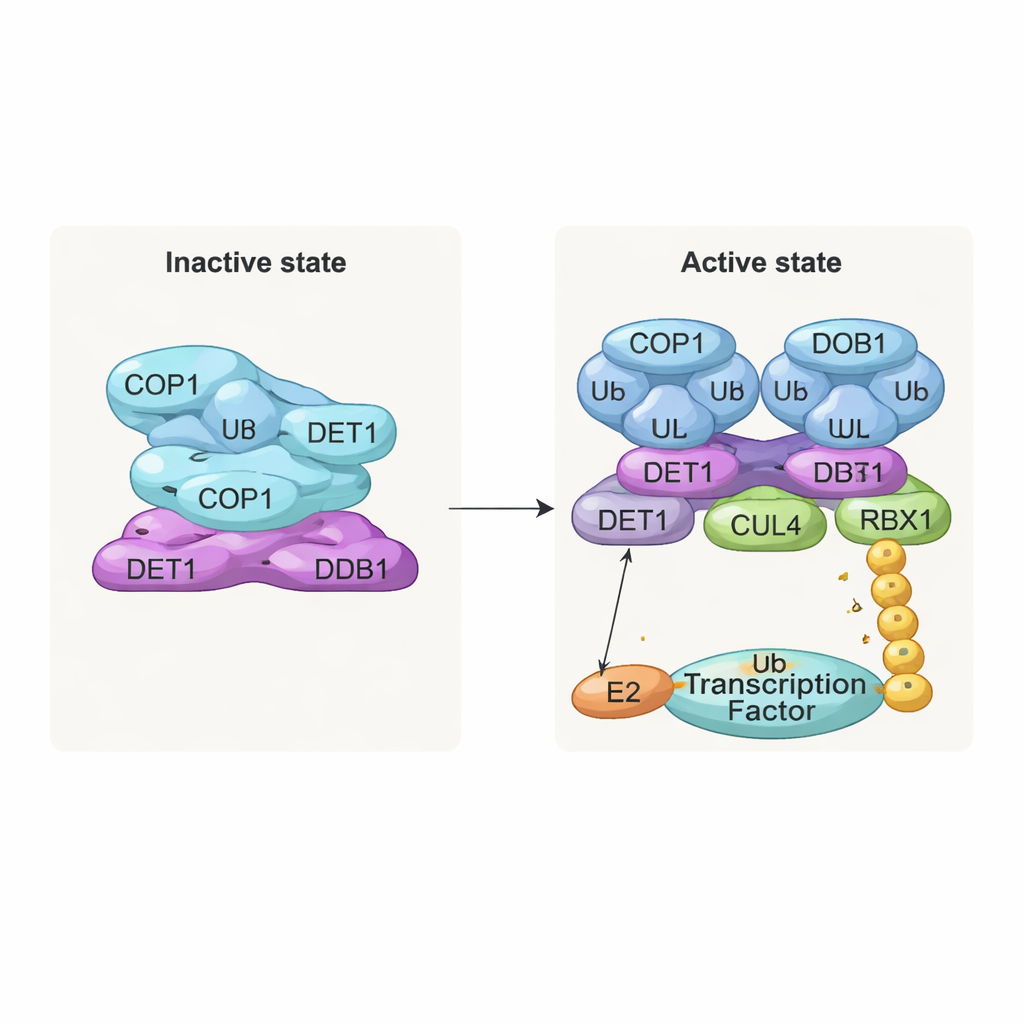
不活跃的堆叠体与活跃的二聚体
最引人注意的发现之一是由复合体重复层构成的堆叠状、类纤维结构。在每一层中,八个 COP1 分子通过它们的螺旋缠绕段相互交织,形成菱形环。它们的底物识别区,即 WD40 结构域,都朝向同一方向并被相邻层部分遮挡。这种紧密包装很可能代表一种“关闭”状态,限制了靶蛋白的接近。相反,当团队检查与 COP1 底物(如 c‑Jun 或 ETS2)共同表达的复合体时,他们观察到另一种二聚形式:两个 COP1 并排排列,WD40 结构域朝外并可用来结合存在于许多转录因子中的短“VP”基序。生化测试证实,只有这种二聚状态能有效支持在 c‑Jun 上构建长泛素链。
作为柔性桥梁与交通指挥的 DET1
DET1 成为连接机器各部分的关键组织者。其 N 端区域嵌入到 DDB1 中,使复合体锚定到 CULLIN4 骨架上,而其爪状区域则缠绕并抓住一类称为 Ube2e 的 E2 酶。详尽的突变实验表明,直接抓握这些 E2 的是 DET1,而不是 COP1,这使得 E2 被定位到靠近 COP1 的催化 RING 区。在这种排列中,Ube2e 似乎有助于在底物上放置最初的泛素标记。随后第二个 E2 酶 Ube2d3 通过 CULLIN4–RBX1 臂被招募来将这些标记延长为更长的链,从而发出完全降解的信号。换句话说,DET1 充当一座柔性的桥梁,将一个 E2 呈递给 COP1,而更大的骨架则引入第二个 E2 来完成工作。
这对健康与疾病为何重要
通过描绘这些结构状态及其活动,研究解释了同一套蛋白如何在空闲的堆叠形式与针对转录因子进行降解的活跃二聚体之间切换。这种开关对像 c‑Jun 这样的因子尤为重要,后者推动细胞分裂,且在失调时与癌症密切相关。理解 COP1 与 DET1 如何协作——DET1 的爪如何选择特定的 E2 酶、COP1 的 WD40 表面如何识别含 VP 的底物,以及活跃二聚体如何形成——为未来工作提供了蓝图。从长远看,能够稳定不活跃堆叠态或偏向活跃二聚态的药物,可能为研究人员提供在癌症及其他蛋白降解异常的疾病中调节基因控制通路的新方法。
引用: Wang, S., Teng, F., Stjepanovic, G. et al. Cryo-EM structure of the human COP1-DET1 ubiquitin ligase complex. Nat Commun 17, 543 (2026). https://doi.org/10.1038/s41467-026-68375-7
关键词: 泛素连接酶, COP1, 蛋白降解, 冷冻电镜结构, c‑Jun