Clear Sky Science · zh
K48-泛素依赖的蛋白酶切割离开内质网后的蛋白质
细胞如何决定销毁哪些蛋白质
我们的细胞不断清除磨损或受损的蛋白质,尤其是那些嵌入膜中、充当门控和感受器的蛋白质。本文揭示,细胞使用一种名为泛素的小标签,不仅仅作为通用的“垃圾”标记,而是作为一种编码,告诉膜蛋白它们将如何被分解。理解这种代码有助于解释细胞如何保持健康,也可能指导未来有意销毁致病蛋白的治疗策略。
蛋白质处置的细胞条形码
细胞用一条条小蛋白泛素的链条修饰不需要的蛋白。这些链可以通过不同方式连接,就像通过不同孔串起的珠子,每种模式可以传递不同的命令。作者关注的是已经离开内质网(ER)并在高尔基体和内体等隔室间运输的膜蛋白。他们探问两种常见链型——称为K48连接和K63连接的泛素链——究竟是可以互换的通用标签,还是会将货物引导到不同的降解通路。
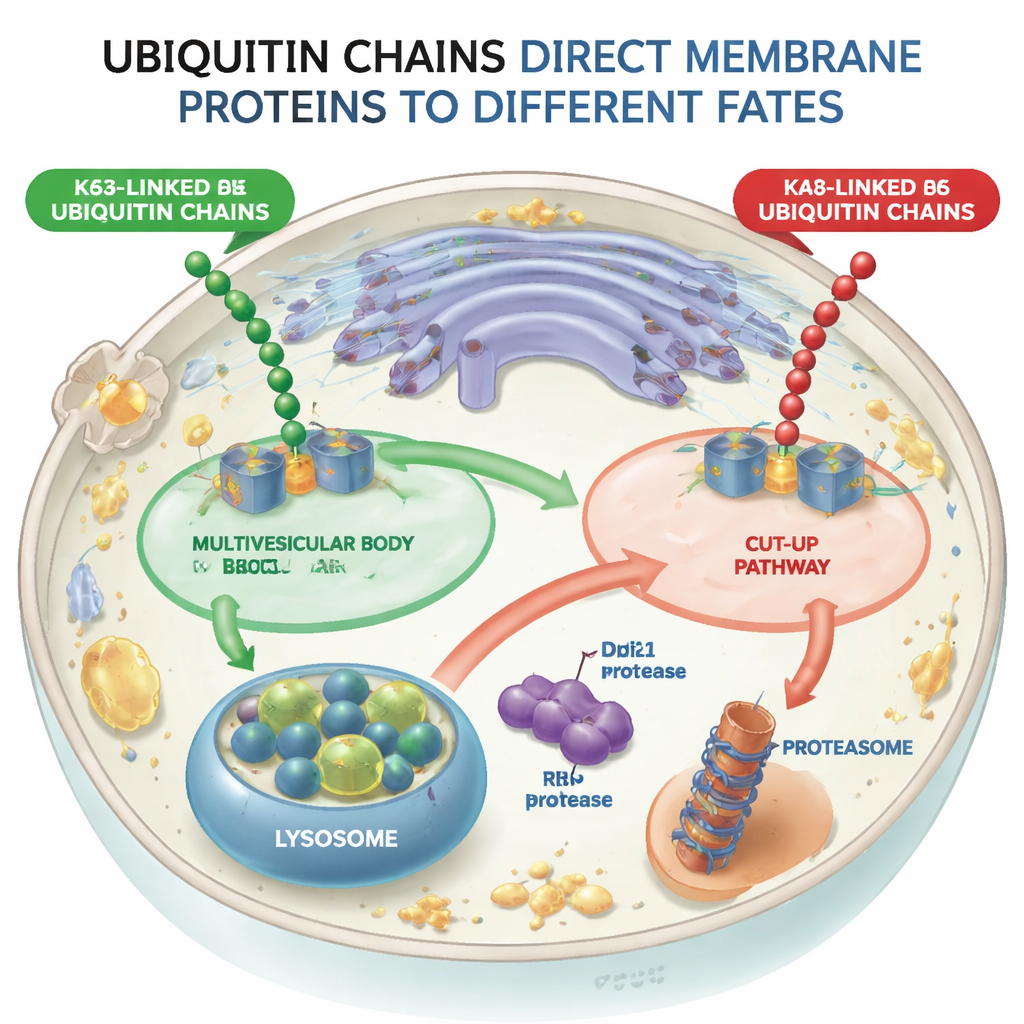
标记蛋白的两条分歧路径
研究人员以酵母为模型,构建了能够向同一测试膜蛋白(一个名为Vps10的分拣受体)附加K48或K63链的分子机器(泛素连接酶)。当Vps10带有K63链时,它被送入内体内的内部小囊——称为多泡体(MVB)——最终与溶酶体融合被降解。相反,当Vps10带有K48链时,它并不走多泡体路线。相反,它以完全不同的方式被分解,这表明细胞能区分这两种链型,而多泡体途径实际上会排斥被K48标记的货物。
将蛋白切割成两部分的“切割-出”通路
团队发现K48链会触发一种他们称为CUT-UP的蛋白切割通路,CUT-UP是“通过依赖泛素的蛋白酶对泛素化靶点进行切割”(Cleavage of Ubiquitinated Targets by Ubiquitin-dependent Proteases)的缩写。CUT-UP不是一次性将整个蛋白从膜中拉出,而是将其切成片段,随后由现有的细胞清除系统完成降解。一个关键酶Ddi1位于细胞质中,切下朝向细胞质的膜蛋白片段,该片段随后被细胞的主要蛋白粉碎器——蛋白酶体消化。与此同时,另一个酶Rbd2位于膜内,切割朝向隔室腔内的部分,将其释放到最终与溶酶体连通的空间中。只有同时阻断Ddi1、Rbd2、蛋白酶体和溶酶体酶,才能完全保护带K48标签的Vps10免受破坏,这证实了这些成分在CUT-UP通路中的协同作用。
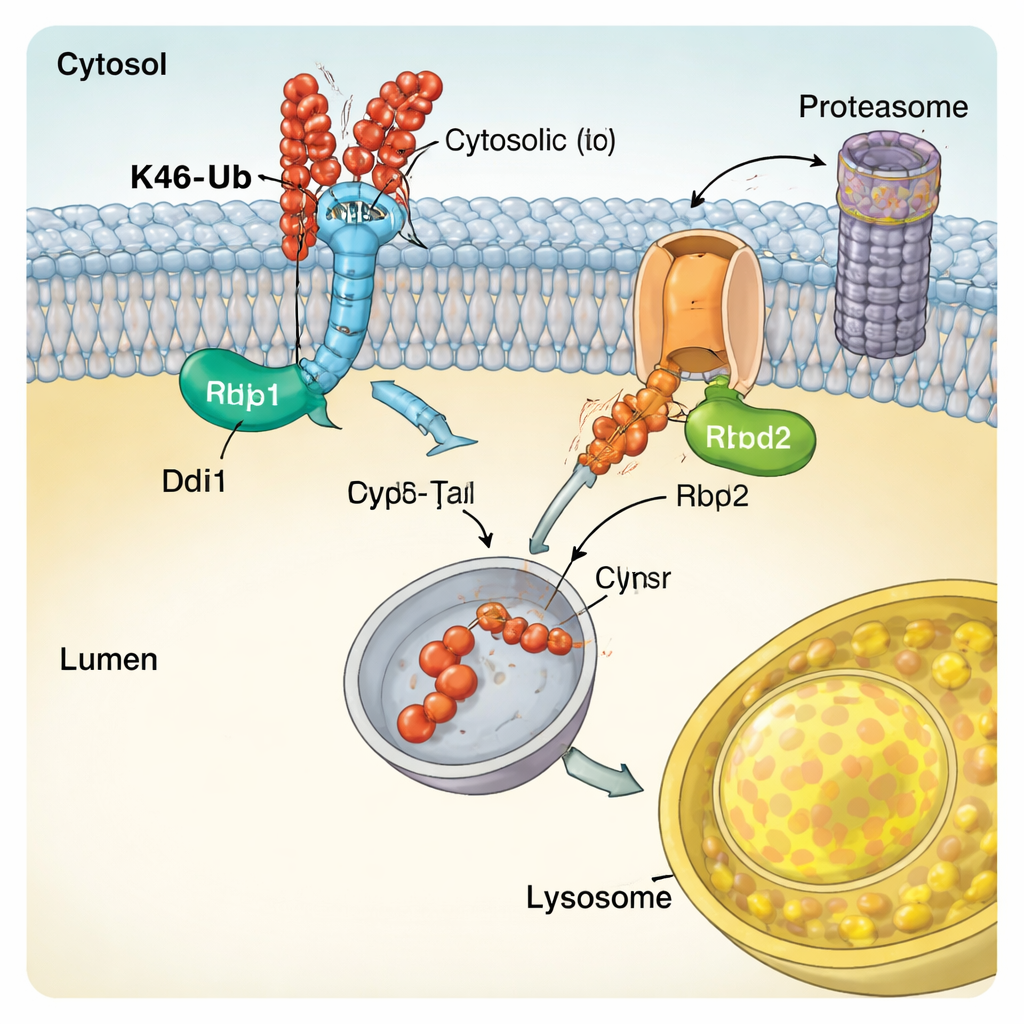
识读泛素密码的专门酶类
为了解CUT-UP如何识别其靶点,作者研究了Ddi1的分子特征。他们表明,Ddi1的中心催化核心不仅能切割蛋白,还能直接结合泛素,并且其活性受能够抓取泛素链的额外区域调控。Ddi1对K48链表现出特异性依赖,与其在CUT-UP中的作用相符。另一方面,Rbd2是跨膜的菱形酶类蛋白酶。研究发现,Rbd2的活性位点对于切割Vps10的腔面部分是必需的,并且该酶在几个分泌通路隔室中迁移,使其能够在多个细胞位置发挥作用。人细胞中存在类似酶,并已被牵连到从神经退行性疾病到癌症的多种病症,提示类似CUT-UP的机制可能具有广泛重要性。
这对健康与治疗的意义
该研究表明,不同的泛素链类型会将同一膜蛋白送入截然不同的命运——要么进入多泡体分选,要么走CUT-UP介导的切割途径——为细胞利用真实的“泛素密码”来微调蛋白质处置提供了有力证据。CUT-UP的发现阐明了顽固的膜蛋白如何被逐块拆解,并突出了Ddi1和Rbd2作为读取并执行这一密码的关键参与者。面向非专业读者的要点是:细胞并非简单地把蛋白标为垃圾;它们还指定了垃圾如何被清除。随着药物开发者设计将有害蛋白标记为泛素以便去除的工具,理解像CUT-UP这样的通路对于预测产生哪些片段以及这些片段如何影响细胞行为将是至关重要的。
引用: Minard, A.Y., Winistorfer, S., Yu, L. et al. K48-ubiquitin-dependent proteases cut-up post-ER proteins. Nat Commun 17, 1669 (2026). https://doi.org/10.1038/s41467-026-68367-7
关键词: 泛素密码, 蛋白质降解, 膜蛋白, 蛋白酶体, 溶酶体