Clear Sky Science · zh
Fsr 群体感应丧失促进生物膜形成并加剧肠球菌感染性心内膜炎的结局
在心脏瓣膜上的无声破坏者
感染性心内膜炎是一种危及生命的心脏瓣膜感染,且在全球范围内日益常见。本研究聚焦于一个主要罪犯——肠道细菌粪肠球菌(Enterococcus faecalis),探究为何某些感染格外难治。通过揭示这些细菌如何相互通信并在心脏瓣膜上构建保护性的生物膜,研究人员解释了为何某些菌株会引发更严重的疾病并抵抗抗生素,以及为何一种名为 Fsr 的细菌通讯系统出乎意料地起到抑制而非加剧损伤的作用。
细菌如何在心脏中筑起堡垒
心脏瓣膜通常要承受体内最快的血流之一,但若瓣膜表面受损,血小板和凝血蛋白会形成微小的血栓或称“植被”。这类血栓成为血流中细菌的着陆点。细菌一旦附着,就会增殖并编织成生物膜——一种粘滑、有结构的群落,能保护它们免受免疫细胞和药物的攻击。团队使用微流控装置在实验室模拟血流,并用大鼠模型在活体中再现心内膜炎,使他们能够观察粪肠球菌如何随着感染从少量散在细胞发展为厚实、成熟的生物膜。 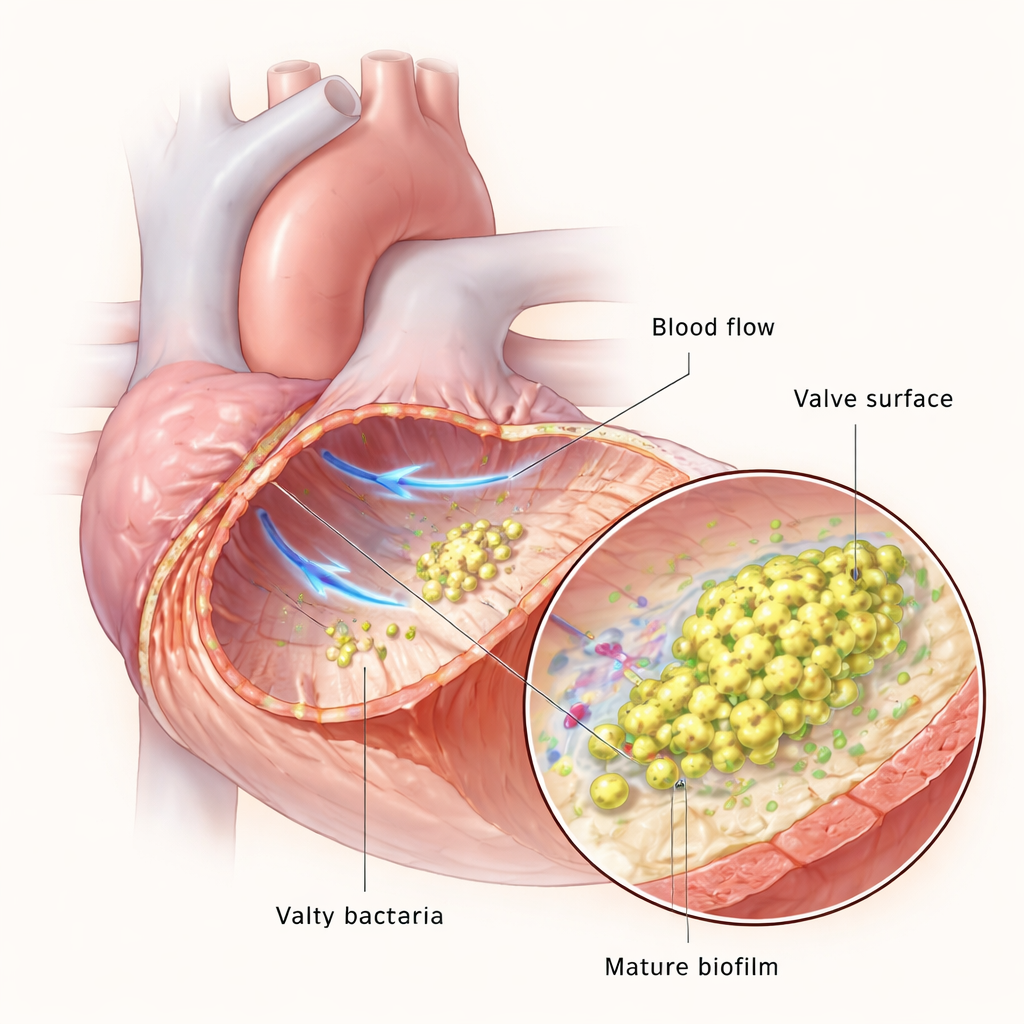
当快速血流关闭细菌“闲聊”
细菌常用群体感应来协调行为,这是一种化学“投票”系统,当细胞数量达到阈值时切换基因的开关。Fsr 是粪肠球菌所使用的群体感应系统。令人惊讶的是,研究人员发现强劲的流动液体会将激活 Fsr 所需的信号分子冲走。在早期感染中,当细菌附着在暴露的植被表面并直接承受血流的强力时,Fsr 大多处于沉默状态。只有在微菌落长大并被埋入植被更深处、免受流动冲刷时,Fsr 才会被激活。这意味着在真实的心脏内,群体感应不仅由细菌数量决定,也由它们在三维结构中的位置决定。
关闭 Fsr 让生物膜过度生长
为了测试 Fsr 对感染的实际作用,团队比较了正常细菌与缺失整套 Fsr 系统的突变株。早期,两者在瓣膜的定植能力相当。但到第三天,感染 Fsr 缺失菌株的动物其植被更大、其中包含的细菌更多。详细成像显示,它们的生物膜覆盖了血栓更多的表面,微菌落也更大。失去 Fsr 还关闭了两种关键分泌酶 GelE 和 SprE,这两种酶通常有助于塑造生物膜并可能限制过度生长。仅缺失这些酶的突变株也产生了更为庞大的生物膜,尽管不如完全缺失 Fsr 的菌株极端,说明还有其他受 Fsr 控制的因子在发挥作用。 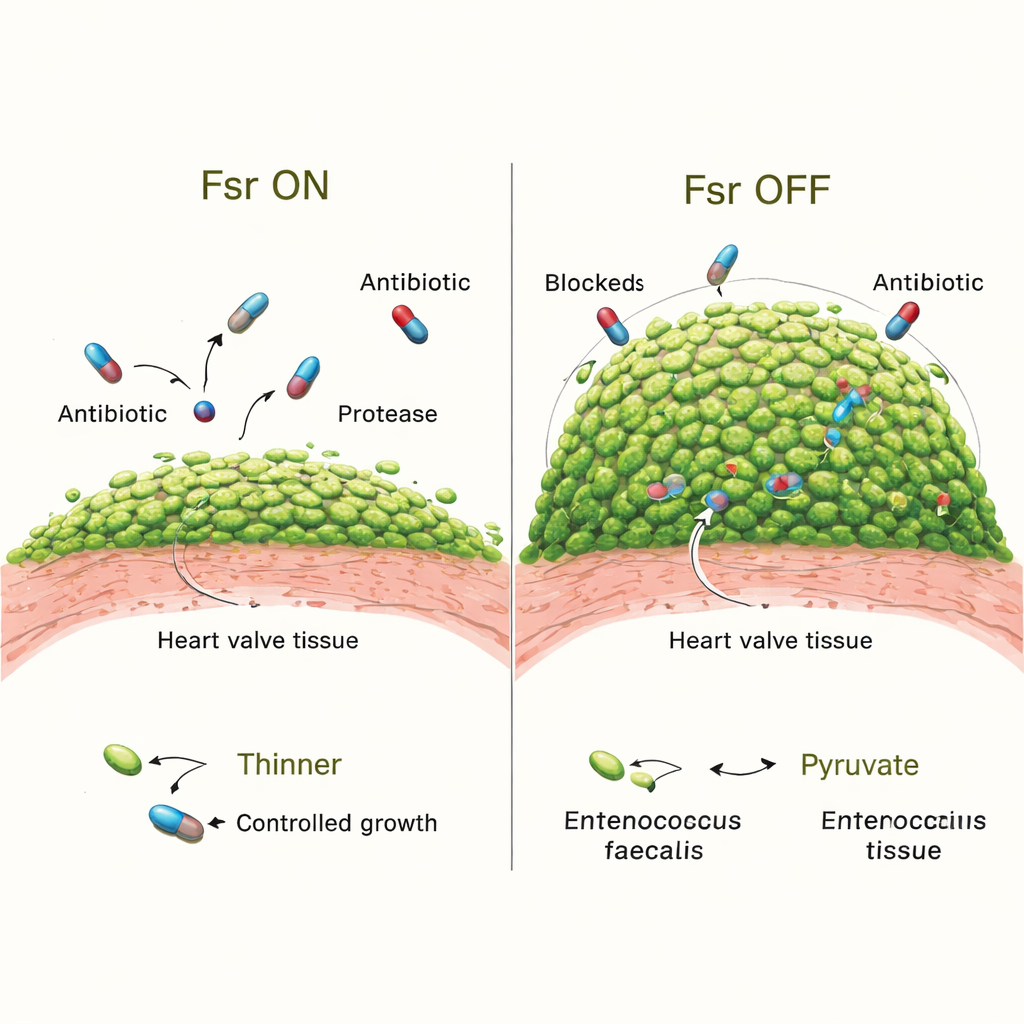
代谢重编程与更强的抗生素耐受性
对感染瓣膜内细菌的基因表达谱分析表明,Fsr 的作用不仅限于控制几种酶。没有 Fsr 时,数百个基因的活性发生改变,尤其是与糖摄取和能量产生相关的基因。lrgA 和 lrgB 这对基因尤为突出:在 Fsr 缺失的细菌中它们被强烈上调,帮助细胞更好地利用血液中存在的一种能量分子丙酮酸(pyruvate)。当研究人员在缺失 Fsr 的同时删除 lrgAB,过度生物膜生长现象消失,表明这一代谢通路在驱动过度生长的感染中发挥关键作用。值得注意的是,Fsr 缺失的生物膜也更难以治疗。在给予链霉素类氨基糖苷抗生素庆大霉素(gentamicin)的老鼠中,正常细菌感染消退、血小板计数——作为疾病严重程度的一个指标——有所改善。相比之下,Fsr 缺失的感染几乎没有反应,尽管在常规实验室耐药性检测中这些细菌并未表现出更高的药物抗性。
与人类炎症反应相关的物种特异性细节
研究还发现了这些细菌可能在人类中激发炎症的一个途径。GelE 酶可以切割人体免疫信号前体 IL‑1β,将其转化为能触发炎性反应的活性形式。有趣的是,GelE 对大鼠 IL‑1β 的切割方式不同,表现为降解而非激活,且大鼠和小鼠蛋白中缺少精确的“激活”切割位点。这种物种特异性效应提示在人体内,GelE 可能在生物膜边缘局部放大炎症,进而在心内膜炎期间加重组织损伤。
从实验台到临床:Fsr 缺失为何对患者重要
为检验这些实验发现是否在现实中具有意义,研究人员分析了来自瑞士和美国 81 名感染性心内膜炎患者分离到的粪肠球菌菌株。近一半菌株天然缺失 Fsr 系统。感染这些 Fsr 阴性菌株的患者出现持续性菌血症的天数更多——血液中可检测到细菌的时间更长——且更可能落入高严重度类别,该类别包括重症监护、延长住院、重大心脏手术或死亡。其他毒力基因无法解释这一模式,直接指向 Fsr 缺失作为更具侵袭性疾病的关键标志。
这对未来治疗意味着什么
综上,这些发现推翻了“阻断细菌通讯总会削弱感染”的简单观念。在粪肠球菌性心内膜炎中,Fsr 系统实际上抑制了生物膜扩张并使细菌对抗生素更为脆弱。当 Fsr 缺失时,细菌形成更致密的生物膜、更高效地利用血液营养,并促成顽固、持续的感染。对患者而言,这意味着缺失 Fsr 的菌株可能预示更难治疗的疾病,而盲目抑制群体感应的疗法在这种情境下可能适得其反。相反,精确地针对像丙酮酸利用这样的代谢通路,或将 Fsr 与 GelE 状态作为预后标志进行监测,可能为管理这些危险的心脏感染提供更好的策略。
引用: Antypas, H., Schmidtchen, V., Staiger, W.I. et al. Loss of Fsr quorum sensing promotes biofilm formation and worsens outcomes in enterococcal infective endocarditis. Nat Commun 17, 1668 (2026). https://doi.org/10.1038/s41467-026-68366-8
关键词: 感染性心内膜炎, 细菌生物膜, 群体感应, 粪肠球菌, 抗生素耐受性