Clear Sky Science · zh
基于转录组特征指导的中间肺泡上皮细胞清除可改善小鼠肺纤维化
为何肺组织瘢痕重要
肺纤维化是一种严重的肺部疾病,细嫩的气囊逐渐被僵硬的瘢痕组织取代,使得每一次呼吸都变得异常费力。医生知道这种瘢痕始于正常修复过程出错,但具体哪些细胞应负主要责任以及如何在不损伤健康肺组织的情况下将其清除尚不明确。本研究探索了一种读取肺细胞内分子信息的新方法,利用这些信息识别有害的过渡性细胞,并选择性地消除它们以减少小鼠的瘢痕形成。
修复过程中被“卡住”的细胞
在肺损伤后,产生表面活性物质的特殊Ⅱ型细胞通常会增殖,随后成熟为覆盖气囊并允许氧气进入血液的薄型Ⅰ型细胞。在纤维化中,许多这些细胞停留在一种介于两者之间的过渡状态,而未能完成这一转变。先前的单细胞RNA测序研究在小鼠和人类中都发现了这些中间细胞,但尚不清楚它们是仅仅作为旁观者出现,还是疾病的关键推动者。作者将注意力集中在小鼠的一类过渡细胞Krt8+肺泡分化中间体及其在人类中对应的异常基底样细胞(aberrant basaloid cells)上,这些细胞在瘢痕化的肺组织中大量出现。
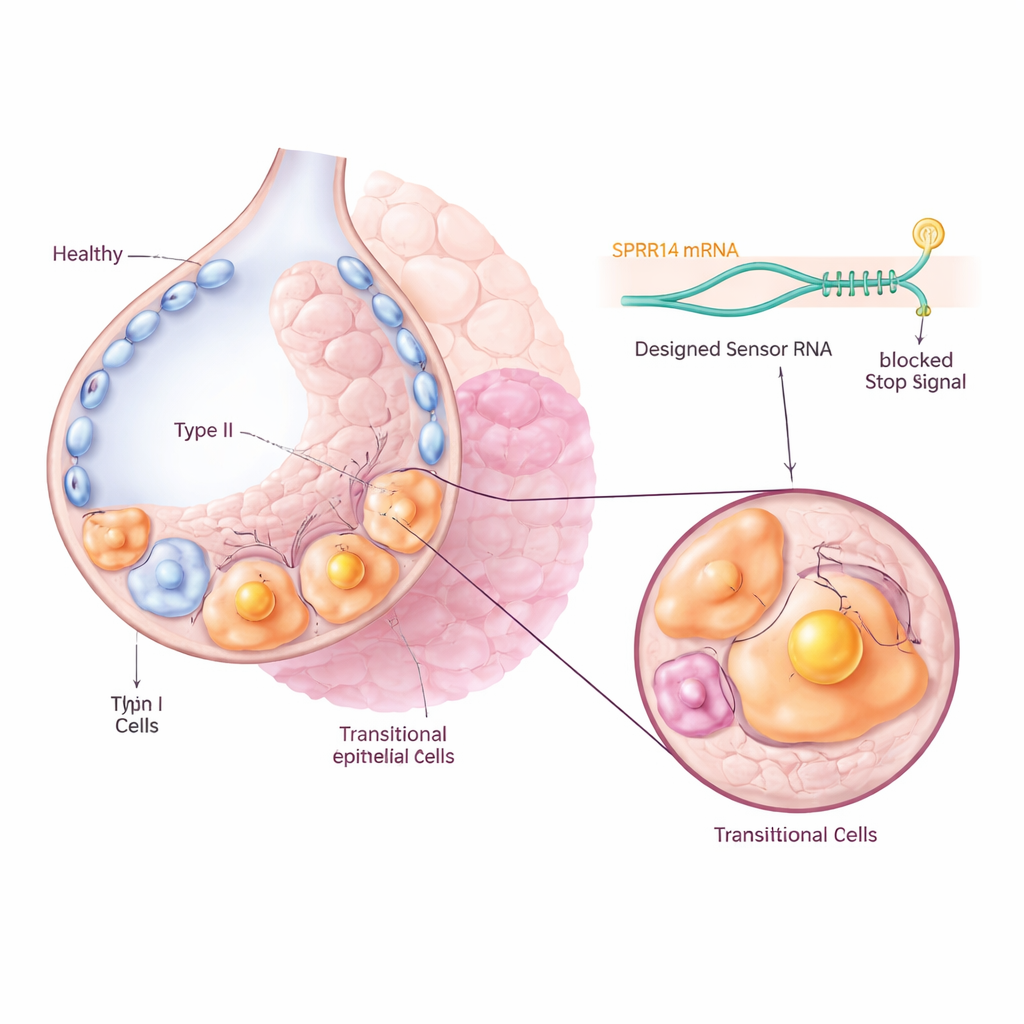
找到独特的分子“名牌”
为了在不影响健康细胞的前提下针对这些问题细胞,研究团队首先在大型基因表达数据集中搜索一种在过渡细胞群中特异性且高表达的标记物。他们鉴定出一种名为SPRR1A的分子作为突出“名牌”:在纤维化小鼠肺的Krt8+中间细胞以及特发性肺纤维化患者的KRT5-/KRT17+异常基底样细胞中高度富集,而在正常肺细胞中基本不表达。对小鼠和人类肺组织的显微镜检查也证实,SPRR1A主要出现在受伤和重塑区域,而非健康的气囊区,表明它可以作为识别病变细胞的精确靶点。
用RNA传感器给细胞“编程”
接着,研究者使用了一种新近开发的技术,称为CellREADR,它像一种细胞内分子传感器。他们设计了可以与细胞内SPRR1A RNA形成碱基配对的短RNA序列。当传感器检测到SPRR1A时,它会触发连接的“效应器”蛋白的产生,例如荧光标签或使细胞对药物敏感的受体。在小鼠中,研究人员用病毒将这些传感器—效应器构建体递送到肺细胞中。只有那些主动产生SPRR1A的细胞会开启荧光信号,从而使团队能够直接从纤维化肺中追踪并分离出过渡细胞。单细胞测序显示被标记的细胞与已知的过渡性基因特征高度一致,证实该RNA传感器准确定位了目标细胞群。
关闭有害的中间细胞
随后,研究者将效应器从无害的荧光蛋白替换为白喉毒素受体,以便在给予白喉毒素时选择性地杀死SPRR1A阳性的细胞。通过将治疗时机与化学性肺损伤后过渡细胞丰度的高峰相匹配,作者能够清除约三分之一的该细胞群。这种靶向清除导致肺瘢痕显著减少:胶原沉积降低,纤维化相关蛋白水平下降,气囊结构更趋于正常。详细分析显示,大多数SPRR1A阳性细胞具有应激或类衰老状态的标志,而一小部分具有较高的增殖能力,表明这些中间细胞既未能完成正常修复,又有助于维持纤维化过程。
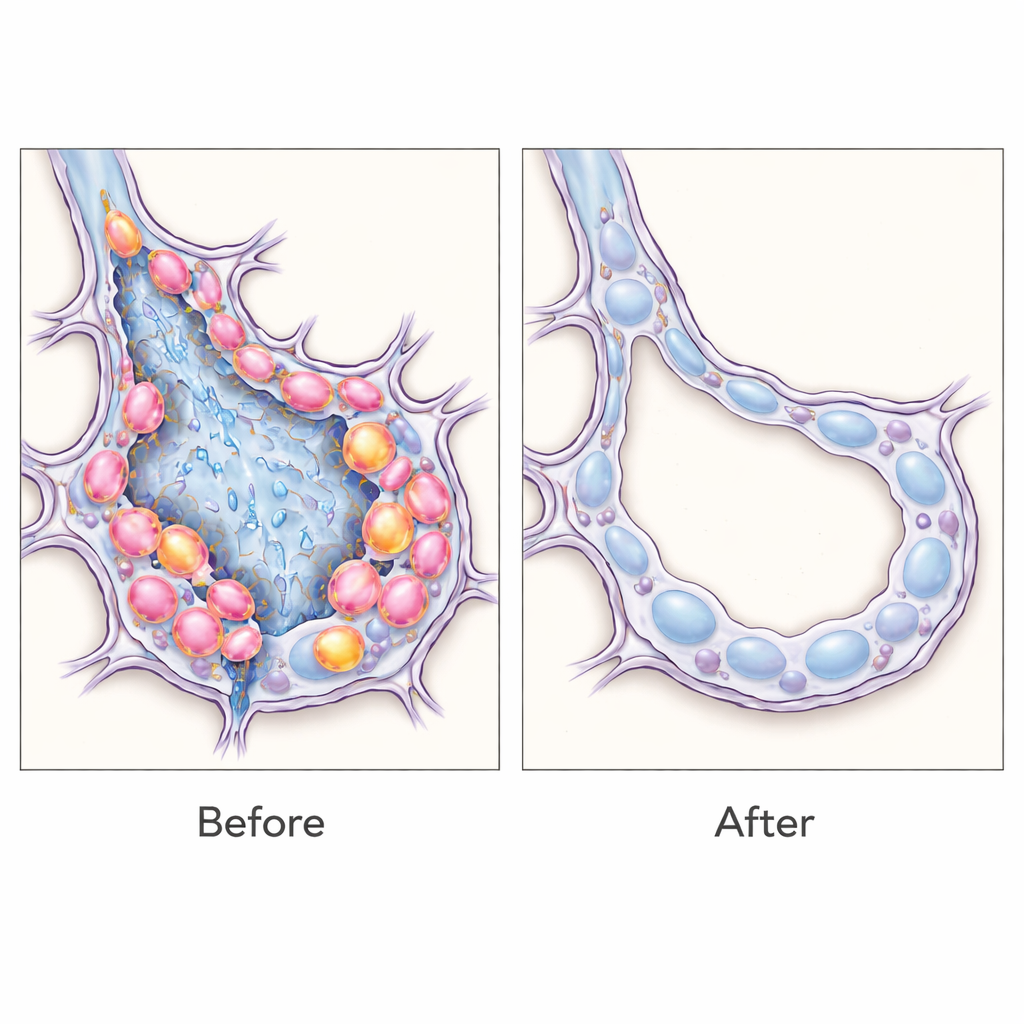
对未来治疗的意义
这些发现表明,过渡性上皮细胞不仅是疾病的标志,还是肺纤维化的主动驱动者,选择性清除它们可以使小鼠的肺组织修复朝向更健康的结构转变。更广泛地说,这项工作展示了一种灵活策略:通过“读取”细胞特异性的RNA特征,研究者可以在活组织中标记、研究乃至消除明确定义的细胞群,而无需每次都建立特制的动物模型。尽管在将此类RNA感应工具安全应用于人类之前仍需大量工作,这一方法为针对导致慢性肺瘢痕修复失常的确切细胞类型——以及潜在用于其他纤维化疾病的精准疗法——开辟了路径。
引用: Peng, F., Jiang, Cs., Zheng, Z. et al. Transcriptomic signature-guided depletion of intermediate alveolar epithelial cells ameliorates pulmonary fibrosis in mice. Nat Commun 17, 1636 (2026). https://doi.org/10.1038/s41467-026-68354-y
关键词: 肺纤维化, 肺泡上皮细胞, 单细胞RNA测序, RNA感应技术, 细胞衰老