Clear Sky Science · zh
从 TDP-43/RNA 复合体形成到与疾病相关的 TDP-43 聚集:结构与细胞学方法的研究
为何这种脑蛋白很重要
像肌萎缩侧索硬化(ALS)和额颞叶痴呆等神经退行性疾病常伴随神经细胞内错误折叠蛋白的聚集。其中一个常见罪魁是称为 TDP-43 的蛋白,它在正常情况下帮助处理 RNA——基因的工作拷贝。本研究提出了一个关键问题:在健康细胞中 TDP-43 扮演什么角色,又是什么导致一个有用的 RNA 助手变成有毒并形成聚集体的蛋白?
TDP-43 在健康神经细胞中的工作方式
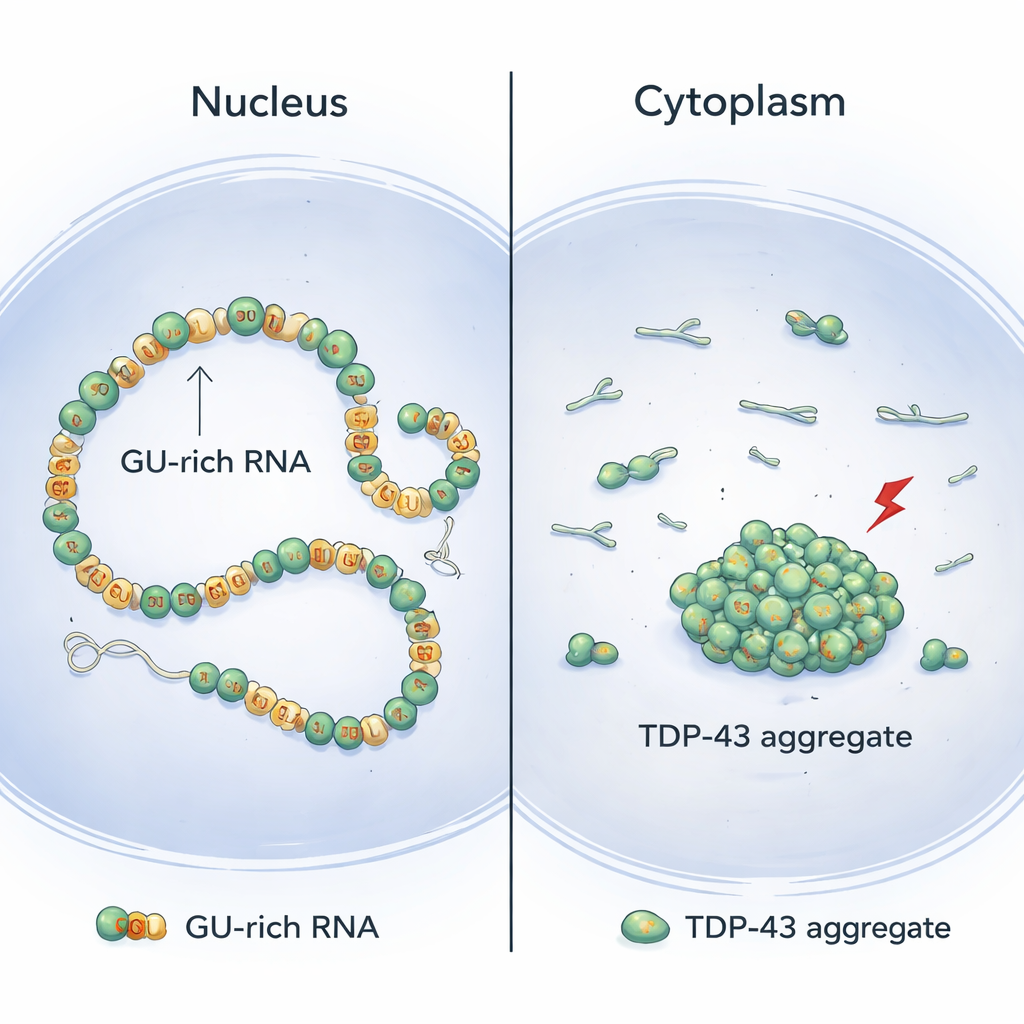
TDP-43 通常位于细胞核内,它结合富含重复“GU”碱基的长片段 RNA。通过结构生物学与细胞实验相结合,作者表明 TDP-43 分子沿这些富 GU 区域协同排列,在 RNA 上形成平滑、连续的链。当以这种方式排列时,蛋白的前端——N 端结构域在相邻分子之间保持物理分隔。因此,这些 N 端片段可以伸展并连接同一 RNA 上相距较远的 GU 富集区域,温和地环绕并压缩长内含子(基因内部的不编码区),而不会发生聚集。
蛋白内部的内在拉锯战
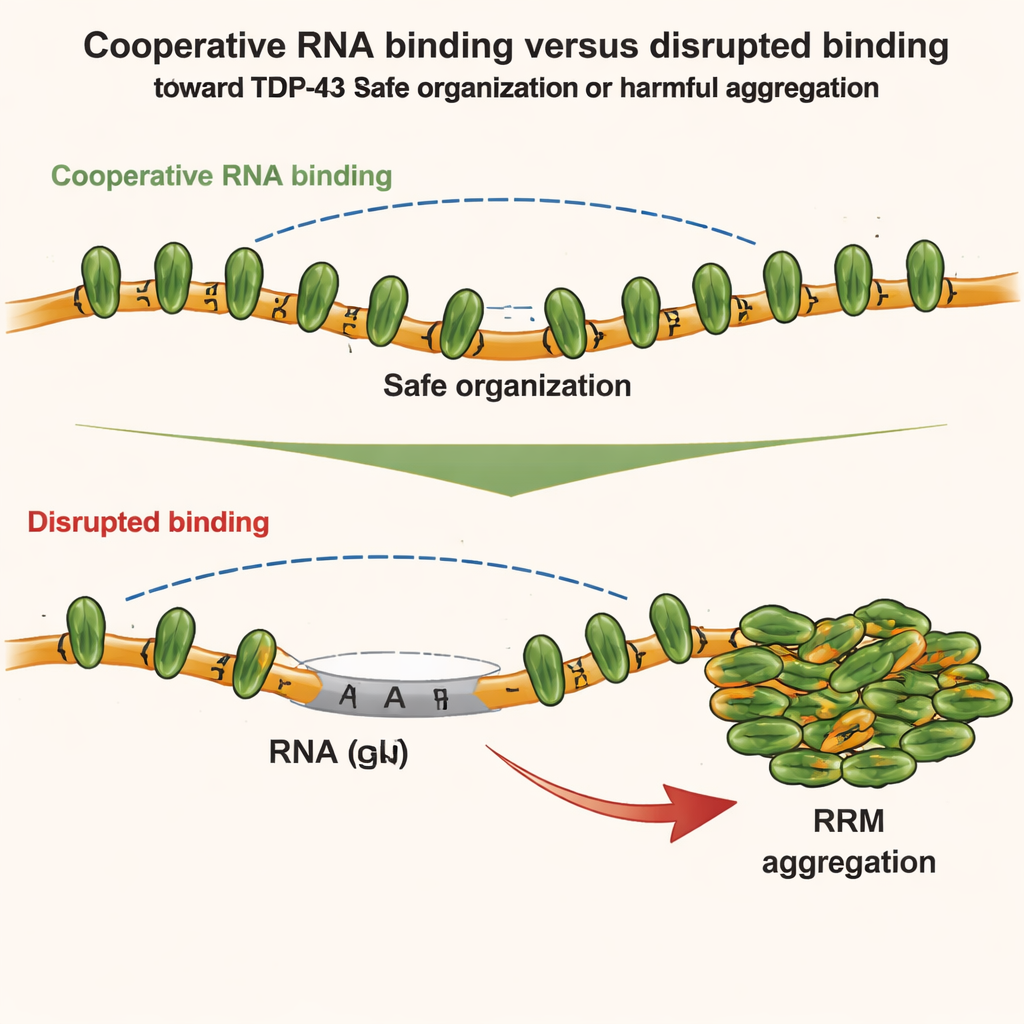
研究小组随后探讨了 TDP-43 的不同部分如何相互竞争或协同。他们关注两个区域:可以相互粘连的 N 端结构域,以及驱动沿 GU 富 RNA 协同结合的中心 RNA 结合模块。使用诸如核磁共振(NMR)光谱学、量热法和小角 X 射线散射等敏感技术,他们发现当 TDP-43 协同结合 RNA 时,链的几何构型实际上削弱了相邻分子之间直接的 N 端对 N 端接触。换言之,强烈的协同 RNA 结合抑制了局部的 N 端相互作用。但当这种协同性被破坏——例如在 RNA 中插入非 GU 片段或对 TDP-43 进行突变时——相邻蛋白的 N 端区域会靠近并能够互相结合。
从有益的压缩到有害的凝聚
这些结构学见解在活细胞中得到了验证。作者使用工程化细胞系统追踪不同 TDP-43 突变体在人工富 RNA 隔室内的混合或分离行为。他们发现协同的 RNA 结合和 N 端相互作用都以不同方式帮助将 TDP-43 组织成高阶组装体。协同结合将蛋白沿 GU 富 RNA 串联排列,而 N 端接触则将相距较远的簇连接起来。然而在轻度氧化应激下,情况会发生变化。一种化学应激因子(亚硒酸盐/砷化物)会在中心 RNA 结合基序上引起特定的化学修饰——乙酰化,使这些区更易相互粘连。如果协同结合保持完整,TDP-43 大多保持可溶状态;若协同性减弱,相邻 TDP-43 分子之间的 N 端连接就像支架一样把被乙酰化的核心拉到一起,促进不可逆的聚集。
为何 TDP-43 更易在细胞质中聚集
本工作提出的模型有助于解释为何病变神经元中常在细胞质而非细胞核发现 TDP-43 聚集物。在细胞核中,含有许多 GU 重复的长内含子很常见,有利于连续的协同结合,这会降低相邻 N 端接触的风险并允许安全的远程环绕。而在细胞质中,成熟 RNA 的 GU 富集区则少得多,这使得 TDP-43 的结合更零散、协同性更低,从而增加邻近 N 端结构域相互作用的可能性,并在应激引起化学改变时为聚集创造条件。支持这一观点的是,在细胞核中人为补充额外的 GU 富内含子可在应激下减少 TDP-43 的聚集。
这对未来治疗意味着什么
简而言之,研究将 TDP-43 描绘为在有益的 RNA 组织与有害的凝聚之间保持平衡的蛋白,协同结合 GU 富 RNA 起到一种安全机制的作用。当该保护网失效——无论是由于 RNA 序列改变、蛋白突变还是细胞应激——那些通常用于压缩长 RNA 片段的结构域就可能转而驱动有毒聚集体的形成。对非专业读者来说,关键结论是:维持 TDP-43 与 RNA 之间适当相互作用的方式,可能是预防或延缓 ALS 及相关脑病中蛋白聚集的一个有前景的策略。
引用: Feng, Y., Joshi, V., Pankivskyi, S. et al. From TDP-43/RNA complex formation to disease-linked TDP-43 aggregation through a structural and cellular approach. Nat Commun 17, 1631 (2026). https://doi.org/10.1038/s41467-026-68346-y
关键词: TDP-43 聚集, RNA 结合蛋白, ALS, 蛋白–RNA 相互作用, 神经退行性