Clear Sky Science · zh
跨物种证据表明成人人类嗜睡症的发育起源与突触黏附分子 beat-Ia/CADM2 丧失相关
为什么过度睡眠可能是个严重问题
许多人羡慕睡眠深的人,但对特发性嗜睡症患者来说,压倒性的困倦会破坏工作、学业和人际关系。这种病症使人即便夜间充分休息仍感精疲力竭,临床上对其成因仍未完全厘清。本研究将人类遗传学与果蝇和斑马鱼的实验相结合,把过度嗜睡追溯到大脑回路在发育期如何连线,指出了一种潜在的新治疗策略。
在人的 DNA 中寻找嗜睡基因
研究者首先从成千上万名报告白天过度嗜睡或频繁打盹的受试者的庞大基因组研究中挖掘数据。他们没有假定每个风险变异旁边最近的基因就是关键,而是查看基因组中更大的三维邻域,称为“拓扑域”,以纳入所有可疑基因。然后使用计算工具在果蝇中寻找对应基因,最终确定了 200 多个供测试的果蝇基因。他们在所有神经元中系统性地降低这些基因的表达,寻找睡眠远超正常的果蝇。最显著的命中之一来自“beaten path”家族基因,是人类基因 CADM2 的对应物,CADM2 编码一种有助于神经元在突触处黏附并形成连接的分子。 
嗜睡的果蝇与嗜睡的鱼
当果蝇中 CADM2 的同源基因 beat-Ia 在神经元中被下调时,果蝇在昼夜都睡得更久。它们清醒时并不迟钝;相反,睡眠片段变长,更难唤醒,而且在开灯后更快再次入睡——这些特征与人类嗜睡症非常相似。团队随后在斑马鱼(一种可以通过视频追踪睡眠的小型脊椎动物)中测试 CADM2。破坏鱼类基因 cadm2b 会使鱼类睡得更多,但并不减少其清醒时的活动量,支持该分子在维持动物警觉性方面的保守作用。
早期大脑连线如何塑造终生睡眠
一个关键见解是 beat-Ia 在大脑发育期间比在成年期更重要。通过仅在昆虫蛹期之前或之后开启基因下调,研究者表明在生命早期扰乱 beat-Ia 就足以导致终生的过度嗜睡,而仅在成体中下调几乎没有影响。他们将 beat-Ia 的作用追溯到一小群产生神经肽 F(NPF,果蝇对应脊椎动物的神经肽 Y,NPY)的神经元。在正常果蝇中,NPF 神经元向称为咽下区(suboesophageal zone)的脑区发送密集的突触投射,在那里它们与特定的抑制性(产生 GABA 的)神经元连接,这些抑制性神经元有助于稳定觉醒。在缺乏 beat-Ia 的果蝇中,该区域的大簇状突触未能形成,尽管神经纤维物理上到达了该区域。这表明,是突触形成故障而非粗糙的错误连线,使得系统更倾向于过度睡眠。
从错误连线到药物靶点
利用果蝇大脑的详尽连线图,团队鉴定出咽下区中几类接受 NPF 细胞输入并被预测为 GABA 能性的下游神经元。沉默这些细胞会增加睡眠,而激活它们会促进觉醒,这与 NPF 正常通过驱动局部抑制性网络来维持清醒的设想一致。研究者接着探讨是否可以通过增强 NPY 信号来弥补丧失的 CADM2 类功能。在 cadm2b 缺陷的斑马鱼幼体中,用能激活一种 NPY 受体亚型(类似于果蝇 NPF 受体)的药物处理,使其过度嗜睡恢复到正常水平,而对正常鱼的影响不大。这一跨物种结果表明,当突触黏附分子在发育期间出现问题时,通过在成年期增强 NPY 通路可能有助于恢复适当的睡眠—觉醒平衡。 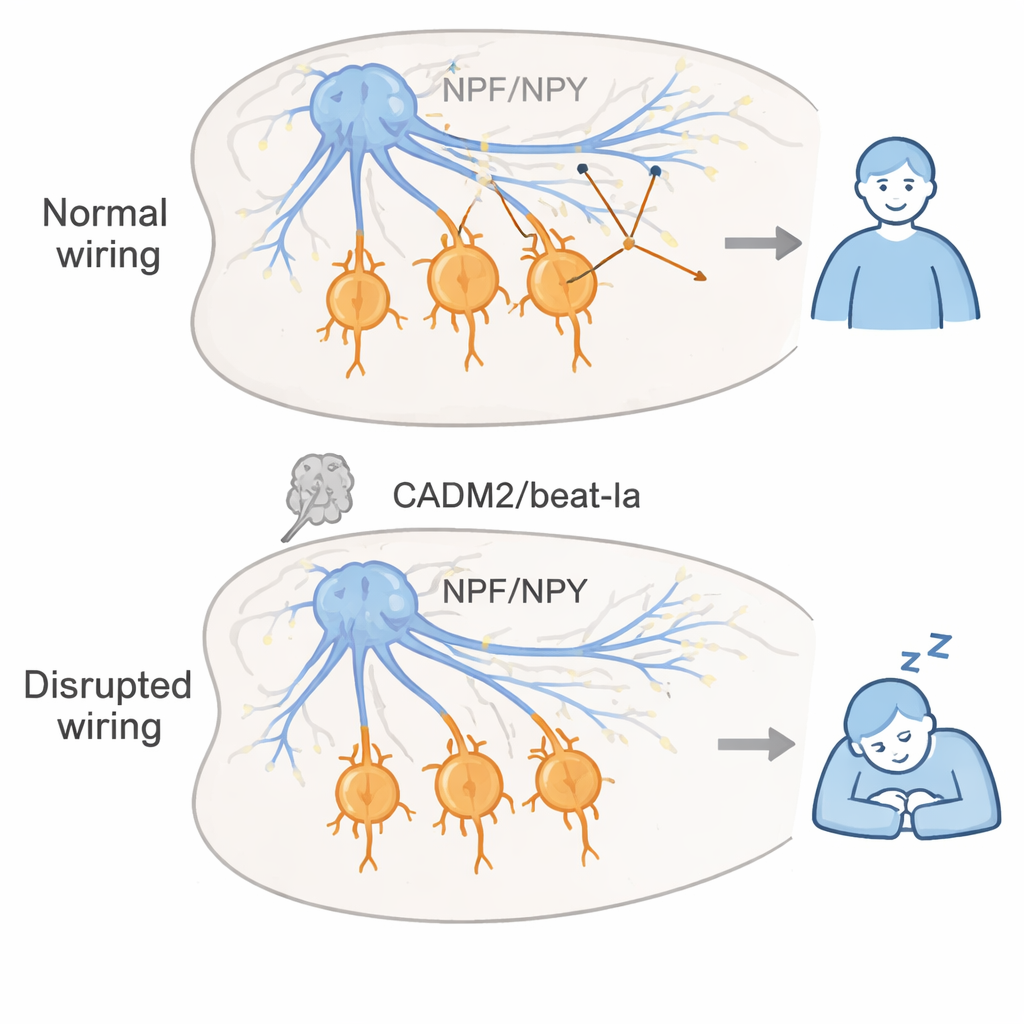
这对无法保持清醒的人意味着什么
总体而言,这项工作提出,一些形式的特发性嗜睡症可能源于早期生命中促觉醒脑回路连线的细微错误,涉及 CADM2 及相关黏附分子。这些变化并不破坏大脑本身,而是重新配置了某些睡眠与唤醒通路相互作用的强度。重要的是,研究还表明,即便连线问题始于发育期,其影响在成年后仍可能通过针对保守的神经肽系统(如 NPY)得到治疗。对患者而言,这提出了未来通过精细调节这些信号通路设计的药物,可能为使白天致残性嗜睡得到更精准缓解的希望。
引用: Mace, K., Zimmerman, A., Chesi, A. et al. Cross-species evidence for a developmental origin of adult hypersomnia with loss of synaptic adhesion molecules beat-Ia/CADM2. Nat Commun 17, 1628 (2026). https://doi.org/10.1038/s41467-026-68343-1
关键词: 特发性嗜睡症, 睡眠遗传学, 突触黏附, 神经肽 Y, 大脑发育