Clear Sky Science · zh
用纳米抗体靶向mGlyR治疗抑郁症
这种新型抑郁症方法为何重要
许多严重抑郁症患者无法从现有药物中获得充分缓解——这些药物起效慢且可能产生不良副作用。本研究探讨了一种截然不同的治疗思路:微小的工程化抗体,称为纳米抗体,它们能定位并作用于与情绪相关的单一脑受体。研究显示,其中一种纳米抗体能迅速缓解小鼠的类抑郁症状,这为难治性抑郁症提供了朝向高度靶向生物疗法的新路径。 
隐藏在脑回路中的新靶点
大多数抗抑郁药作用于经典神经递质,如血清素和多巴胺。这里关注的是另一个由甘氨酸构成的系统——甘氨酸是一种在大脑中也充当信使的小分子。最近发现的一种甘氨酸受体,称为mGlyR,在帮助控制情绪与应激反应的前额叶皮层中含量很高。患有重度抑郁症的人往往该受体表达较多,而没有mGlyR的基因改造小鼠对压力异常耐受,表现出更少的类抑郁行为。这些线索表明,降低mGlyR活性可能具有抗抑郁作用。
设计一种微小而精确的抗抑郁工具
研究人员没有寻找传统的小分子药物,而是转向纳米抗体——来自羊驼等动物的单域抗体。纳米抗体比常规抗体小得多,特异性高,且日益被探索用于药物开发。团队用表达mGlyR的细胞对一只羊驼进行免疫,然后利用噬菌体展示技术筛选数十亿片段。在61个有前途的候选者中,一种名为Nb20的纳米抗体脱颖而出,成为对mGlyR结合最强且选择性最高的分子。培养细胞试验显示,Nb20紧密附着在受体的外部结构域,但不会与相关的脑受体发生结合,证实了其精确性。
纳米抗体如何重塑细胞信号传导
mGlyR以一种不寻常的方式控制大脑信号。在其内侧,它并不直接耦联典型的G蛋白,而是与一个名为RGS7/Gβ5的辅助复合体结合,该复合体加速G蛋白信号的关闭。当该复合体高度活跃时,会抑制神经细胞反应。利用活细胞中的光学测定,研究者发现Nb20干扰了这一关闭机制:在Nb20存在且mGlyR被激活时,G蛋白关闭得更慢,说明RGS7/Gβ5复合体的效能降低。近原子分辨率的冷冻电镜图像显示,Nb20抓握住受体外部的“Cache”结构域并微妙地改变其构象。这些构象变化似乎沿蛋白传播到内侧,使RGS7/Gβ5复合体变得更松散、更具柔性,从而降低了其对信号的抑制能力。 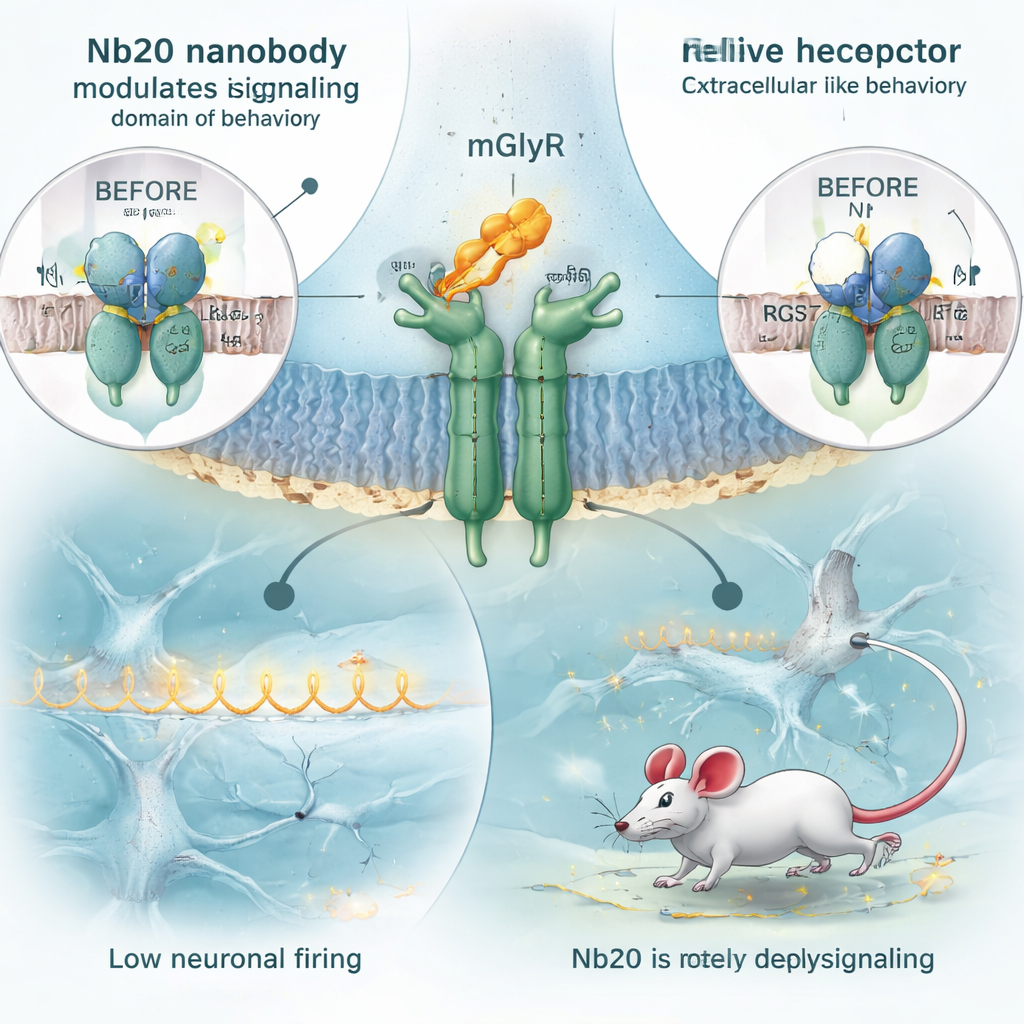
从分子作用到小鼠情绪
随后团队考察这一分子效应是否会影响行为。当将Nb20直接输送到小鼠大脑时,动物表现出更少的类抑郁特征:在基于压力的试验中挣扎时间增加,在掩埋玻璃弹珠的测试中掩埋行为减少——该行为与焦虑和强迫倾向相关。值得注意的是,通过简单的鼻内给药——将纳米抗体溶液滴入鼻腔——对经历数周不可预测压力的小鼠也产生了显著的抗抑郁样效果。在多项行为学测试中,Nb20的益处可与快速起效的抗抑郁药氯胺酮相媲美,但未见基本运动或协调性的改变。脑片记录显示,Nb20使某些前额叶皮层神经元更易被激活,这与向更积极的情绪控制回路转变一致。
这对未来治疗意味着什么
这项研究提供了概念验证:一种高度特异的生物学工具,瞄准与抑郁相关的单一受体,能迅速改善动物的情绪相关行为。研究表明,基于纳米抗体的药物靶向mGlyR,未来或可为对现有药物无反应的抑郁症患者提供新选项。在进入人体试验之前仍需大量工作,包括改善Nb20进入大脑的方式、确保安全性以及确认人体是否存在类似机制。不过,这些结果强调了一个强有力的理念:与其广泛改变脑化学,不如通过精确调整一个关键受体及其信号伙伴,将其诱导到更健康的状态,从而缓解抑郁。
引用: Laboute, T., Zucca, S., Sial, O.K. et al. Targeting mGlyR with nanobodies for depression. Nat Commun 17, 831 (2026). https://doi.org/10.1038/s41467-026-68339-x
关键词: 抑郁症治疗, 纳米抗体, 甘氨酸受体, 脑免疫疗法, 前额叶皮层