Clear Sky Science · zh
具有立体异构选择性分歧的广谱环丙烷酶的计算设计
为何微小的三元环对药物很重要
环丙烷——三元碳环——是体积小且受张力的构建单元,会显著改变药物在体内的行为。原子的精确三维排列(即立体化学)常决定一个分子是成为有效药物、还是变成无活性甚至有害的类似物。本文描述了一种计算策略,可设计酶从相同起始物可靠地合成这类环的四种可能三维形式,为更快速、更清洁地筛选药物候选分子打开了大门。
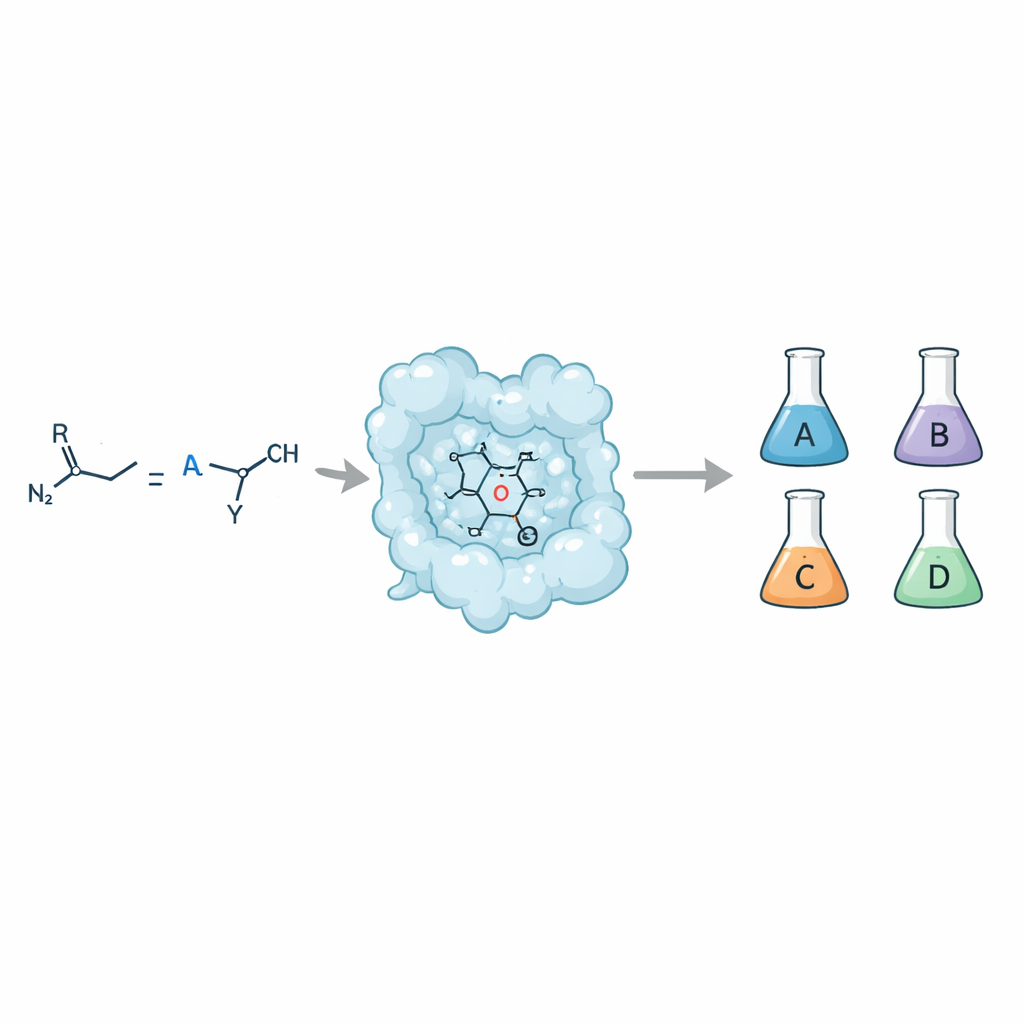
从一道配方得到四种不同结果
当一个简单的双键(烯烃)与氮亚甲基供体等卡宾来源(例如叠氮化物)反应时,可生成一个环丙烷。但是该环可以呈现四种不同的立体异构体,每种具有相同原子但在空间中排列不同。化学家希望获取每一种构型,因为它们与生物靶点的相互作用以及对吸收、代谢和安全性等药物关键性质的影响可能截然不同。传统的小分子催化剂有时能实现这种控制,但用酶——天然催化剂——实现在高选择性同时又对多种底物具耐受性一直很困难。
在电脑上设计酶
作者们开发了一套基于机制的多态态计算流程来解决这一问题。首先他们利用量子化学计算模拟每一种形成环丙烷立体异构体的短寿命过渡态——反应路径上的高能结构。将这些模型置入不同血红素含量蛋白的活性位点后,使用Rosetta蛋白设计软件评估各蛋白对每一过渡态的稳定或不稳定作用。关键在于,设计评分既奖励有利于期望过渡态的突变(正向设计),又惩罚有利于竞争过渡态的改变(负向设计),有效地教会酶“偏好”某一种三维产物而非其他。
构建完整的酶工具箱
基于该方法,团队创建了一系列“广谱”环丙烷酶。从肌红蛋白出发,他们重塑其活性位点,得到能以极高选择性产生trans-(1R,2R)环丙烷的变体,并在20多种不同烯烃上保持良好活性,包括难反应的未活化和电子贫化底物。先前工程化的肌红蛋白已经能提供互补的trans-(1S,2S)产物。为获得两种cis产物,作者转向其他血红素蛋白:他们改造了细菌的P450cam酶,得到选择性生成cis-(1S,2R)的变体,并将人类的吲哚胺2,3-双加氧酶1(IDO1)重新用于卡宾化学(此前未用于此类反应),以偏好生成cis-(1R,2S)。总之,这四种生物催化剂能够提供同一系列环丙烷的每一种立体异构体,常能在二面体和对映体两方面实现高达99%的控制。
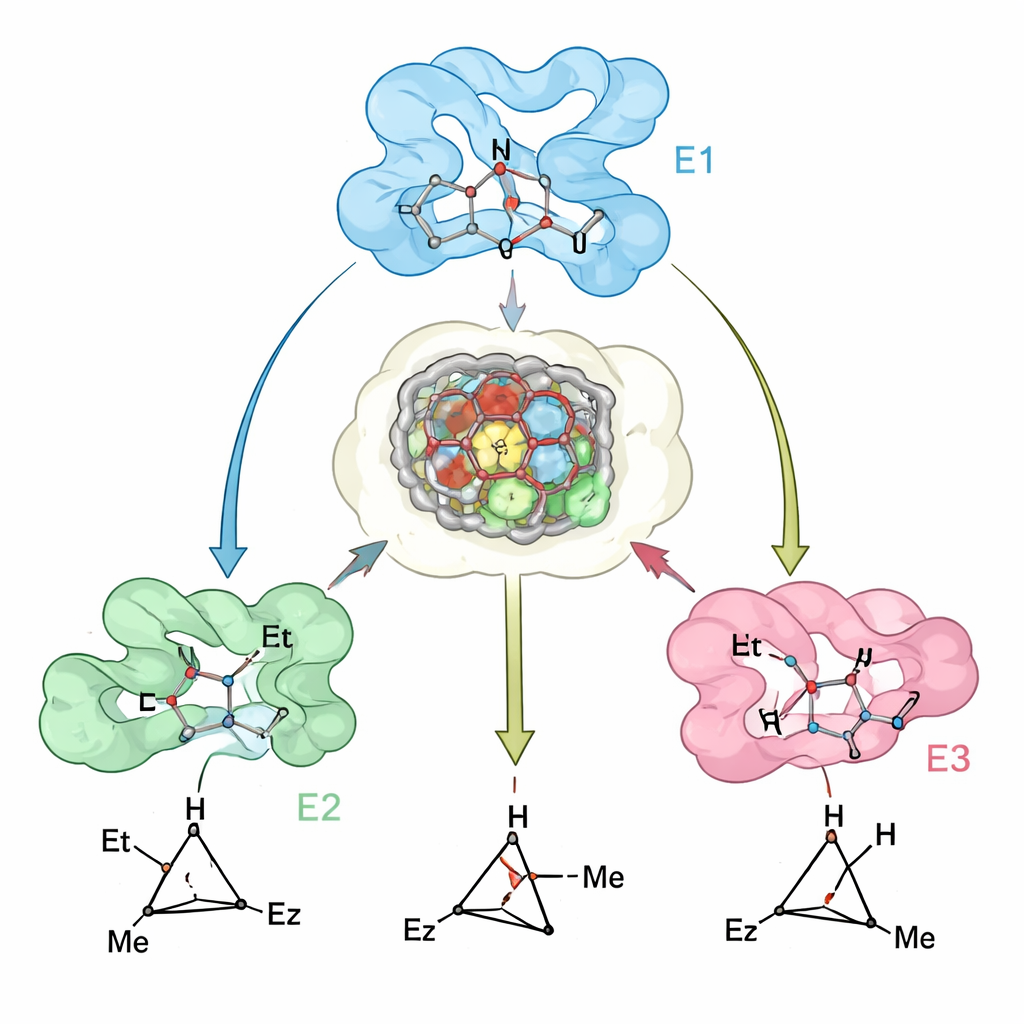
检验设计与现实的吻合程度
为检验计算模型与真实酶的契合度,研究人员解析了一个关键肌红蛋白变体的晶体结构并与预测结构进行比较。两者高度一致,实验数据突出了一个微妙但重要的特征:蛋白活性位点是预先组织好的以迎合首选过渡态,而附近环与螺旋的小幅移动则使“错误”过渡态的结合在能量上不利。在预测较不准确的情况——例如对于一些体积较大的底物——差异可追溯到建模未能充分捕捉的主链移动,这指明了改进未来设计方法的明确方向。
对未来药物与催化剂的意义
通过将基于物理的过渡态建模与巧妙的蛋白重设计相结合,这项工作展示了酶催化反应的立体化学结果可以被预先编程,而不必仅靠试错进化来发现。所得的环丙烷酶套件为化学家提供了一种实用手段,能从广泛的起始烯烃合成完整的环丙烷立体异构体集合,大大简化了药物发现和天然产物合成中的构效关系研究。相同策略应可推广到其他酶类型和反应类别,加速开发能够对复杂分子提供精确三维控制的生物催化剂。
引用: Shen, Z., Siriboe, M.G., Ren, X. et al. Computational design of generalist cyclopropanases with stereodivergent selectivity. Nat Commun 17, 1620 (2026). https://doi.org/10.1038/s41467-026-68327-1
关键词: 生物催化, 环丙烷化, 酶设计, 立体化学, 血红素蛋白