Clear Sky Science · zh
SHOC2-KRAS-PP1C 复合体结构揭示了 RAS 亚型特异性决定因子并为通过 RAS 抑制剂干预复合体组装提供见解
细胞如何决定何时生长
我们的细胞依赖一套内部连线系统来决定何时生长、分裂或保持静止。该系统的核心是 RAS 蛋白——这些微小的分子开关在癌症中经常出问题。本研究深入探讨了一组特定蛋白(SHOC2、RAS 和 PP1C)如何组装在一起以翻转一个关键的生长开关,以及现代抗癌药物如何可能被调整以更有效地阻断这一过程并防止肿瘤逃避治疗。
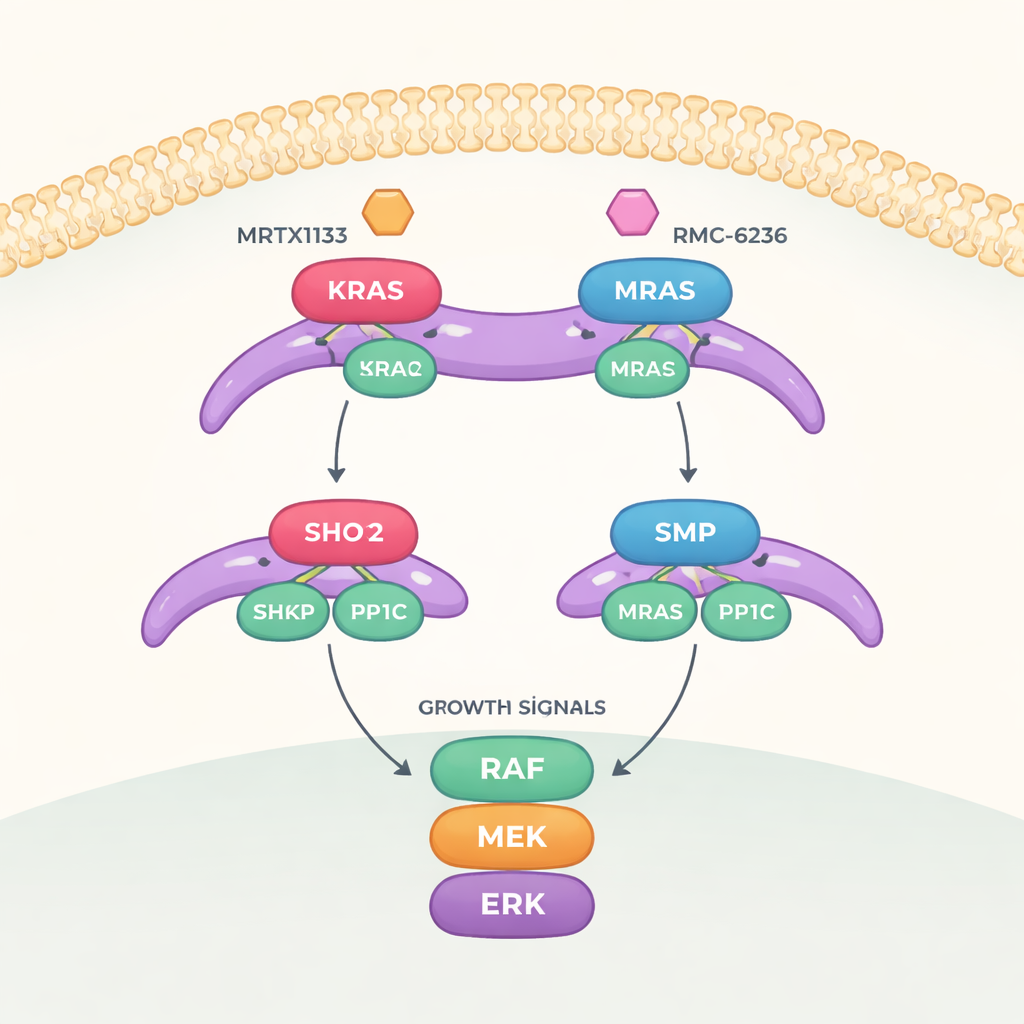
由三部分构成的生长开关
该工作聚焦于被称为 MAPK 的信号通路,它将来自细胞表面的生长信号传递到细胞核。要将这一路径完全开启,另一个称为 RAF 的蛋白必须从“关闭”状态切换到“开启”状态。这个切换受一个三元复合体的控制,复合体由 SHOC2(作为支架起连接作用)、PP1C(去除磷酸标签的酶)和处于活性状态的 RAS 蛋白组成。组装后,这个三联体去除了 RAF 的特定位点上的磷酸标记,使其能够激活下游的生长级联反应。
为何低亲和力的伙伴在癌症中仍然重要
RAS 蛋白有几种类型。MRAS 与 SHOC2 和 PP1C 形成非常稳定的复合体,而更常见的癌症驱动子 KRAS、HRAS 和 NRAS 则形成较弱的同类复合体。出人意料的是,由突变 KRAS、HRAS 或 NRAS 驱动的癌细胞对 SHOC2 展现出强烈依赖,尽管它们的复合体稳定性较低。大型基因筛查数据表明,许多携带特定 RAS 突变的肿瘤——尤其是影响关键位点如 Q61 和 G13 的突变——对失去 SHOC2 非常敏感,这意味着这种组装对它们的存活至关重要。
揭示 KRAS 复合体的形态
此前,科学家们仅获得了基于 MRAS 的高分辨率结构。较弱的 KRAS 版本太容易解离而无法捕获。在本研究中,作者利用与疾病相关的突变来微妙增强组件之间的接触,从而稳定 SHOC2–KRAS–PP1C 复合体,使其在冷冻电镜下得以成像。他们发现整体结构与 MRAS 复合体大体一致,但 KRAS 缺少 MRAS 用来更紧密抓握 SHOC2 和 PP1C 的若干小结构特征。结果,KRAS 组装埋藏的接触面积较小,形成的键更少,这解释了它本质上为何不如 MRAS 稳定,尽管在 KRAS 过度活跃的肿瘤中它仍然极为重要。
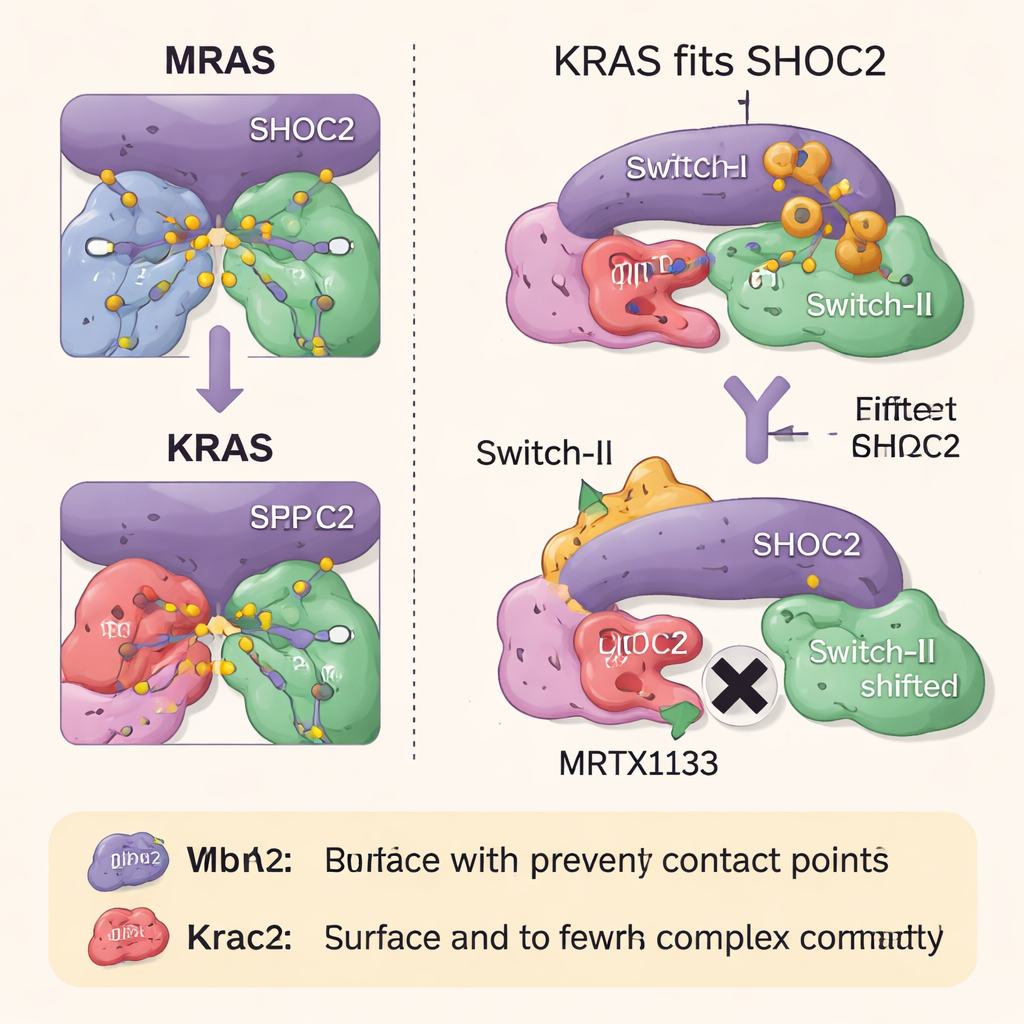
RAS 药物如何阻断复合体组装
研究团队接着探索了两类针对 RAS 的药物如何影响这一三元复合体。MRTX1133 被设计为结合到靠近 KRAS 可塑区域 Switch-II 的口袋,将该区域锁定成与 SHOC2 表面相冲突的构象。这强烈阻止了新的 SHOC2–KRAS–PP1C 复合体形成,尽管对已存在的复合体解离的效果较弱。第二种药物 RMC-6236 与一个辅助蛋白(环孢素 A)协同作用,同样阻断了 SHOC2 结合所需的 KRAS 表面。然而,这两种药物天然并不结合 MRAS,因此高亲和力的 MRAS 复合体仍然完好,并可能在 KRAS 被抑制时帮助重新激活生长通路。
迈向双重靶向以防止耐药
为了检验是否可以进行双重靶向,研究者们工程化了一种 MRAS 变体,使其 Switch-II 口袋被改造,可以让 MRTX1133 结合。该突变体仍能与 SHOC2 和 PP1C 形成强复合体,但药物现在可以阻断其组装并在试管实验中降低其激活 RAF 的能力。结合对 SHOC2 结合化合物的数据,这些结果表明设计能够同时关闭基于 KRAS 和基于 MRAS 的复合体的药物是切实可行的。对非专业读者而言,关键结论是:癌细胞使用多条密切相关的备用开关来维持生长信号,尤其是在其中一个开关被药物抑制时。通过理解这些蛋白组装体的精确形状和接触点,研究人员现在可以规划同时打击两条备用通路的疗法,从而使 RAS 驱动的癌症更难以适应并产生耐药性。
引用: Bonsor, D.A., Finci, L.I., Potter, J.R. et al. Structure of SHOC2-KRAS-PP1C complex reveals RAS isoform-specific determinants and insights into targeting complex assembly by RAS inhibitors. Nat Commun 17, 1614 (2026). https://doi.org/10.1038/s41467-026-68319-1
关键词: RAS 信号传导, KRAS 抑制剂, MAPK 通路, 蛋白质复合体, 药物耐药