Clear Sky Science · zh
HEXIM1 单体间自抑制决定 7SK RNA 结合特异性及 P‑TEFb 失活
为什么这个小小的 RNA 对基因调控很重要
每个细胞都必须决定何时开启或关闭基因,这通过对驱动 RNA 生成的酶进行精细控制来实现。本文揭示了一种小蛋白 HEXIM1 如何与一种称为 7SK 的非编码 RNA 协同工作,像安全闩一样约束该酶。理解这一分子安全系统有助于解释细胞如何防止基因活动失控,并阐明病毒(如 HIV)如何劫持相同的机器。
对基因表达的分子刹车
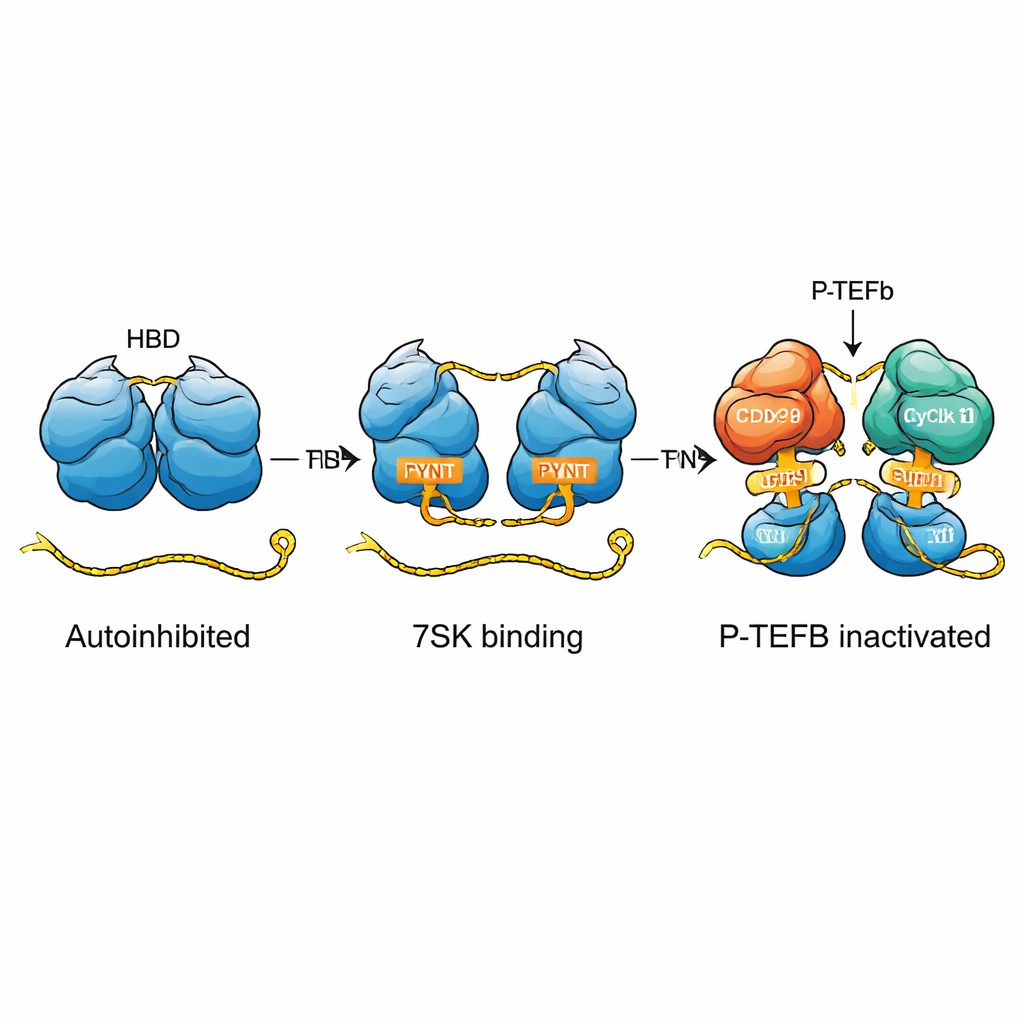
在人体细胞中,表达基因的一个关键步骤由称为 P‑TEFb 的因子控制,它帮助 RNA 聚合酶 II 从停滞状态进入高速转录。HEXIM 蛋白,尤其是 HEXIM1,在抑制 P‑TEFb 活性方面起着核心作用。它们在一个以 7SK RNA 为核心的大型复合体(7SK RNP)内发挥作用。当 HEXIM1 与 7SK 联手时,它们将 P‑TEFb 锁住,使其无法推动转录。此前未解的一环是 HEXIM1 自身如何避免过早地抓取 P‑TEFb,以及 7SK RNA 如何在恰当时机将 HEXIM1 从非活性状态翻转为活性抑制因子。
自我拥抱的蛋白被束缚
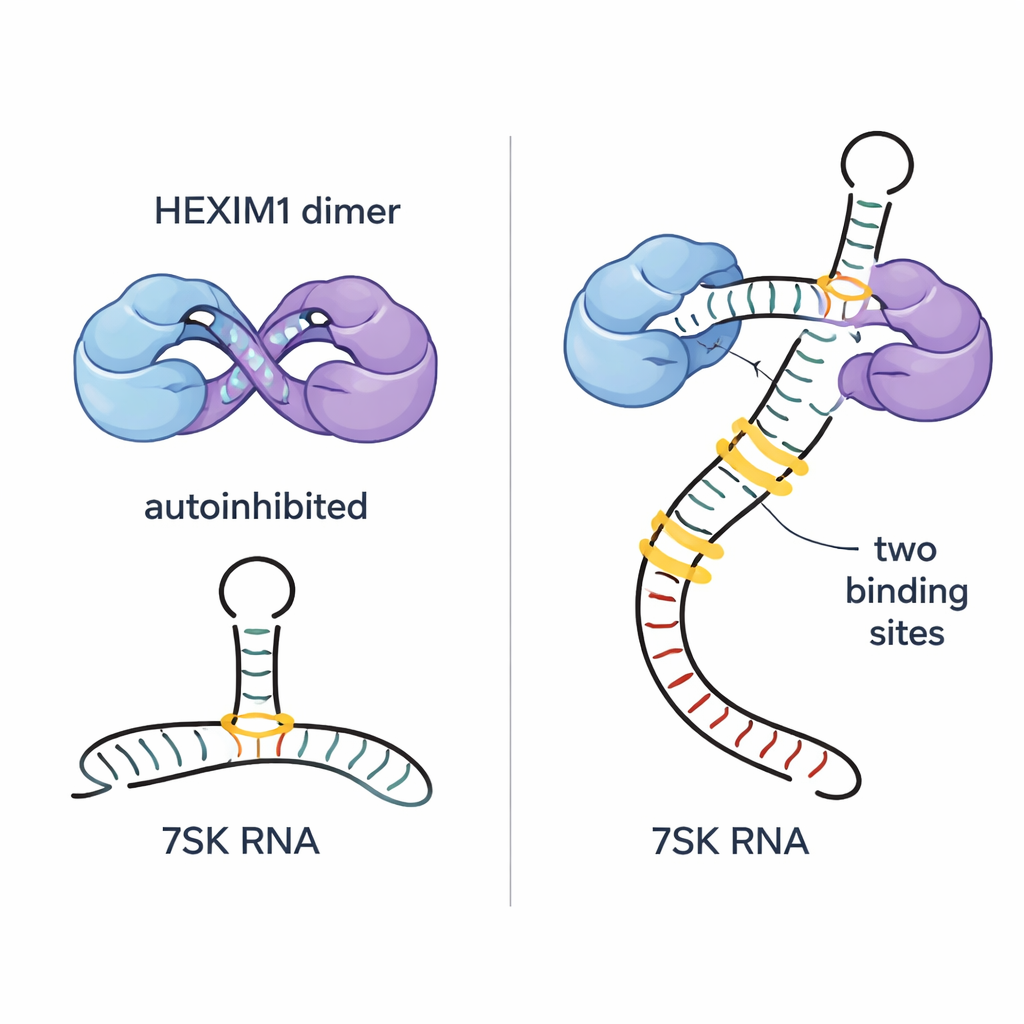
作者表明 HEXIM1 自然形成二聚体——两条相同的蛋白链配对——且每条链的柔性中间部分相互缠绕,形成一种“自我拥抱”构象。在这种状态下,一个关键的短肽段称为 PYNT 基序(通常用于结合并关闭 P‑TEFb 激酶活性)被掩藏在两链的界面处。研究组利用灵敏的核磁共振(NMR)与生物物理学方法,绘制出两单体中带正电的碱性区与带负电的酸性区如何相互作用以形成这种自抑制二聚体。这种内在限制使 HEXIM1 在没有 7SK RNA 时不会随意夹持 P‑TEFb。
7SK RNA 如何解锁 HEXIM1
7SK RNA 含有若干结构特征,其中包括一个称为 SL1 的长茎环区域。通过将该 RNA 解剖成较小片段并追踪 NMR 信号的细微变化,研究者定位了沿 SL1 的五个潜在 HEXIM1 结合位点。其中两个位点突显为高亲和力的对接点;这两个位点都具有富 A–U 的双链段和邻近的富 U 的凸出区,能够形成特殊的三碱基相互作用。研究组发现 HEXIM1 二聚体的每一半各结合线性 7SK RNA 上的这两个强结合位点之一。当两个位点同时被占据时,HEXIM1 的中心区发生重排,打破自我拥抱的接触并暴露被隐藏的 PYNT 基序,从而有效地使蛋白准备捕获 P‑TEFb。
选择正确的 RNA 构象——并避免错误的
7SK RNA 并非只有一种构象;它可以在呈现两个高亲和力位点的线性形式和仅有一个合适位点的类环形构象之间切换。作者表明 HEXIM1 的自抑制使其出人意料地挑剔:二聚体对单个位点的结合较弱,但对提供两个强位点的完整线性 SL1 片段结合得更紧且具有协同性。这个双位点要求防止 HEXIM1 停留在细胞中其他随机的 RNA 上,从而使其结合高度特异于能组装为有效抑制复合体的线性 7SK 构象。他们还证明,在 RNA 结合区域附近引入额外负电荷(模拟在某一关键丝氨酸上的磷酸化)会削弱 RNA 结合但不完全破坏自抑制,这可能是细胞在需要时释放 P‑TEFb 的一种机制。
从分子开关到细胞影响
总体而言,这项研究将 HEXIM1 描述为一个精细调节的分子开关。在其静息的自我拥抱状态下,HEXIM1 将能阻断 P‑TEFb 的 PYNT 片段隐藏起来。只有在遇到具有两个恰当排列结合位点的线性 7SK RNA 时,蛋白才会切换到“开启”状态,暴露这些片段以捕获并失活 P‑TEFb——通常是同时捕获两个拷贝。该机制解释了细胞如何利用一种小 RNA 和一个柔性的蛋白对转录施加精确控制,并为理解细胞信号、化学修饰或像 HIV Tat 这样的病毒蛋白如何改变停滞与活跃基因表达之间的平衡提供了更清晰的框架。
引用: Yang, Y., Murrali, M.G., Galvan, S. et al. HEXIM1 inter-monomer autoinhibition governs 7SK RNA binding specificity and P-TEFb inactivation. Nat Commun 17, 1570 (2026). https://doi.org/10.1038/s41467-026-68285-8
关键词: 转录调控, 7SK RNA, HEXIM1, P-TEFb, HIV Tat