Clear Sky Science · zh
剪接因子基因 SF3B1 的新生变异与神经发育障碍相关
当单个基因扰乱大脑的早期蓝图
为什么有些儿童在妊娠和分娩看似正常的情况下仍会出现学习困难、癫痫或喂养问题?这项研究聚焦于一个名为 SF3B1 的基因,它帮助细胞处理遗传信息。研究人员表明,这个基因中的新发、随机变异会微妙地扰乱脑细胞读取 DNA 指令的方式,从而导致一种此前未被识别的神经发育综合征。
遗传信息的主编辑者
我们体内的每个细胞在制造蛋白质之前,都必须将原始的遗传文本转换为清晰的指令。这一步称为 RNA 剪接,会去除非编码片段并拼接有用部分。SF3B1 是细胞“剪接机器”的核心组分。此前,SF3B1 的改变主要与肿瘤相关,人类在生命过程中肿瘤细胞会获得该基因的突变。新的研究提出了另一个问题:如果从受孕起每个细胞中就存在有害的 SF3B1 变异,会发生什么?
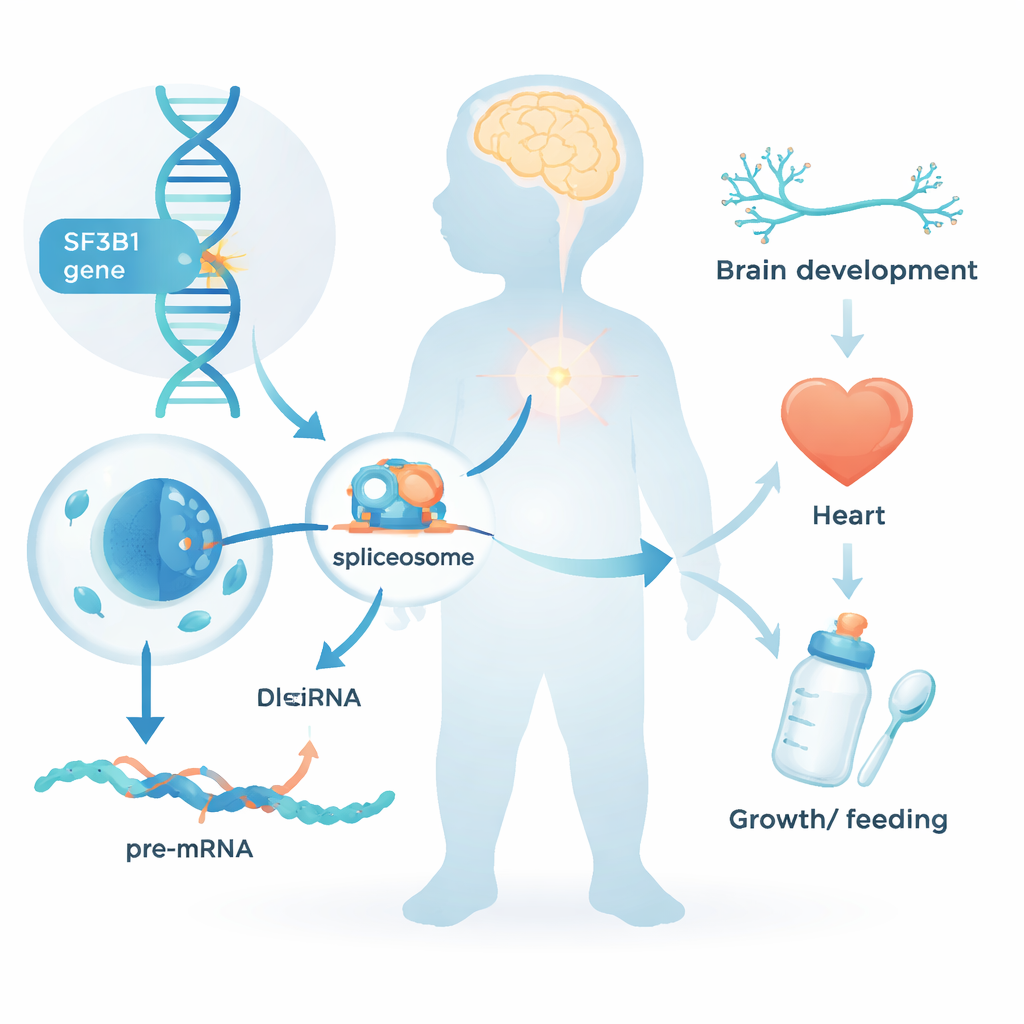
一种新识别的儿童综合征
研究团队收集了 26 名携带罕见 SF3B1 变异的儿童和青年的数据,这些变异大多为新发——即既非从任何一方父母继承。几乎所有人都有神经发育问题:翻身、坐、走或说话等里程碑发生延迟;多为轻至中度的智力障碍;以及约一半病例出现癫痫。许多人肌张力低,需要额外的喂养支持,有时需经胃管进食。面部特征有细微异常但各不完全相同;一个显著且常见的特征是高腭或腭裂。若干参与者还出现心脏畸形、发育受限或头围小,表明 SF3B1 变异的影响超出了大脑范围。
两类基因改变、两种临床模式
研究者将 SF3B1 变异大致分为两类。一类为“功能缺失”改变,例如导致提前终止的变异,预计会减少功能性 SF3B1 蛋白的量。另一类为错义变异,其中蛋白的单个氨基酸被替换。通过对患儿临床特征进行聚类,团队观察到携带错义变异的个体往往出现更严重和更复杂的问题,包括更高比例的心脏与胃肠异常、矮小和小头畸形。相比之下,功能缺失变异有时可从轻微受影响甚至看起来健康的父母处遗传下来,这提示仅仅降低 SF3B1 的量在某些人中可能与较轻的症状相容。
微调错误,而非完全失效
为了弄清楚错义变异在细胞内的作用,科学家在实验室细胞系中重现了这些变异。令人惊讶的是,这些变异的 SF3B1 蛋白仍能在一定程度上执行基本的剪接功能,足以拯救那些正常 SF3B1 被沉默的细胞。这排除了简单的功能缺失解释。利用深度 RNA 测序,团队随后在全转录组范围内进行了分析,发现错义变异会微妙地改变数百个基因的剪接方式,尤其是通过改变外显子末端选择的剪接位点以及偶发的外显子跳跃。总体扰动程度低于经典癌症相关 SF3B1 突变 K700E,但仍然相当显著:许多受影响基因参与大脑发育、神经连线及 RNA 处理与蛋白质合成等基本过程。
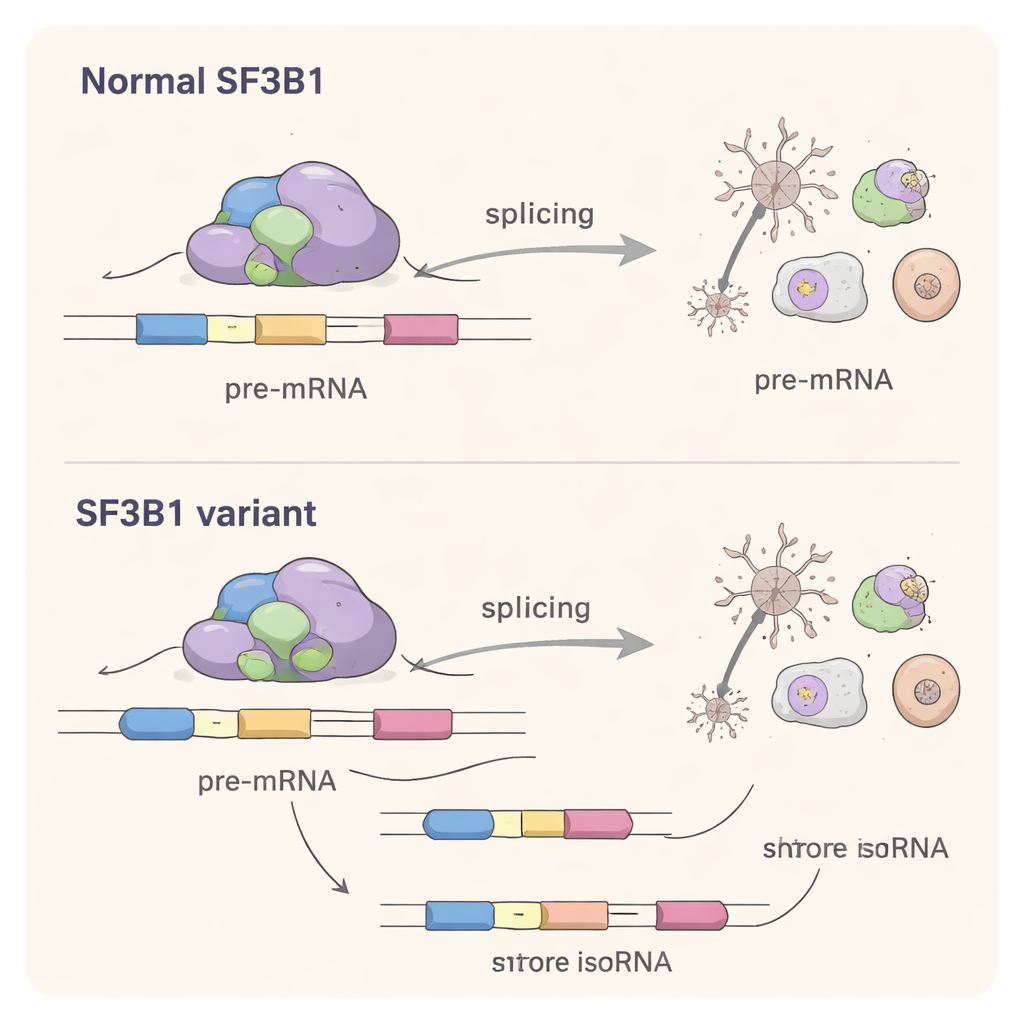
癌症与脑部疾病之间的共同机制
尽管大多数与神经发育相关的 SF3B1 变异发生在与众所周知的癌症突变不同的位置,但它们扰乱的是相同的核心过程:RNA 中剪接位点的精确识别。研究显示,这些发育期变异具有自身的“剪接特征”,其选择的备选剪接位点通常比癌症中偏好的位点更接近正常位点。这支持一种功能改变机制:突变蛋白与正常拷贝竞争,使剪接机器在许多基因中偏向一些略微错误的选择。
对家庭与未来研究的意义
对受影响家庭而言,这项工作将 SF3B1 识别为一种新的神经发育障碍致因,现可在遗传门诊中进行检测,可能终结长期的诊断寻找。更广泛地说,它把 SF3B1 加入到一小类但不断增长的剪接基因名单中:这些基因的改变可在何时何种方式发生时既驱动癌症,又引发儿童期脑疾病。通过绘制特定 SF3B1 变异如何重塑 RNA 剪接的图谱,研究为未来旨在针对性纠正错误剪接的治疗奠定了基础。
引用: Uguen, K., Bergot, T., Scott-Boyer, MP. et al. De novo variants in the splicing factor gene SF3B1 are associated with neurodevelopmental disorders. Nat Commun 17, 1569 (2026). https://doi.org/10.1038/s41467-026-68284-9
关键词: RNA 剪接, SF3B1, 神经发育障碍, 新生变异, 剪接体病