Clear Sky Science · zh
cfGWAS揭示无细胞DNA末端基序的遗传基础
漂浮在血液中的DNA线索
每时每刻,微小的DNA片段在我们的血液中漂浮,来自正在凋亡或更新的细胞。医生已经利用这种“无细胞DNA”来筛查妊娠期情况并寻找癌症的早期信号,但我们对这些片段如何产生和被清除知之甚少。本研究通过史无前例规模的遗传学追踪,揭示了哪些人类基因塑造了这些DNA片段末端的细微模式——这些信息可能能改善液体活检的灵敏度,并指向免疫和炎症疾病的新治疗思路。 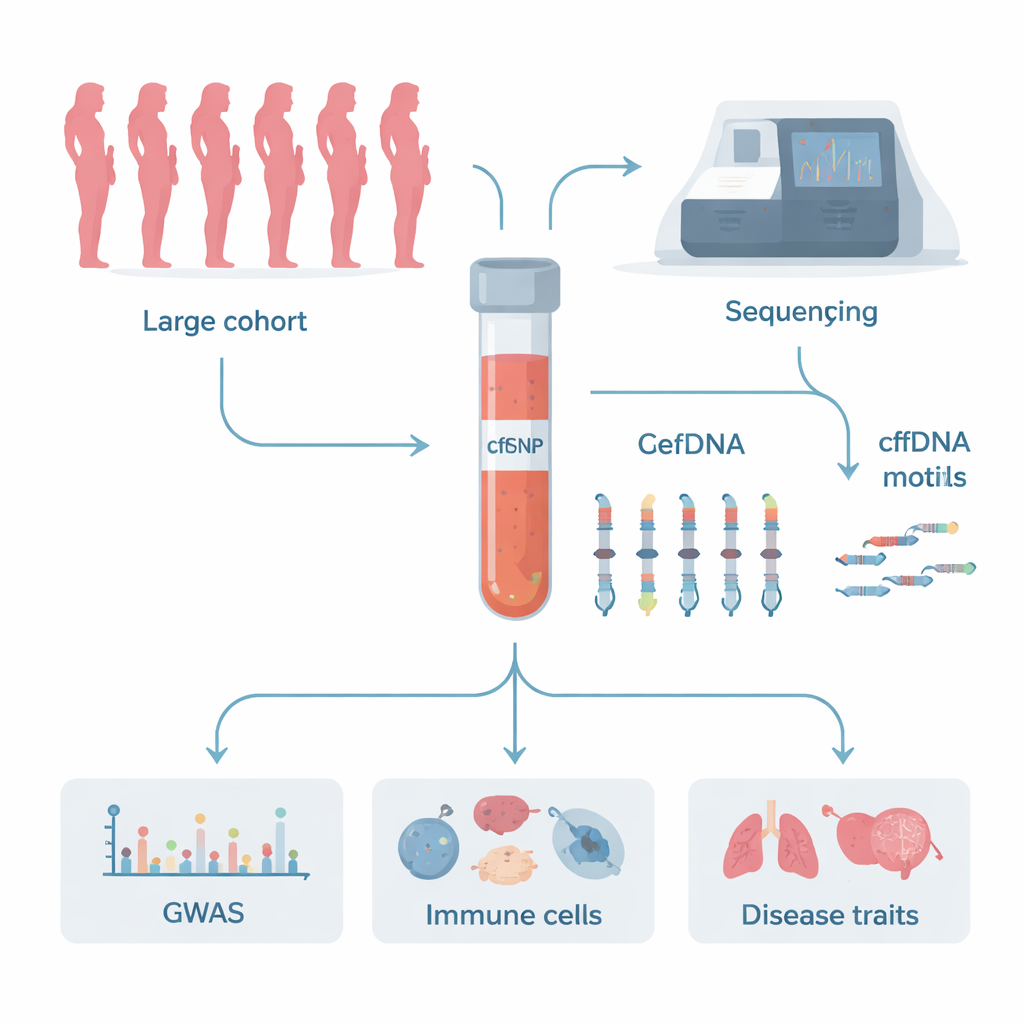
这些自由漂浮的DNA片段是什么?
无细胞DNA(cfDNA)由短小的遗传物质片段组成,作为细胞死亡或主动释放内容物的一部分进入血液、唾液和尿液等体液。在妊娠期,母体血液中的胎儿cfDNA使非侵入性产前检测成为可能。在癌症中,来自肿瘤的cfDNA可在肿块可见之前提示疾病。除了cfDNA的总体量外,研究者现在关注其“片段组学”:每段片段的长度、断切方式,以及在片段起始端出现的短序列模式,或称“末端基序”。这些末端基序像分子指纹,反映了DNA被切割的方式与位置,体现了酶的作用和供体细胞类型的信息。
对DNA片段模式的大规模遗传扫描
为了找出哪些基因影响这些末端基序,作者开展了一种新型的全基因组关联研究,称为cfGWAS。他们分析了来自中国28,016名接受常规产前筛查的孕妇的血样。利用同一低覆盖测序数据,他们既提取了这些女性的遗传变异,又计算出cfDNA片段末端所有256种四核苷酸基序的详细频率。通过在统计模型中校正年龄、孕周和技术因素,他们扫描了近2.9百万个常见遗传变异,寻找与个体间这些基序模式变化相关的位点。
决定DNA如何被切割的关键基因
cfGWAS发现了15个与176种不同末端基序显著相关的遗传区域。一些命中位点确认了已知DNA切割酶的核心作用,包括在程序化细胞死亡中帮助切割DNA的DFFB和DNASE1L3,以及相关的酶基因DNASE1L1。更令人意外的是,最强的信号来自PANX1,该基因编码细胞膜上的通道,参与细胞间通信、炎症和细胞死亡。携带不同基因变体的人在血液中常见或罕见的末端基序上表现出不同模式。研究人员在三个独立队列中复制了大多数这些信号——包括另一个中国的大型孕期队列、荷兰的孕期研究和一个较小的健康非孕成年人组——表明这些发现稳健,不局限于某一家医院或国家。 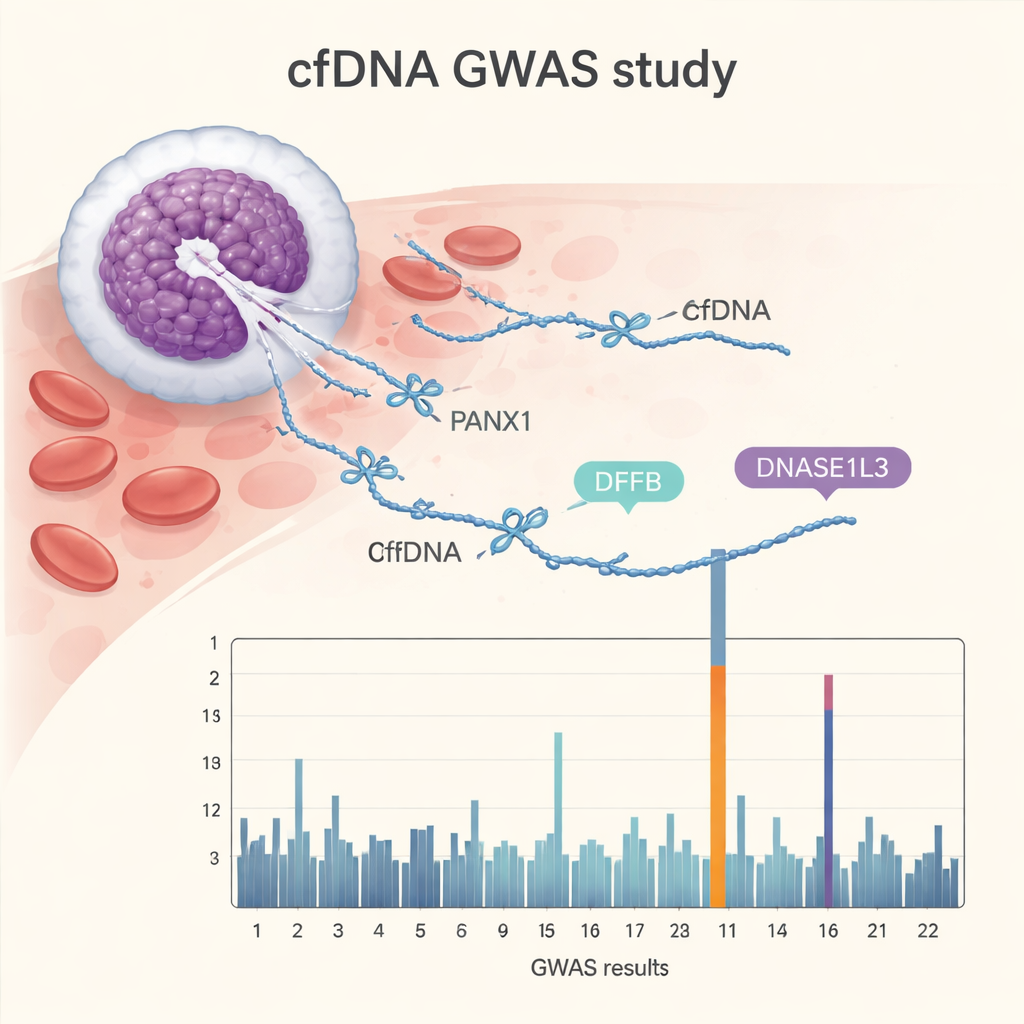
从基因到免疫细胞与身体性状
遗传信号很少孤立发挥作用,因此研究团队进一步探讨了cfDNA基序如何与同一批孕妇中测量的其他性状相关联。通过将他们的cfDNA结果与104项临床测量(如血常规、体重和肝功能)的全基因组扫描比对,他们发现某些末端基序与体重指数、白细胞计数,尤其是中性粒细胞数量等性状具有共同的遗传根源。更详细的因果分析表明,驱动基序模式变化的更可能是免疫细胞的改变,而不是cfDNA本身。附加的通路与组织分析指向血液与免疫细胞——尤其是能在免疫反应中释放DNA网的中性粒细胞——在产生和清除cfDNA方面的核心作用。在小鼠与培养细胞中关闭PANX1的实验工作证实,该基因可直接改变末端基序的多样性以及释放的cfDNA总量。
这对未来医学意味着什么
对非专业读者而言,追踪DNA片段末端的四字母模式听起来或许玄妙。但这项工作表明,这些模式并非随机噪声:它们具有遗传性,由特定基因塑造,与免疫细胞行为紧密相关,并对体重等身体特征敏感。鉴于世界各地已有数百万人为产前筛查和癌症检测接受cfDNA测序,相同的数据可以用cfGWAS重新分析,以发现更多控制DNA断裂与清除的基因。从长远看,这些知识可完善液体活检,帮助区分哪些组织释放出异常DNA,甚至指示药物靶点以增强DNA清除(如在自身免疫病中)或保护脆弱的肿瘤DNA以改善早期检测。
引用: Zhu, H., Zhang, Y., Li, L. et al. cfGWAS reveal genetic basis of cell-free DNA end motifs. Nat Commun 17, 1714 (2026). https://doi.org/10.1038/s41467-025-67940-w
关键词: 无细胞DNA, 全基因组关联研究, 液体活检, 免疫细胞, 妊娠