Clear Sky Science · zh
TCL1A抑制新生DNA甲基化的分子基础
细胞如何决定保留哪些记忆
你体内的每个细胞基本上都携带相同的DNA,但脑细胞、血细胞和皮肤细胞的行为却大相径庭。细胞“记住”自身身份的一个方式是通过添加到DNA上的化学标签,这一过程称为DNA甲基化。本研究以原子级细节揭示了一种名为TCL1A的小蛋白如何关闭负责添加这些甲基标记的酶。由于DNA甲基化和TCL1A都与癌症及生殖疾病相关,理解这一分子拉锯战最终可能为新疗法提供启发。
细胞的DNA标记机器
DNA甲基化像基因组边缘的铅笔标记,帮助在细胞发育时沉默某些基因并稳定基因组。两种酶DNMT3A和DNMT3B是放置新甲基标记的主要“写入者”,它们在早期发育和干细胞分化时发挥作用。如果这些酶发生突变或调控失衡,DNA标记模式可能被打乱,从而促成发育综合征和血液肿瘤。TCL1A是一种以在免疫细胞肿瘤中过度表达著称的蛋白。早期研究提示TCL1A可以与DNMT3A和DNMT3B结合并削弱其活性,但究竟如何实现这一抑制尚不清楚。
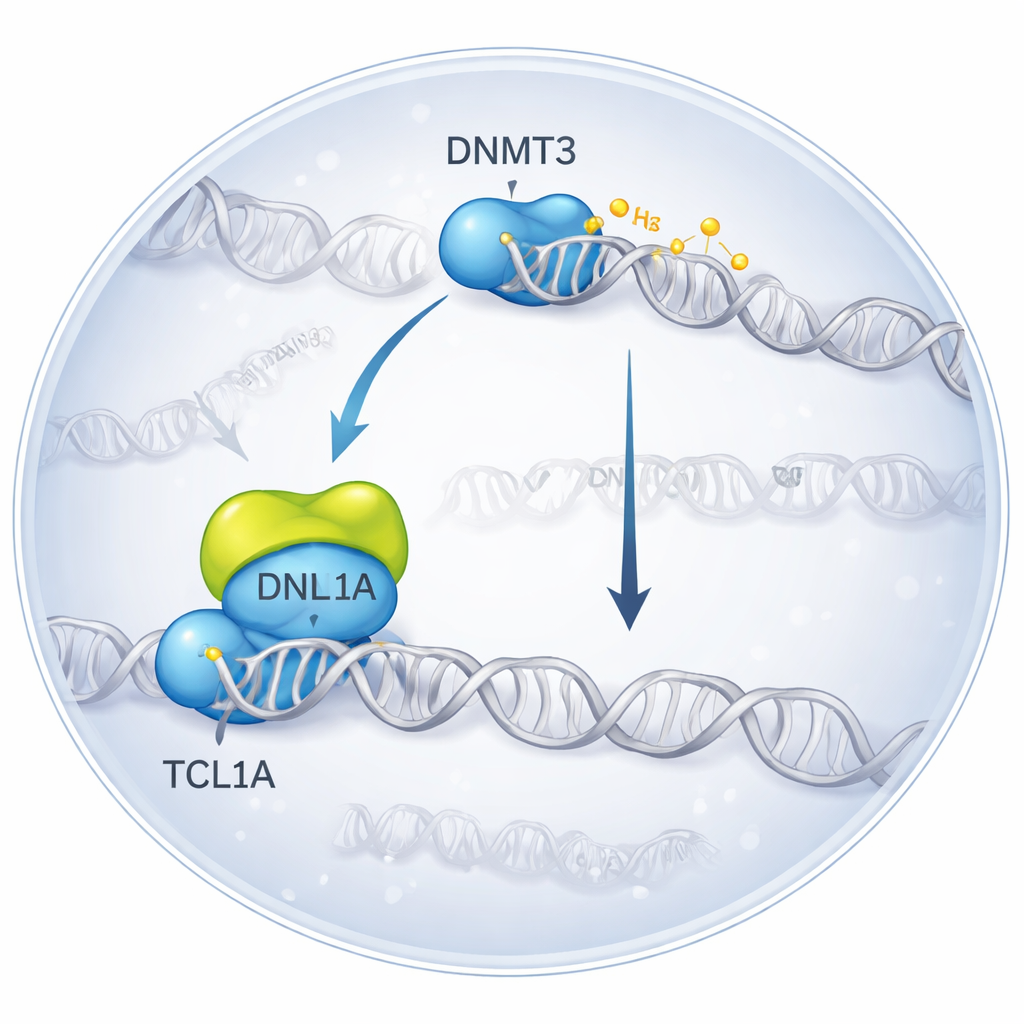
在三维中“冻结”一次分子相遇
研究人员使用冷冻电镜(一种对闪冻分子成像的技术)来可视化DNMT3A与TCL1A结合时形成的复合体。他们发现两分子DNMT3A配对形成二聚体,并且在每一侧都有一个TCL1A二聚体停靠到DNMT3A的催化区域——正是通常与辅助蛋白和DNA相互作用的部位。这个结合面与另一个伙伴DNMT3L通常附着以增强DNMT3A活性的位点重叠。在生化测试中,加入TCL1A显著降低了DNMT3A和DNMT3B的甲基化DNA能力,即便在存在DNMT3L的情况下也如此,证实了该结构复合体对应着一种高度抑制的状态。
一种使酶失灵的构象变化
进一步观察发现,TCL1A的结合并非简单像盖子那样覆盖活性位点。相反,它触发了DNMT3A构象上的细微但广泛的变化。酶的两个柔性区—靶识别环和催化环—远离它们在DNMT3A与DNA结合时占据的位置。在活跃形式中,这些环紧贴DNA并形成供小分子燃料SAM(供甲基的分子)的口袋。而在TCL1A附着时,催化环折入了SAM口袋并将其阻塞,同时也使DNA更难接近酶。结合测量证实,与TCL1A配对的DNMT3A已无法明显结合DNA或SAM。
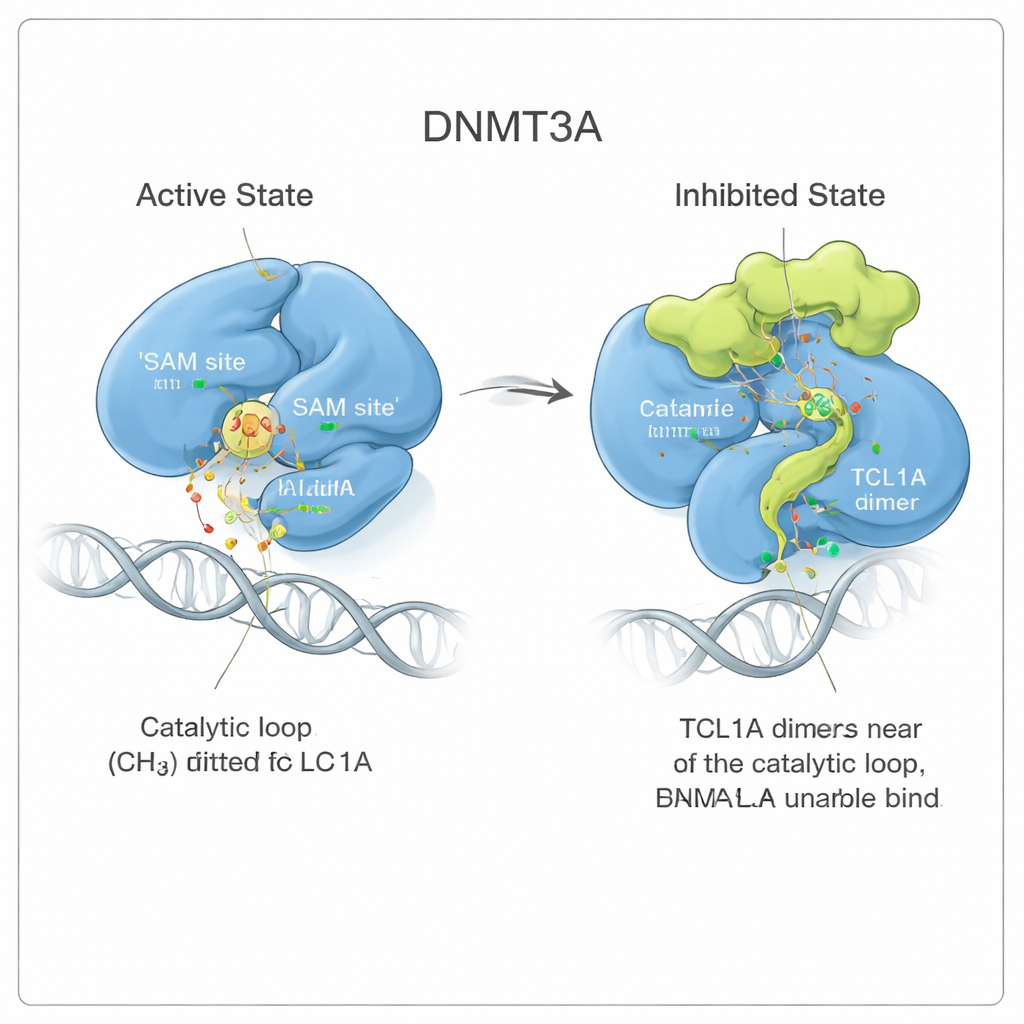
观察动态堵塞的运动
为了解这种被抑制构象的稳定性,作者进行了长时间的分子动力学模拟,基本上是分子在溶液中基于物理的“电影”。当DNMT3A与其激活子DNMT3L结合时,催化环保持在其活性位置。存在TCL1A时,该环变得更加可动,摇摆不定但反复占据SAM口袋,像海藻旋转却仍然堵住排水口那样。这种不断的运动将SAM可用空间缩小了十倍以上,支持这样一种模型:TCL1A利用DNMT3A的自然柔性以施加一种动态(而非刚性的)抑制形式。
对发育细胞与疾病的影响
研究团队接着探究这种分子阻断对真实细胞意味着什么。他们在小鼠胚胎干细胞中工程化表达人类TCL1A,恰逢细胞在分化起始阶段通常会增加DNA甲基化的时期。全基因组甲基化图谱显示,过表达TCL1A的细胞未能获得通常的高水平DNA甲基化,表现与同时敲除Dnmt3a和Dnmt3b基因的细胞高度相似。一个与DNMT3酶结合能力较差的TCL1A突变体几乎没有影响,这强调了物理相互作用的重要性。这些发现将结构机制与全基因组水平的表观遗传变化联系了起来。
对健康的意义
综上所述,这项工作揭示了TCL1A如何作为对置入新DNA甲基标记的酶的强有力刹车。通过停靠在关键界面,TCL1A重新定位了DNMT3A和DNMT3B的柔性环,使它们无法再结合DNA模板或化学燃料,从而导致细胞中甲基标记的全球丧失。在正常发育中,这种精细调控可能有助于平衡甲基化何时何地被添加。当TCL1A位置错误或过度表达(如某些血液肿瘤和罕见生殖疾病中)时,同一机制可使细胞的表观遗传程序脱轨。以原子分辨率理解这一相互作用为设计模拟或拮抗TCL1A作用的分子打开了大门,或可望恢复健康的DNA甲基化模式。
引用: Liu, Q., Li, J., Wang, X. et al. Molecular basis for the inhibition of de novo DNA methylation by TCL1A. Nat Commun 17, 2159 (2026). https://doi.org/10.1038/s41467-025-67710-8
关键词: DNA甲基化, DNMT3A, TCL1A, 表观遗传学, 癌症