Clear Sky Science · zh
蛋白质X射线晶体学的样品递送方法示例,重点关注样品消耗
观察分子在起作用
X射线晶体学让科学家看到蛋白质中原子的排列——这些驱动生命的微小机器。一个较新的方法,称为串行晶体学,进一步推进:它可以捕捉蛋白质作用的“分子电影”,例如酶处理药物或光合蛋白分解水的过程。但这有一个问题。许多重要蛋白质难以制备和结晶,现有实验可能消耗毫克到克量级的宝贵物质。本文综述提出了一个看似简单的问题:如何将晶体递送到强烈的X射线束中,同时尽量减少样品浪费?
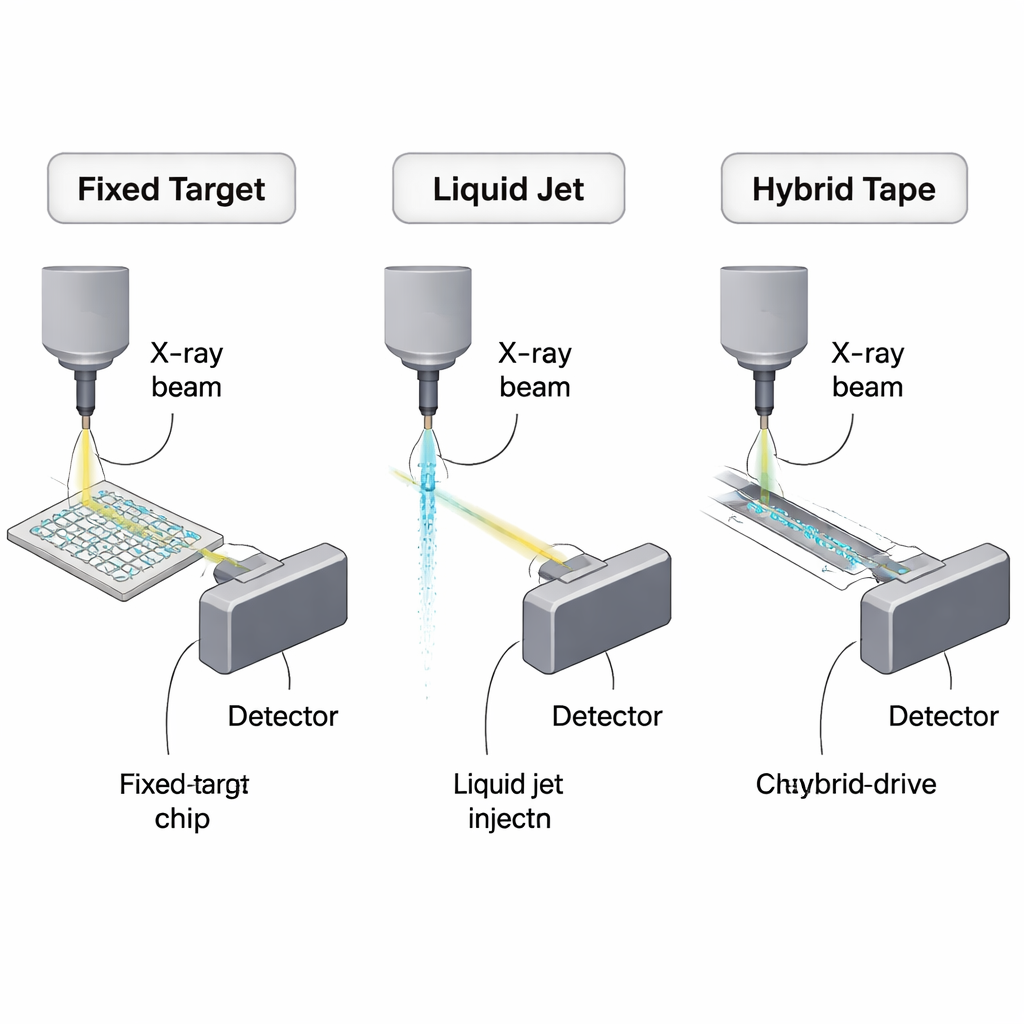
为什么串行晶体学需要更好的递送方式
传统晶体学依赖单个大晶体在X射线束中旋转。串行晶体学则颠覆了这一模式:不是一个大晶体,而是成千上万的微晶体,每个仅使用一次,被同步辐射或X射线自由电子激光(XFEL)发出的超亮X射线脉冲射入或扫描过去。这使得常温数据采集和化学反应的快速“快照”成为可能,但也意味着必须以与X射线脉冲列匹配的速率不断补充晶体,脉冲频率可高达每秒数百万次。大部分晶体悬浮液根本没有与光束相遇就被丢弃,因此减少样品消耗已成为该领域的核心技术和经济挑战。
固定靶:将每一滴样品都拉伸到极致的小芯片
一种主要策略是将微晶体固定在称为固定靶的小固体支撑物上。研究人员将晶体排列在硅或聚合物芯片的阵列上,并移动芯片使每个晶体只被带到X射线焦点一次,而不是将晶体喷过光束。在最理想的思想实验中,约10,000个模型蛋白的微晶体理论上可用仅约450纳克的蛋白质产生完整数据集。实际设备尚未达到如此节约,但它们已将需求降低到几十微克到几百微克——比早期串行实验好几个数量级。综述比较了硅网格、超薄聚合物薄膜和多层塑料芯片,权衡其优点(低背景散射、芯片上晶体生长、与常温研究的兼容性)与实际问题,如脱水、芯片材料的杂散散射以及人工移液引入的额外“死体积”。
液体喷射与高粘流:速度快但耗料多
另一类方法保持晶体悬浮于液体中,并连续将其输送穿过光束。气动虚拟喷嘴可生成毛发般细的射流,能够跟上快速的XFEL脉冲列,是时间分辨研究和在曝光前通过快速混合触发反应的混合注射实验的主力工具。然而,由于喷射是连续进行的,大部分射流从未遇到X射线脉冲。即使经过精细调节,实际实验消耗的蛋白质仍远高于理论最小值——通常是几十到数百微升的浓缩晶体浆液。为缓解这一点,研究者开发了更高效的设计,例如用牺牲液体包裹晶体射流的双流喷嘴、在更低流速下工作的电纺“ MESH”注射器,以及以凝胶或脂质立方相中嵌入晶体并以微升/分钟或更慢速率推送的高粘度挤出器。这些高粘方法对脆弱的膜蛋白以及在同步辐射下的常温研究尤其有价值,但其较厚的射流会增加背景散射,并不太适合最快速的X射线光源。
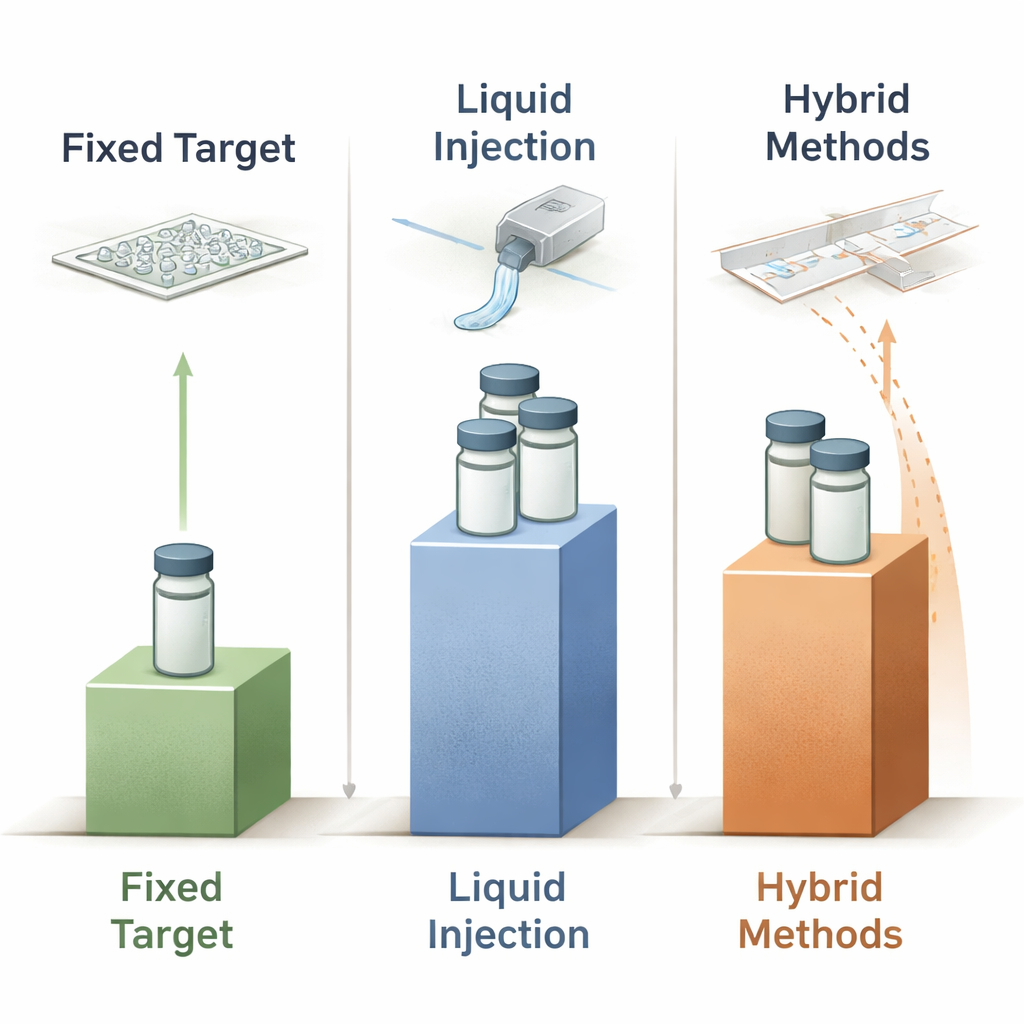
液滴、胶带与混合方案:逐脉冲匹配
第三类日益创新的“混合”方法将固体支撑与受控液体或液滴递送结合。胶带驱动系统例如将液滴或细液条沉积到通过光束移动的聚合物薄膜上;通过定时运动可以在预定延迟下探测反应步骤或气体暴露。按需滴射系统更进一步,使用声学或压电装置仅在预期有X射线脉冲时喷出纳升甚至皮升液滴,从而大幅减少浪费。一些设计在胶带上将配体液滴混入预先放置的含晶体液滴中,恰在其到达光束前进行混合,使得用量受限的时间分辨酶学成为可能。其他混合方案,如LAMA芯片法,则将微量底物直接滴加到预先装载在固定靶芯片上的晶体上。各类设计报告的蛋白质使用量范围很广——从接近毫克级到数毫克用于完整的时间分辨系列——既展示了节省潜力,也反映了同步液滴、晶体与X射线脉冲时的工程挑战。
我们离理论最小值有多近?
通过比较数十项发表的固定靶、液体注射器和混合系统实验,作者表明目前没有任何方法接近理想的450纳克基准;即使是最好的设备仍大约超出两个数量级。然而,可以看到明确的趋势。固定靶通常使用最少的蛋白质,并在时间分辨混合非必须或可在芯片上实现时非常有吸引力。液体喷射仍主导最苛刻的时间分辨XFEL研究,但仍然消耗大量样品,特别是在需要许多时间点时。混合液滴与胶带方案在相对节省方面表现突出,尤其是在液滴定时与X射线源紧密同步时。展望未来,文章认为进一步进展将来自更好的微流控控制、消除浪费操作步骤的自动化,以及利用紧凑X射线源和数据驱动的优化来协同设计实验与递送系统,从而使蛋白质使用量更接近理论极限。
引用: Manna, A., Doppler, D., Sripati, M.P. et al. Sample delivery methods for protein X-ray crystallography with a special focus on sample consumption. Nat Commun 16, 9856 (2025). https://doi.org/10.1038/s41467-025-65173-5
关键词: 串行晶体学, 蛋白质X射线晶体学, 样品递送, X射线自由电子激光, 微流控