Clear Sky Science · zh
减少 RAD23A 可延长寿命并减轻小鼠 TDP-43 蛋白病模型的病理
这项研究对家庭与患者为何重要
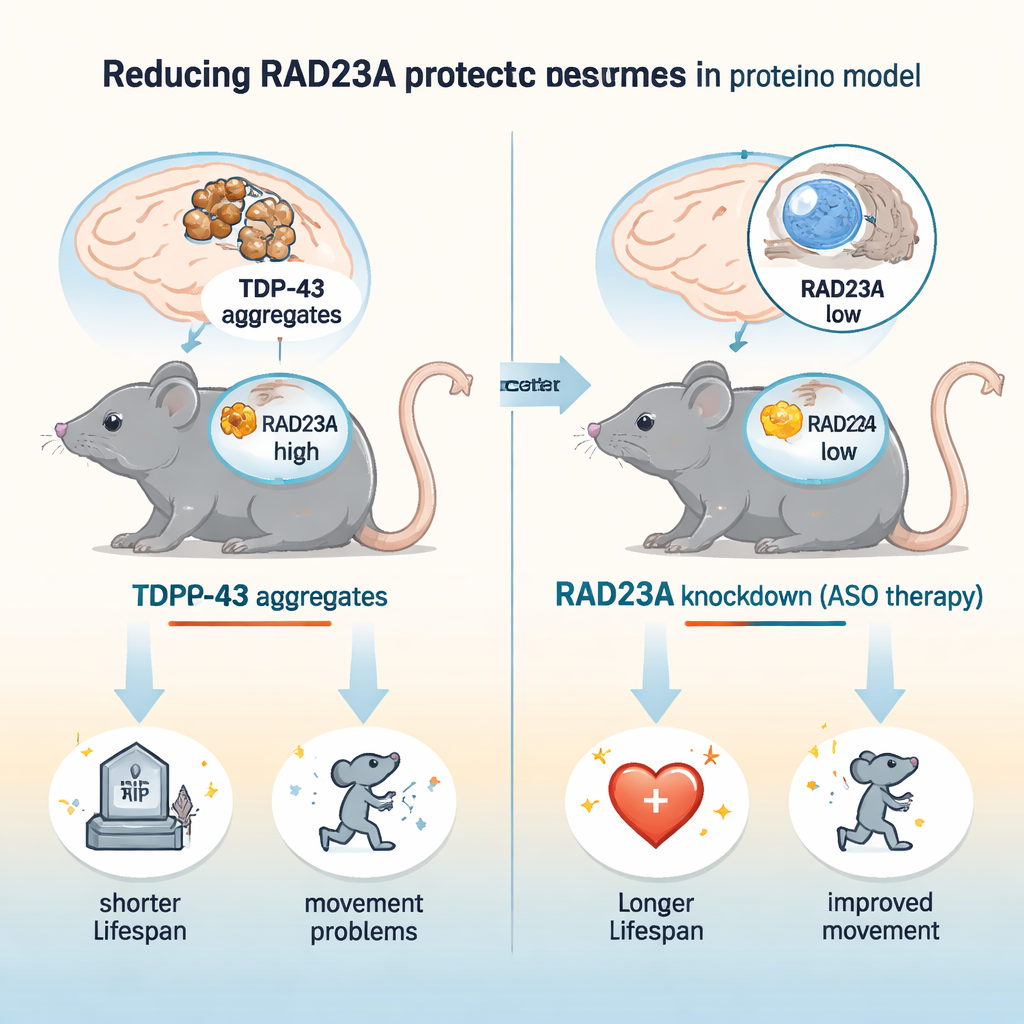
许多形式的痴呆和运动神经元疾病,包括肌萎缩侧索硬化症(ALS)和额颞叶痴呆(FTD),都涉及脑细胞内蛋白质错误折叠、聚集并逐渐毒害神经元。其中一个主要罪魁祸首是称为 TDP-43 的蛋白,它在正常情况下参与 RNA 调控,但在聚集时会变得有毒。这项研究提出了一个充满希望的问题:我们能否通过降低另一个参与受损蛋白处理的蛋白 RAD23A,让脑细胞更具抗逆性?作者在小鼠中证明,降低 RAD23A 可以延长寿命、改善运动功能并减轻 TDP-43 驱动疾病模型的脑损伤,提示了一种新的治疗策略。
病变神经元中的蛋白质交通堵塞
神经退行性疾病常以错误折叠蛋白堆积为特征,而细胞的清除机制未能将其清除。在 ALS 和 FTD 中,TDP-43 从细胞核移出,形成黏性的团块,并被大量标记上泛素——这种标记通常将蛋白引导到细胞的主要降解机器蛋白酶体。RAD23A 是几种可以把被泛素标记的货物运送到蛋白酶体的“穿梭”蛋白之一。然而先前在线虫和培养神经元中的工作表明,失去 RAD23 类蛋白反而可能保护免受 TDP-43 诱导的损伤——这是一个悖论,本研究旨在在哺乳动物大脑中进一步探索这一现象。
在 TDP-43 小鼠模型中降低 RAD23A
研究人员使用了一个成熟的小鼠模型,称为 TAR4/4,该模型在神经元中过度表达人源 TDP-43,并出现运动障碍、脊柱弯曲、震颤和早亡,反映了 ALS/FTD 的关键特征。他们用两种方式降低 RAD23A:向新生小鼠注射可减少 Rad23a RNA 的反义寡核苷酸(ASO),以及繁殖携带 Rad23a 基因敲除的小鼠。一次 ASO 治疗将脑和脊髓中的 RAD23A 水平降低约四分之三。在这些 TDP-43 小鼠中,RAD23A 敲低使寿命延长约 50%,并延缓步态异常、震颤、脊柱弯曲和后肢抱夹的发生及严重程度。有趣的是,完全的基因缺失并未带来额外益处,表明部分降低可能是最佳选择,而长期完全缺失可能引发代偿性变化。
炎症减少、更清洁的蛋白处理与更平静的基因组
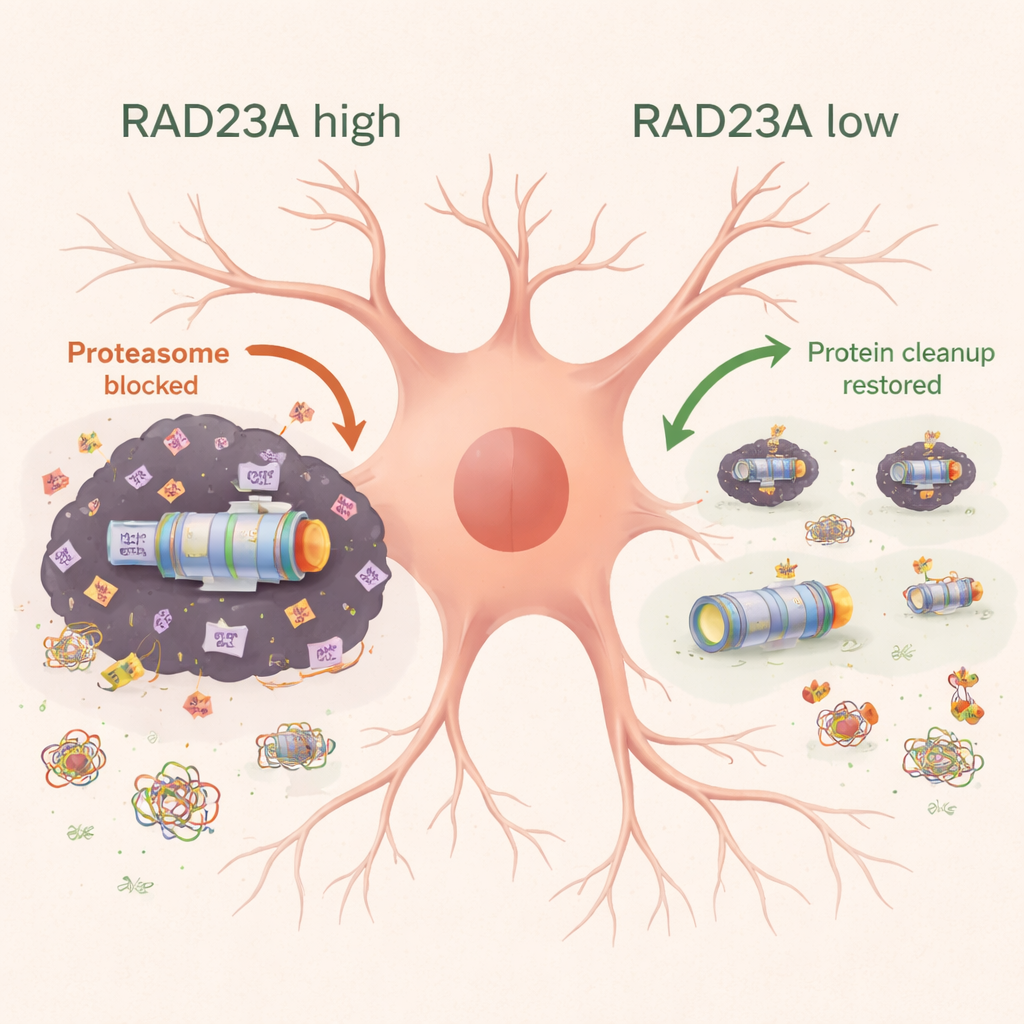
对运动皮层的显微检查表明,TDP-43 小鼠出现神经元丧失,并伴随星形胶质细胞和小胶质细胞(脑内的支持和免疫细胞)强烈活化。降低 RAD23A 保留了更多神经元并减少了炎症和细胞死亡的标志物。生化分析显示,过度表达 TDP-43 使细胞充斥着被泛素标记的去离子洗涤剂不溶性蛋白,并将蛋白酶体亚基拖入这些聚集体中,削弱了细胞清除受损蛋白的能力。降低 RAD23A 降低了泛素化蛋白的总体负荷,使更多蛋白酶体保持在可溶的、可工作状态,并将若干类型的蛋白酶体活性恢复到接近正常。与此同时,RAD23A 敲低减少了 TDP-43 的总量和聚集形式,包括一种特别有毒的 25 千道尔顿片段,并将 TDP-43 从胞质向细胞核重新定位。全基因组 RNA 测序显示,TDP-43 触发的成千上万的基因表达变化在降低 RAD23A 后部分逆转,尤其是与神经元功能、线粒体能量产生和清除聚集体的通路(如聚集自噬)相关的基因。
重塑隐性“不可溶”蛋白组
为更仔细地观察那些抵抗常规洗涤剂的顽固聚集体,团队使用重同位素质谱法对小鼠皮层不可溶部分中被困的蛋白进行了目录式分析。人源 TDP-43 的表达吸引了蛋白酶体组分、细胞骨架与运输蛋白以及其他细胞机械装置。当 RAD23A 被敲低时,这个不可溶蛋白组的总体组成发生了变化:被隔离的蛋白酶体和运输相关蛋白减少,而一些核糖体与应激相关蛋白在聚集中增加。值得注意的是,这种重塑并不简简单单反映 RNA 水平的变化,表明 RAD23A 主要影响已有蛋白如何在可溶与聚集状态之间分配,而不是决定每种蛋白的生成量。
这对未来疗法可能意味着什么
总体而言,这些发现将 RAD23A 描绘为在受压神经元中强有力的蛋白质质量控制调节因子。通过在 TDP-43 驱动的小鼠模型中部分降低 RAD23A,作者得以减少有毒蛋白聚块、恢复蛋白清除机械的活性、平息有害的基因表达改变、限制脑内炎症并延长寿命与运动功能。鉴于异常的 TDP-43 积累在遗传性与散发性 ALS、FTD 及相关疾病中普遍存在,用适合人类的反义药物靶向 RAD23A 可能提供一种无需直接阻断 TDP-43(这是一种必需蛋白)即可保护神经元的方法。尽管还需在其他模型与人体中进行大量验证,这项工作将 RAD23A 确认为对抗神经退行性病变的一个有希望的新切入点。
引用: Guo, X., Prajapati, R.S., Chun, J. et al. Reduction of RAD23A extends lifespan and mitigates pathology in a mouse model of TDP-43 proteinopathy. Nat Commun 17, 1820 (2026). https://doi.org/10.1038/s41467-025-65104-4
关键词: TDP-43, ALS, 蛋白聚集, 蛋白酶体, 反义疗法