Clear Sky Science · zh
甲醛固定石蜡包埋组织样本的光学超分辨组织学:挑战与机遇
在存储的组织样本中看得更清楚
世界各地的医院将患者器官的薄片保存在石蜡块中,以便像癌症或肾损伤这样的疾病能够被长期研究。本文综述说明了新型光学显微镜如何将这些常规样本转变为观察疾病的强大窗口,揭示标准医院显微镜无法看见的极小细节。这些进展可能帮助医生更早发现疾病、理解其进展并更精确地定制治疗方案。
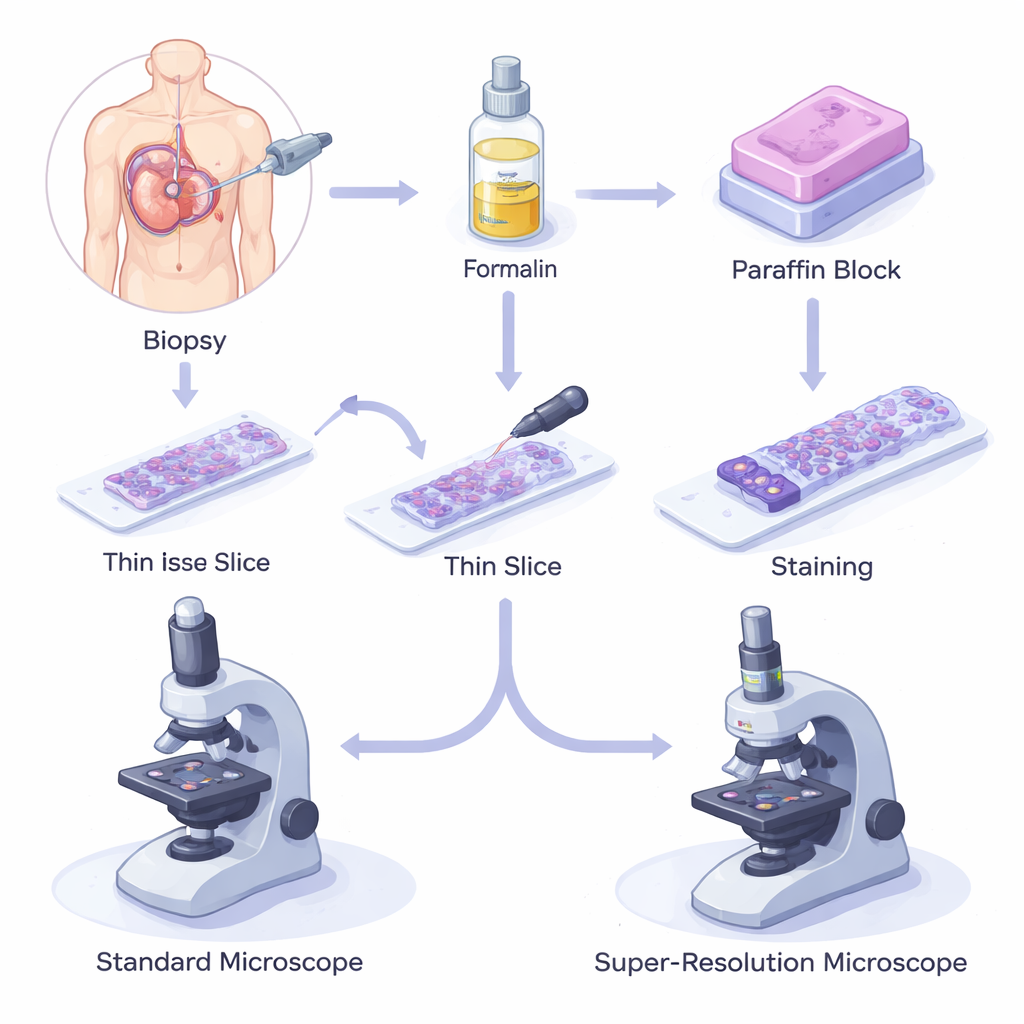
石蜡保存的组织如何支撑现代医学
在活检过程中,会取下一小块组织,用称为甲醛的化学物质固定以防止腐败,然后包埋在石蜡中。石蜡块被切成头发般薄的切片,置于玻片上、染色并在光学显微镜下检查。这种甲醛固定石蜡包埋(FFPE)方法成本低、可靠,并能在室温下保存样本数十年。因此,全球生物样本库中存储着数以百万计的 FFPE 样本,支持从基础生物学到先进的基因和蛋白研究,并构成现代诊断与预后的支柱。
为什么普通显微镜已经不够用
传统光学显微镜受限于光学物理:小于约250纳米的细节会模糊在一起。许多与疾病相关的结构——如肾脏的精细滤器、神经细胞之间的连接,或细胞核内 DNA 架构的微小变化——都低于这一极限。如今的工作流程通常将标准光学显微镜用于宏观概览,再辅以电子显微镜观察纳米级细节,但这种方法速度慢、成本高,并且需要完全不同的样本制备。因此,临床医生和研究人员正在寻求一种单一、灵活的系统,既能快速扫描大面积,又能在同一 FFPE 切片中放大观察纳米尺度的特征。
让视野更清晰的新方法
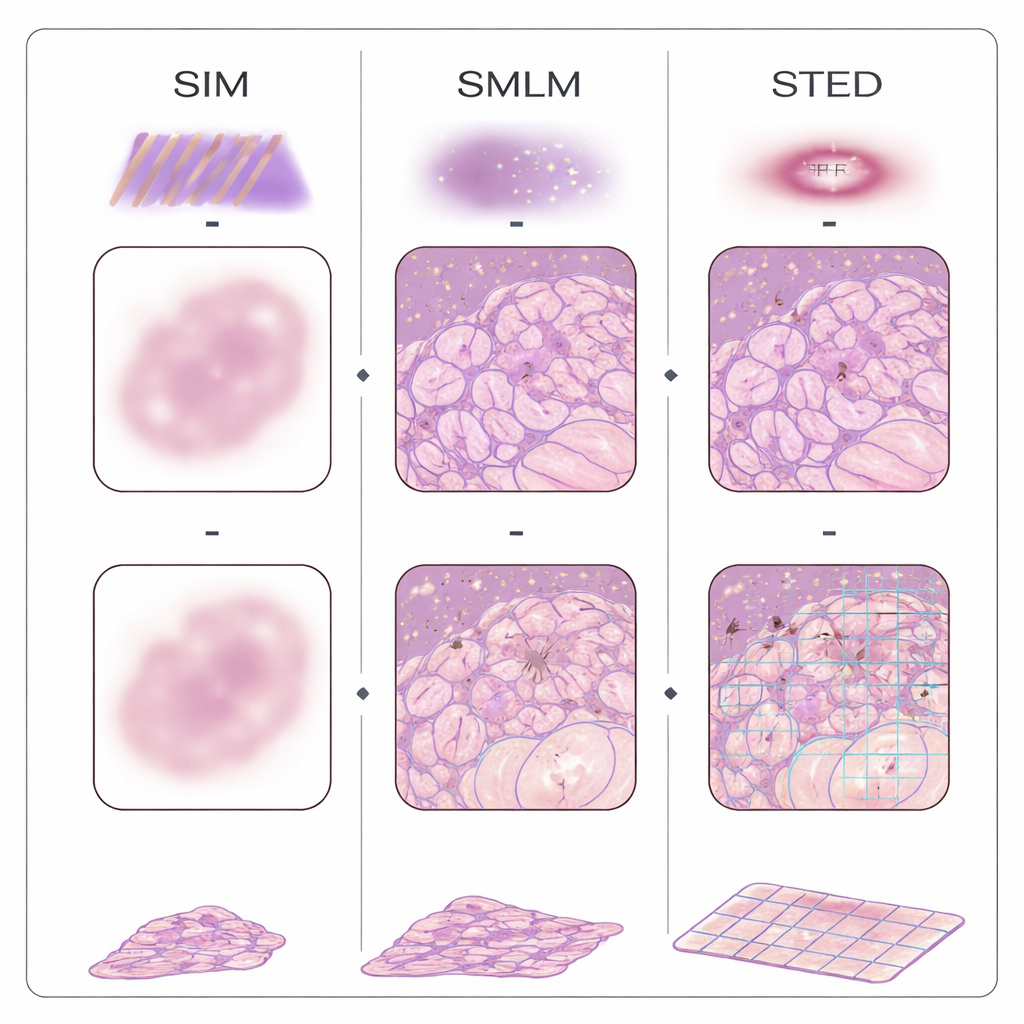
过去二十年间,几类“超分辨”显微镜利用荧光标记和巧妙的光学设计打破了传统分辨率极限。单分子定位方法通过开关分子并逐一定位其位置;结构化照明显示将条纹光投射到组织上并通过计算恢复更细的细节;受激发射耗尽(STED)用甜甜圈形的光束雕刻出一个微小的发光点;基于波动的方法分析图像中的细微闪烁以推断结构。另一种策略,称为扩增显微术,通过将组织在凝胶中物理膨胀来避免复杂光学,使普通显微镜能够看到先前不可见的细节。这些方法已被应用于来自乳腺、结肠、胰腺、肾脏、脑、皮肤、胎盘等器官的 FFPE 样本,揭示肿瘤中线粒体的变化、肾小球滤器的失效以及阿尔茨海默病中蛋白质聚集的形成等现象。
走向日常应用的障碍
尽管前景可期,但这些技术尚未准备好成为大多数病理实验室的常规工具。许多超分辨系统速度慢、视野狭小,或需要数万张图像来构建一幅高细节图,这在病理学家需要评估大面积组织时并不现实。FFPE 组织本身在光学上具有挑战性:它们会散射光、产生自发荧光,并可能掩盖需要标记的分子,所有这些都会导致图像模糊或产生伪结构。有些方法还要求特殊染料、定制缓冲液或多步化学处理,这些都难以融入标准组织学流程。此外,商业仪器昂贵且操作复杂,所得数据也需要大量计算处理与存储。
把智能光学与智能软件结合起来
为克服这些障碍,研究人员正在将改进的光学技术与无标记成像和人工智能结合。高通量、衍射极限的方法,如傅里叶衍射层析(Fourier ptychography)和非线性光学显微镜,能够快速扫描大面积甚至未染色的 FFPE 切片,并提供组织结构的定量图谱。数字病理平台现在可以高分辨率地捕获整张玻片,并使用机器学习检测肿瘤和评估诸如 HER2、Ki‑67 与 PD‑L1 等生物标志物的评分。深度学习模型甚至可以将低分辨率图像转换为超分辨视图,可能减少对某些专用硬件的需求,同时更好地利用现有的活检档案。
这对未来患者意味着什么
作者总结认为,真正的 FFPE “超分辨组织学”——将纳米尺度细节、高速度、合理成本与与现有实验室流程的兼容性结合起来——尚未完全实现,但已触手可及。随着光学方法变得更快、更稳健,以及基于 AI 的分析日趋成熟,这些工具有望揭示当前被忽视的组织微小早期改变,提高诊断准确性,并指导更个性化的治疗决策。从长远看,将每一个存档的石蜡块转变为疾病的高清地图,可能会改变研究和临床护理两方面的面貌。
引用: Villegas-Hernández, L.E., Dubey, V.K., Acharya, G. et al. Optical super-resolution histology of formalin-fixed paraffin-embedded tissue samples: challenges and opportunities. Nat Commun 16, 9760 (2025). https://doi.org/10.1038/s41467-025-64626-1
关键词: 超分辨显微镜, FFPE 组织, 数字病理, 光学成像, 癌症诊断