Clear Sky Science · zh
用于现场检测的纳米孔蛋白质和肽构象传感
为什么微小的蛋白形态可能改变你的下一次体检
随着人口老龄化,阿尔茨海默病、帕金森病、心脏病和癌症等疾病越来越常见。许多此类疾病在症状出现之前很长一段时间就始于关键蛋白和小肽(peptide)微小的构象变化。当前的临床检测通常测量生物标志物的含量,而不是其形态是否正常或发生了异常。本文探讨了一种称为纳米孔传感的技术,它能够通过电学方式“感知”单个蛋白分子的形状与化学特征,并论证该技术有望成为未来可在小型设备上分钟级完成的现场检测方法的基础。
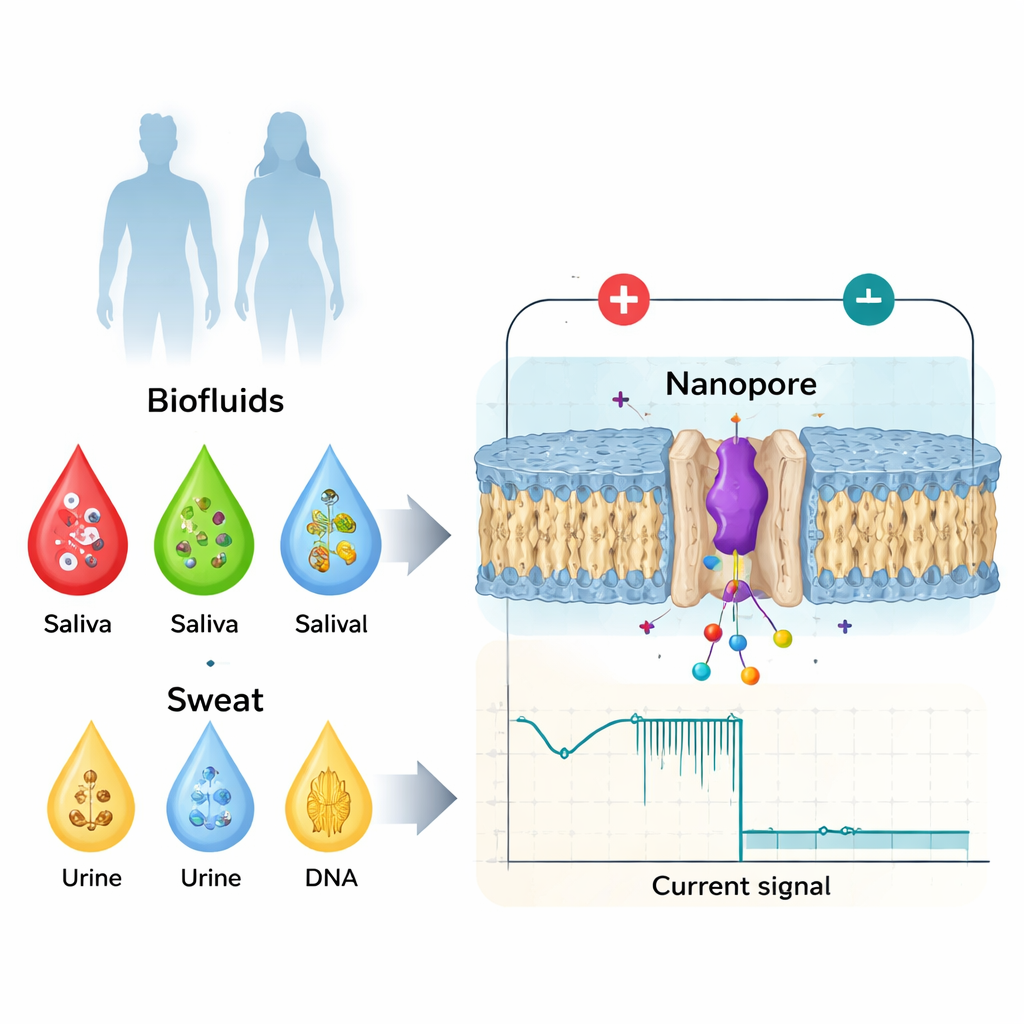
从简单血检到对形态敏感的生物标志物
医生已经利用来自血液、唾液、尿液或汗液的多种生物标志物(如蛋白质、激素或小分子)来监测健康与疾病。传统上,关注点在于总体变化:蛋白数量增多、DNA 损伤或病原体成分的存在。但生物学更为微妙:相同的蛋白可以通过结构的细微变化、合成后添加的化学标签,或其构建单元的镜像异构体而被开关调节。这些小变化会影响蛋白与配体的结合、聚集或信号传递方式,并与血栓形成问题、神经退行性疾病和癌症相关。质谱、抗体检测和高分辨成像等医院常用工具功能强大,但代价高、速度慢、需要高技能人员,而且通常难以作为快速、简单的现场检测设备部署。
纳米孔怎样与众不同
纳米孔传感将问题颠倒过来。它不对数万亿分子取平均,而是逐个分子地在通过一张仅数十亿分之一米宽的小孔时进行检测。施加电压使离子通过孔流动并产生稳定电流。当蛋白或肽进入孔内时,会部分阻断该电流。电流下降的幅度、持续时间以及细微形状取决于分子的体积、电荷和构象(三维折叠)。通过精心设计孔结构——使用工程化蛋白或固态材料——研究者可以将单个生物分子限制足够长的时间,从而得到丰富的电学“指纹”,不仅能区分不同蛋白,还能识别同一生物标志物的细微变体。
逐分子读出与疾病相关的变化
综述强调了纳米孔已被用于解析其他方法难以识别的医学重要差异的实例。它们能区分相差一个氨基酸的肽片段,直接从血液中检测与疾病相关的血红蛋白变体,并分辨仅相差一个构建单元的短激素样肽,甚至区分该构建单元的镜像异构体。纳米孔还能感测翻译后修饰——如磷酸、糖基或硫酸等小化学基团——这些修饰决定了参与阿尔茨海默、帕金森、凝血或癌症的蛋白是正常还是病理性的。在某些实验中,单个酶或结合蛋白被固定在孔内,其电信号的变化实时揭示了其如何与配体结合或执行反应,可能揭示疾病中失调的通路。
迈向快速床旁检测
由于每次阻断事件对应单个分子,纳米孔设备可以非常灵敏,在复杂体系中检测到仅数千份生物标志物拷贝。作者讨论了实现临床应用的关键策略:提高稀有分子的捕获速率、稳定膜或采用固–生物杂化孔,以及使用机器学习自动将复杂电学模式分类为明确的诊断类别。他们还展示了间接方法(例如连接 DNA 标签或结合配体)如何放大微弱信号或允许同时测量多种生物标志物,同时仍保留赋予纳米孔独特性的许多构象细节。
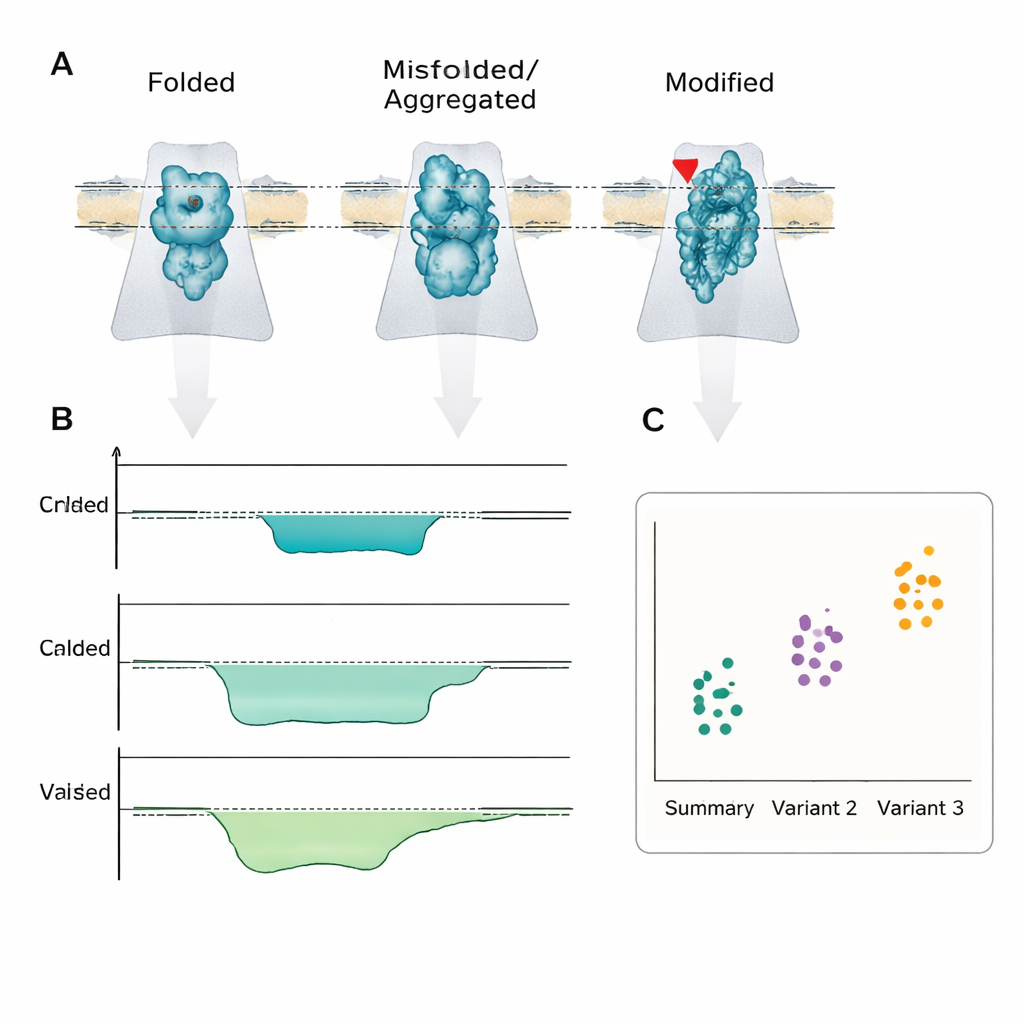
这对患者可能意味着什么
核心观点是,疾病往往与蛋白质的哪种形态或化学版本存在相关,而不是蛋白质的总量。纳米孔传感是少数能够在单分子水平直接读取这些差异的技术之一,其速度和简便性有望使其集成到便携设备中。尽管仍有重大工程和标准化挑战,但作者认为,正如纳米孔 DNA 测序仪已进入临床领域,纳米孔蛋白与肽传感器最终也可能提供快速的床旁检测,不仅能提示“有问题”,还能够揭示导致患者状况的确切分子折叠错误或修饰。
引用: Ratinho, L., Meyer, N., Greive, S. et al. Nanopore sensing of protein and peptide conformation for point-of-care applications. Nat Commun 16, 3211 (2025). https://doi.org/10.1038/s41467-025-58509-8
关键词: 纳米孔传感, 蛋白质生物标志物, 现场诊断, 翻译后修饰, 构象性疾病