Clear Sky Science · zh
内源性阿片受体与适应不良进食的盛宴或饥荒
为何我们的脑子会推动我们暴饮或几乎不吃
大多数人都曾在不同时间既强烈渴望油腻美食,又在压力下食欲不振。本文解释了大脑自身的阿片系统——与止痛和药物成瘾相关的那类化学物质——如何将进食行为推向危险的极端。通过考察肥胖和神经性厌食症,作者展示了相似的脑回路和化学信号如何产生相反的结果:慢性暴食或严重自我饥饿。

大脑的愉悦与疼痛化学物质
机体自然产生类似阿片的分子,如内啡肽、脑啡肽和强啡肽。这些化学物质作用于分布在大脑各处的阿片受体,尤以控制奖赏、动机、饥饿和疼痛的区域为重。当我们进食,尤其是美味的高热量食物时,这些系统会发出信号,使食物变得令人愉悦并减轻不适。在正常情况下,这有助于我们寻求足够的食物而不走极端。但当这些受体过度活跃、活性不足或连接方式不同,就可能扭曲食物的奖励感、我们对饥饿的主观感受以及对疼痛或压力的感知。
天然阿片如何助长暴食与肥胖
在肥胖中,大脑的奖赏回路似乎被重塑为类似成瘾药物引起的改变。位于被核(nucleus accumbens)的关键奖赏中枢中的阿片受体帮助驱动对富含脂肪和糖分的可口食物的寻求与享受。遗传学研究表明,μ-阿片受体基因的某些变体可能保护部分人群免于体重增加,而其他基因调控模式则与肥胖相关。啮齿动物实验显示,阻断阿片受体会降低甜高脂饮食的吸引力,而移除这些受体可使动物对饮食诱导性肥胖产生抵抗。同时,肥胖者常在奖赏系统中表现出较低的μ-阿片受体可利用性,但在下丘脑等感知饥饿与饱足的区域中显示较高水平,暗示大脑对食物的价值与调控在长期内发生了迁移。
相同系统何时支持自我饥饿
神经性厌食症虽然在表面上与肥胖相反,但同样涉及阿片信号的改变。遗传学研究反复指出δ-阿片受体基因为一项危险因素,脑成像显示处理奖赏、恐惧与厌恶的区域整体上阿片受体可利用性降低。长期存在的理论提出,在易感个体中,饥饿会触发一种自我强化的“快感”:节食和剧烈运动释放的天然阿片减轻压力并产生情绪缓解,促使进一步减重而非正常摄食。将食物限制与自愿跑动结合的动物模型显示出类似模式——过度活动、体重下降,以及阿片系统被推到如此高的基线以致外源性阿片失去影响的迹象。重要的是,在一些研究中阻断阿片受体似乎有助于厌食症患者恢复体重,并促使啮齿动物增加脂肪摄入,提示这可能是一条潜在的治疗途径。
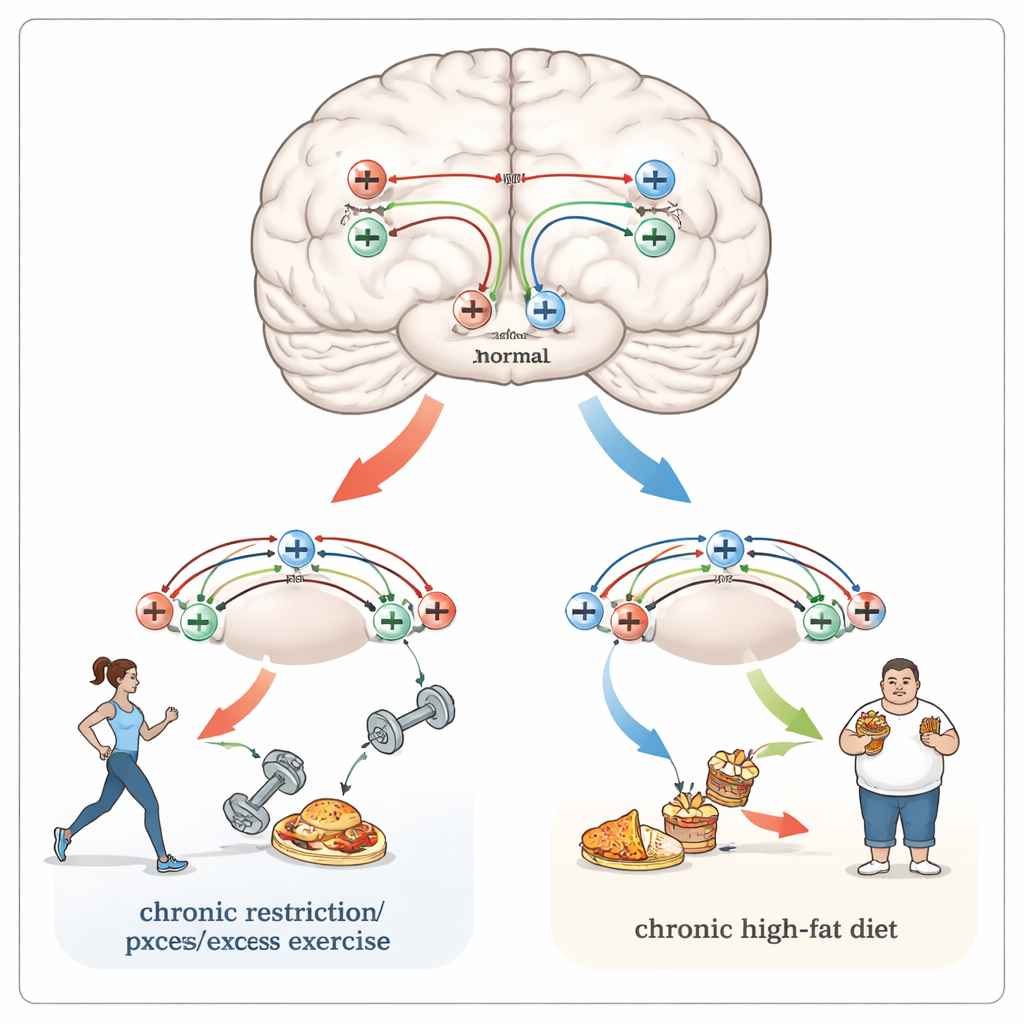
与疼痛、成瘾和刻板习惯的共同联系
塑造进食行为的相同脑区和受体也参与处理疼痛和药物奖赏。肥胖者往往经历更多疼痛,包括偏头痛,而长期厌食者常对疼痛刺激表现出迟钝反应。天然阿片在下丘脑、脑干和被核等区域的作用既能缓和疼痛,又能将注意力转向诸如饥饿等紧迫需求。这些回路与被成瘾药物重塑的通路重叠,长期食物限制已知会在动物研究中增敏对阿片类等物质的反应。肥胖和厌食还都与认知灵活性下降有关——即将习惯适应新情境的能力减弱——这可能反映了由阿片受体部分驱动的神经元连接层面更深、更持久的变化。
这对理解和治疗极端饮食意味着什么
综上所述,证据表明大脑自身的阿片系统有助于决定进食变化(如接触高热量食物或节食时期)是保持短暂且适应性的,还是螺旋式陷入长期有害的模式。在肥胖中,反复暴食似乎重塑了奖赏与饥饿回路,使高热量食物变得尤其具有诱惑力。在厌食中,饥饿和过度运动可能劫持相同的阿片驱动学习过程,使自我克制和过度活动在尽管体重危险下降的情况下仍被感受为有奖励。作者认为,通过定位这些受体何处以及如何发生改变,未来研究或可引导更精确的治疗——例如有针对性的受体阻断、脑刺激或恢复突触可塑性的药物——以将大脑的“盛宴或饥荒”回路重新拉回平衡。
引用: Sutton Hickey, A.K., Matikainen-Ankney, B.A. Endogenous opioid receptors and the feast or famine of maladaptive feeding. Nat Commun 16, 2270 (2025). https://doi.org/10.1038/s41467-025-57515-0
关键词: 内源性阿片类物质, 饮食失调, 肥胖, 神经性厌食症, 大脑奖赏回路