Clear Sky Science · zh
照亮氨基端乙酰化的影响:从蛋白质到生理学
小小化学标签如何改变蛋白质行为
你体内的每个细胞都充斥着必须正确折叠、前往正确位置、组装成分子机器并在受损时被清除的蛋白质。这篇综述探讨了一种发生在许多蛋白质一端的微妙但极为常见的化学变化——称为氨基端乙酰化——并展示了这种小小的“帽”如何帮助控制从细胞生长和应激反应到心脏发育与大脑功能的各种过程。
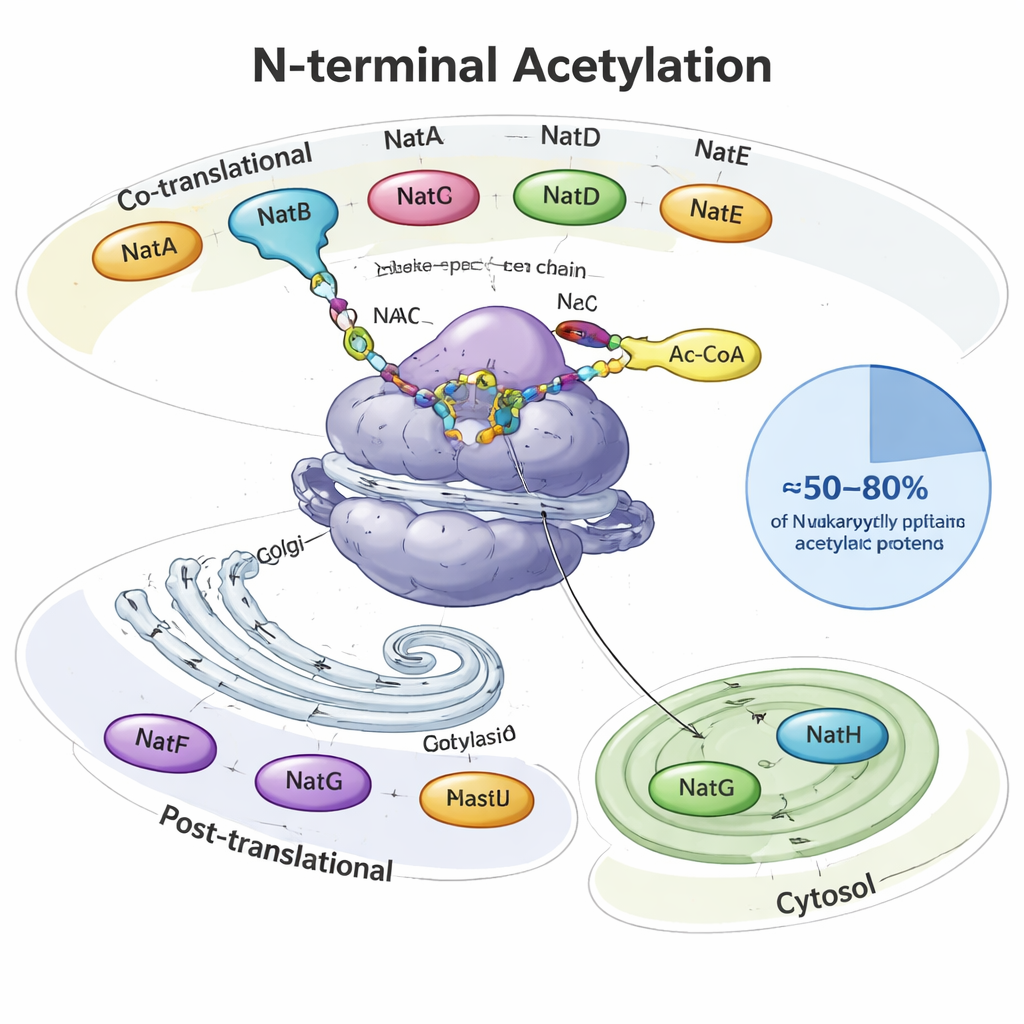
我们大多数人从未听说过的蛋白质帽
当蛋白质合成时,它像一根生长的线一样从细胞的蛋白质工厂——核糖体中伸出。在它的最前端——氨基端,许多真核蛋白会接受一个乙酰基,这是一个由两个碳构成的小帽。专门的酶称为氨基端乙酰转移酶(NATs)执行这一工作,以常见的代谢分子(乙酰辅酶A)作为供体。在酵母、植物和动物中,八种主要的NAT类型(NatA–NatH)分工合作。有些在蛋白质合成过程中就起作用,另一些在之后工作并驻留在特定位置,如高尔基体或植物质体。它们共同修饰了约一半到四分之五的细胞蛋白,每种NAT识别两到四个氨基酸组成的首端偏好序列。
多种酶,各有专长
NatA、NatB和NatC是主要执行者,它们直接在核糖体上作用,覆盖了大范围的“氨基端乙酰组”。单是NatA就能修饰约40%的人人类蛋白,通常是其首位甲硫氨酸被截去的那些蛋白。NatB和NatC作用于保留初始甲硫氨酸的蛋白,但在其邻近氨基酸的偏好上有所不同。其他NAT则更具选择性:NatD专注于少数包装DNA的组蛋白,NatF针对位于高尔基体的跨膜蛋白,NatG在植物质体内工作,而NatH(NAA80)在肌动蛋白这一细胞骨架重要成分上完成一个特殊的两步成熟过程。文章整合了结构学和生化研究,展示了助手亚基如何将这些酶锚定到核糖体或膜上并微调它们的底物选择性。
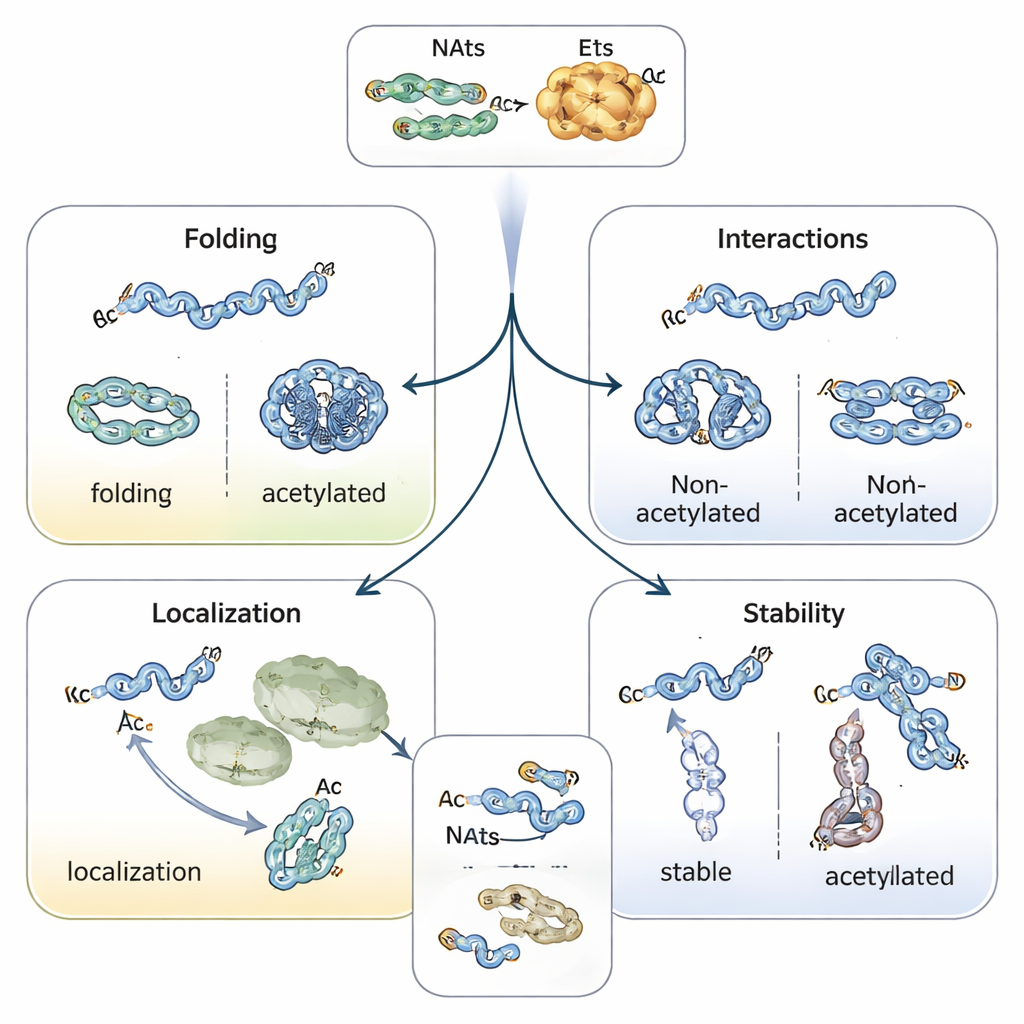
引导蛋白折叠、定位与寿命
添加乙酰帽会改变蛋白前端的化学性质,常常稳定螺旋结构并影响蛋白的折叠。例如,与帕金森病相关的α-突触核蛋白在其氨基端被乙酰化时更不易聚集并采取更安全的构象。与肌动蛋白相互作用的调节蛋白热赖蛋白(tropomyosin)在正确乙酰化时对肌动蛋白丝的结合与调控能力显著增强。在植物和动物中,氨基端乙酰化也可作为一种地址标签,帮助蛋白找到叶绿体、溶酶体或高尔基体。也许最引人注目的是它在决定蛋白存活时间方面的作用:未被保护的氨基端可能被泛素标记酶识别为“降解信号”,而乙酰化可以掩盖该信号从而稳定蛋白——或者在某些情况下,产生只有在蛋白错误折叠或未进入正确复合体时才被识别的条件性标签。
从细胞生理到发育与疾病
因为氨基端乙酰化影响众多蛋白,破坏NATs会对整个生物体产生广泛影响。在模式生物中去除NatA、NatB或NatC常导致严重的发育缺陷、应激反应改变甚至致死,而更专一的酶如NatF和NatH则产生更有限的问题,如脑部钙化或听力损失。在人类中,若干NAT基因的遗传突变导致罕见的神经发育综合征,伴有智力障碍、心脏缺陷或肌无力。同一套机器在癌症中常表现为过度活跃,NAT水平升高与预后不良相关,可能驱动肿瘤生长、转移和对治疗的抵抗。氨基端乙酰化的变化也影响易聚集的蛋白,如α-突触核蛋白和亨廷顿蛋白,将这一修饰与神经退行性疾病的机制联系起来。
未来方向与医学前景
作者总结道,尽管我们现在已知大多数添加这些氨基端帽的核心酶,但对具体蛋白靶点和调控规则的理解仍十分有限。一个主要主题是,蛋白前端的乙酰化常常将其从过早降解中保护出来,同时又为质量控制创造情境依赖的信号。确切识别哪些泛素连接酶识别哪些氨基端模式,以及是否存在能够去除这些帽的酶,仍是关键未决问题。由于NATs位于蛋白稳定性、基因调控和细胞应激反应的交汇处,选择性NAT抑制剂——以及或许未来能够精确调整特定疾病相关蛋白氨基端乙酰化的工具——正成为治疗癌症、心脏病和神经退行性疾病的新兴有希望途径。
引用: McTiernan, N., Kjosås, I. & Arnesen, T. Illuminating the impact of N-terminal acetylation: from protein to physiology. Nat Commun 16, 703 (2025). https://doi.org/10.1038/s41467-025-55960-5
关键词: 蛋白质修饰, 氨基端乙酰化, 蛋白质量控制, 神经退行性疾病, 癌症生物学