Clear Sky Science · zh
CRISPR-AuNP:用于成本效益高且模块化的非病毒性HSPC基因编辑的金纳米粒子平台的物化学优化
让基因编辑惠及更多患者
像CRISPR这样的基因编辑工具已经改变了部分遗传性血液病患者的生活,但相关治疗仍然昂贵、技术要求高,并且主要局限于少数专科中心。本文介绍了一种将CRISPR递送到造血干细胞的新方法:使用基于金的微小颗粒,这些颗粒可以在实验台上几小时内混合制备。目标是让强大的基因编辑方法更简便、更便宜,并更容易在全球更多地方推广应用。
为什么造血干细胞很重要
造血干/祖细胞位于骨髓内,不断补充体内各种血细胞类型。如果医生能在这些细胞中安全修复致病突变,一次性治疗即可为镰状细胞病和某些免疫缺陷等疾病提供终生治愈。目前,将CRISPR引入这些细胞的最常见方法是电穿孔,利用电脉冲在细胞膜上打开孔洞。尽管强大,电穿孔对细胞具有较大损伤,需要昂贵设备和专用试剂,也不易规模化或推广到资源有限的地区。较为安全的病毒载体在许多基因治疗中表现出色,但对CRISPR递送不太适合,因为它们会持续表达编辑工具太长时间,从而增加脱靶改变的风险。
构建微小的金属递送载体
研究团队着手改进先前报道的一种将CRISPR组分携带在表面的金纳米粒子系统。在早期设计中,引导CRISPR切割蛋白到靶点的RNA直接锚定在金核上,然后与Cas9蛋白配对。这种方法对某些CRISPR酶效果尚可,但对以Cas9为核心的许多治疗策略表现不佳。通过仔细检查Cas9及其引导RNA在颗粒组装时所用酸性条件下的行为,团队发现引导RNA双链在金表面变得不稳定,导致几乎没有活性Cas9附着在颗粒上。共焦显微镜观察还表明,旨在帮助颗粒从细胞隔室中逸出的聚合物涂层在完成其功能前就被剥落了。
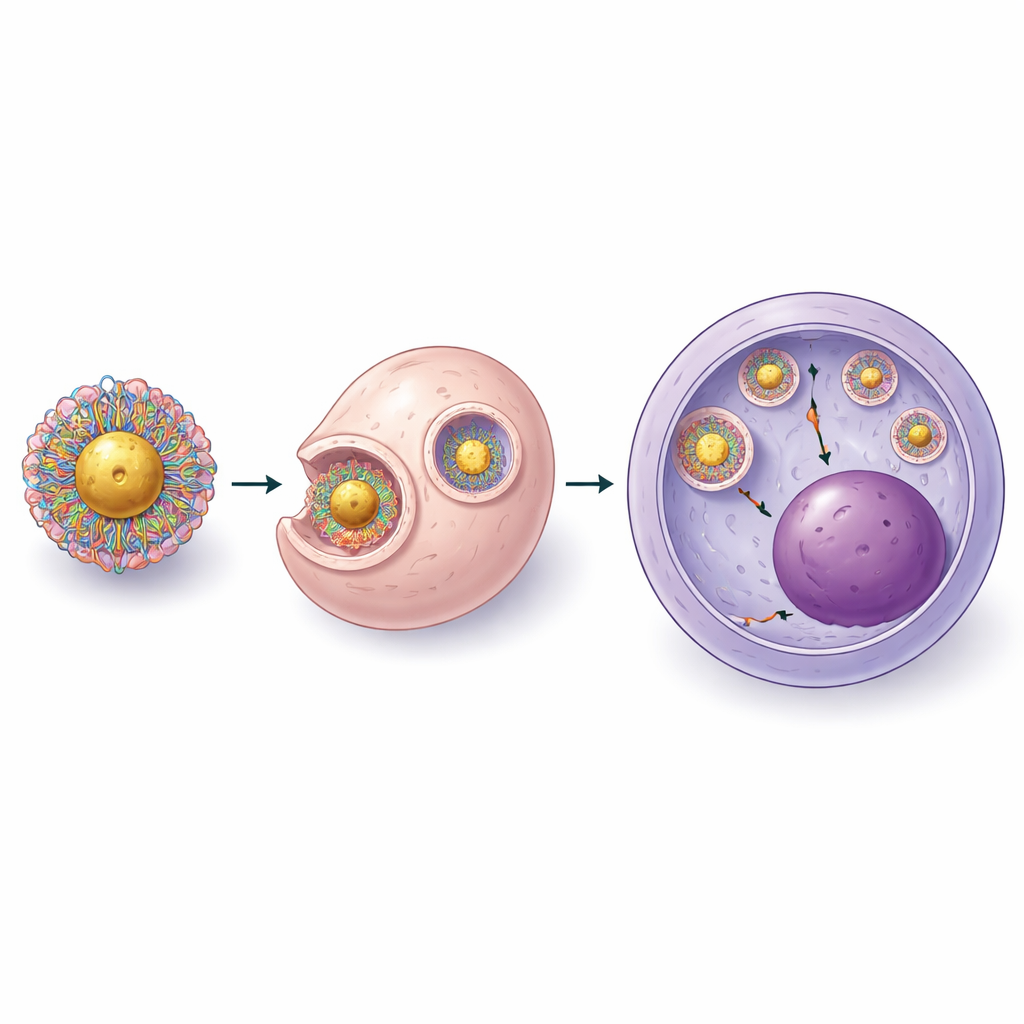
平台的分步重构
为了解决这些问题,科学家们从头分三阶段重建了系统。首先,他们不再把裸RNA锚定到金表面再添加蛋白,而是在与金表面接触之前先组装完整的CRISPR核糖核蛋白复合体(蛋白加引导RNA)。他们确定了一种轻微酸性条件,既允许这些复合体与颗粒结合,又能保持切割蛋白的活性。接着,他们用经特殊设计的聚合物包裹已负载的颗粒,这些聚合物结合了带正电的链(帮助突破细胞隔室)和柔性亲水的聚乙二醇片段(防止团聚)。通过测量颗粒尺寸、表面电荷和蛋白含量,他们证明可以可重复地在每个颗粒上装载数十个CRISPR复合体,同时在溶液中保持稳定性。
攻克细胞防御
即便负载有所改进,第二代颗粒仍然面临关键难题:将CRISPR从细胞内囊泡释放到含有DNA的细胞区室中。为此,团队系统性地调节了聚合物层的化学性质以及聚合物上正电基团与CRISPR复合体负电基团之间的比例。他们发现,增加更多短链聚乙二醇和受控数量的含硫锚定基既改善了颗粒稳定性,又能在不损伤细胞的情况下增强破坏内体膜的能力。在最终的第三代设计中,他们先形成紧凑的CRISPR与聚合物复合体,再将这些复合体连接到浓缩的金核上。电子显微镜显示每个金球周围有一层薄薄的CRISPR-聚合物壳,活体干细胞成像证实货物能够逃逸至细胞内部并到达细胞核。
多种CRISPR工具的编辑结果
为评估优化后颗粒的效能,研究者靶向了名为β2-微球蛋白的基因,该基因编码的蛋白存在于几乎所有血细胞表面,可通过流式细胞术轻松测量。使用第三代金平台,他们在原代人体造血干/祖细胞中实现了超过10%的该基因精确破坏——这一水平对于许多治疗应用被认为具有意义——同时保持了很高的细胞存活率。尽管这一效率低于电穿孔可达到的水平,金基系统不需要专用设备且对细胞的应激最小。重要的是,同一平台可与不同的CRISPR蛋白一起使用,包括Cas9、Cas12a以及一种名为Cas12a-M29-1的新酶,显示出相似的编辑水平且无可检测毒性,突出了设计的模块化特性。
这对未来疗法意味着什么
通俗地说,这项工作表明可以构建一个小巧、精心设计的金基载体,将CRISPR工具在无需电力或病毒、使用现成材料的条件下递送到敏感的造血干细胞,成本低于每百万个细胞七十美元。尽管仍需进一步提高效率以匹配当今最佳临床方法,特别是对于需要极高纠正细胞比例的疾病,这种可以在实验台组装的平台降低了实施复杂基因编辑的实际门槛。通过持续优化和安全性检测,此类纳米粒子有望将CRISPR疗法的益处扩展到专科中心之外,使全球患者更容易获得治愈性治疗。
引用: Gottimukkala, K.S.V., Lane, D.D., Cunningham, R. et al. CRISPR-AuNP: physicochemical optimization of a gold nanoparticle platform for cost-effective and modular non-viral gene editing in HSPCs. Gene Ther 33, 188–202 (2026). https://doi.org/10.1038/s41434-025-00591-0
关键词: CRISPR基因编辑, 金纳米粒子, 造血干细胞, 非病毒递送, 纳米医学