Clear Sky Science · zh
人工伴护分子:从传统设计到智能系统
帮助分子正确折叠
在每一个活细胞内,长链的蛋白质和遗传物质必须弯曲和扭转成恰当的形状才能正常工作。当它们折叠错误时,可能会聚集、丧失功能,甚至触发如神经退行性疾病等病理过程。自然界依靠“伴护”分子来维持这微观秩序,但这些天然帮手成本高、脆弱,且难以在细胞外使用。本文探讨了科学家如何构建人工伴护分子——可诱导走偏分子回到正确构象的工程化帮手,甚至可以像智能工具一样被开关控制。
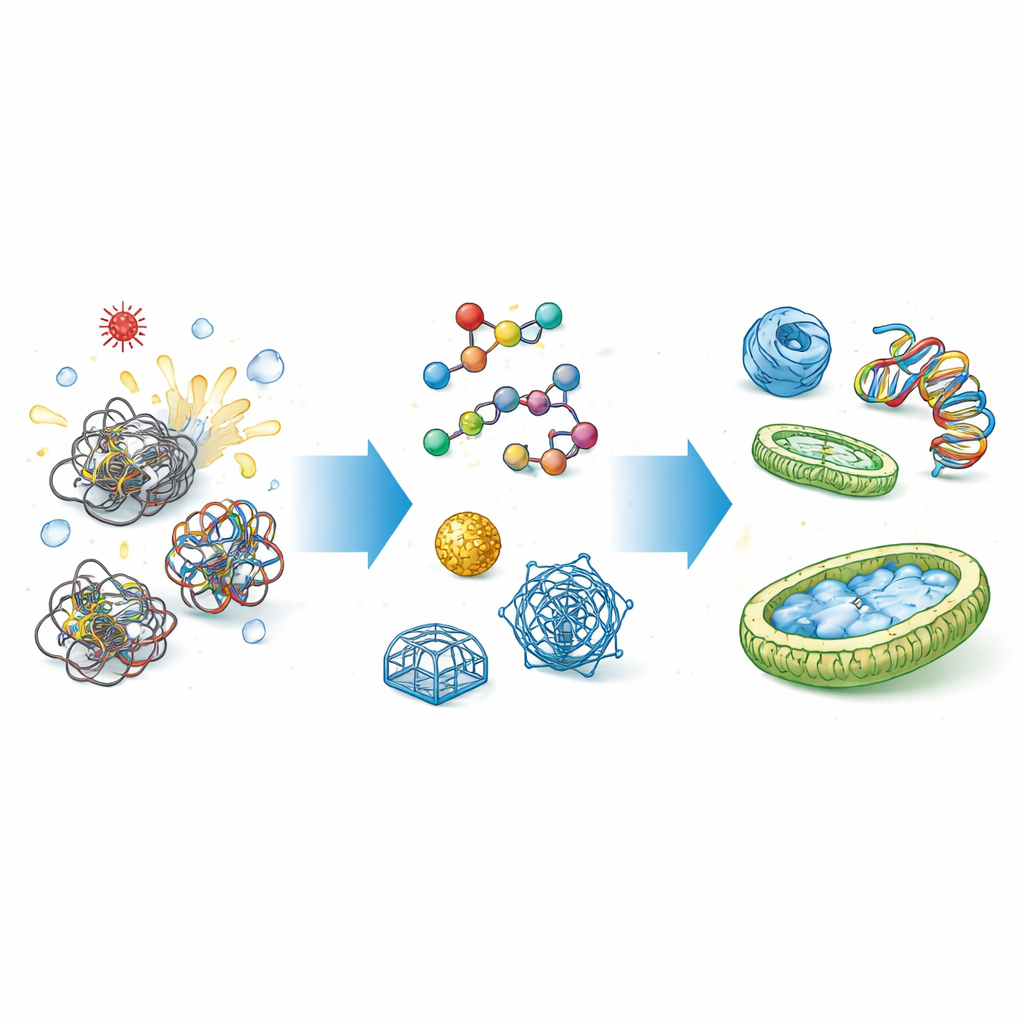
细胞为何需要折叠帮手
蛋白质和核酸(如DNA和RNA)并非天生即具备功能;它们必须折叠为复杂的三维构象。通向这些构象的道路充满陷阱,链条可能卡住或相互粘连。天然伴护分子,例如热休克蛋白,抓住这些柔软的链段,遮蔽其易粘连的区域,并为其提供一个受保护的空间以正确折叠。对于核酸,伴护分子也扮演类似的引导角色,帮助解开结、重排碱基配对。当这种控制失效时,可能导致功能丧失、有毒团块、疾病以及工业蛋白质生产中的代价高昂的失败。
从简单化学物质到定制聚合物
最早的人工伴护分子是相对简单的化学物质,它们改变分子所处环境的性质。某些溶剂和表面活性剂能掩盖蛋白的粘性区域,防止聚集,并给它们二次折叠的机会。例如,一些小分子脂肪酸有助于突变型胶原蛋白更正确折叠,缓解受遗传性疾病影响细胞内的应激。但这些化学帮手通常需要高剂量、难以针对特定靶点精细调控,并可能干扰复杂混合物中的其他成分。为了获得更好的控制,研究者转向更大、可定制的聚合物——可用带电或亲水侧链装饰的柔性链,用以更有选择性地包裹DNA、RNA和蛋白质。
聚合物与纳米凝胶工具箱
定制聚合物可以与DNA带电骨架或蛋白质暴露的斑块结合,平滑能量景观,使这些分子更快、更可靠地找到其优选构象。对于核酸,阳离子(带正电)聚合物可中和链间排斥,加速碱基配对、链交换以及在DNA计算和生物传感器中使用的奇特结构的形成。对于蛋白质,诸如特定形状的聚乙二醇环或合成聚阴离子等聚合物在防止热诱导聚集方面可优于某些天然伴护分子。其他系统将柔性伴护聚合物与短肽配对,重塑类细胞膜为平面纳米片或囊泡,创造可逆的二维平台用于货物递送和组织工程。

构建智能、可开关的伴护分子
除了简单地抓取和释放客户分子外,现代人工伴护分子现在还能对环境做出响应。研究人员已构建出纳米凝胶、纳米颗粒和聚合物网络,其对蛋白质的握持力会随酸碱度、温度、光或特定化学物质(如葡萄糖)的变化而收紧或放松。例如,一些胶束在轻度酸性pH下变得更疏水,模仿天然伴护分子捕获受威胁蛋白,然后在pH再次变化时释放它们。温度响应性聚合物在穿过阈值时会塌缩或膨胀,使其在一种温度下隔离受损蛋白,在另一种温度下释放已经重折叠的蛋白。光敏基团可作为分子开关,用闪光开启或关闭DNA组装通路,而糖响应性颗粒可在血糖升高时优先释放并保护治疗性激素。
这对医学与技术意味着什么
文章总结道,人工伴护分子正在从简单的化学稳定剂演变为高度可编程的“分子工具”,能够按需识别、保护并重塑多种生物结构。通过精心平衡吸引与排斥力,并将对pH、热、光或机械应力等信号的敏感性接入系统,这些材料能在合适的时间与地点折叠目标分子。从长远看,这类智能帮手有望提高工业蛋白质生产效率、提升生物传感器性能、推动分子计算,并提供新的手段来应对与错误折叠蛋白相关的疾病——可能包括阿尔茨海默病等状况——同时密切模仿活细胞已实现的微妙控制。
引用: Zhang, W., Maruyama, A. Artificial chaperones: from conventional designs to smart systems. NPG Asia Mater 18, 12 (2026). https://doi.org/10.1038/s41427-026-00640-z
关键词: 人工伴护分子, 蛋白质折叠, 智能聚合物, 纳米医学, 刺激响应材料