Clear Sky Science · zh
溶瘤病毒 M1 通过脾脏中依赖 B 细胞的抗原交叉呈递重振对胶质母细胞瘤的 CD8+ T 细胞免疫
重新激活免疫系统
胶质母细胞瘤是最致命的大脑癌症之一,部分原因在于它极为擅长关闭机体防御。本研究探索了一种通过静脉输注的专门设计病毒,将这种防御再次激活的途径:该病毒既直接攻击肿瘤细胞,又动员免疫细胞对抗癌症。研究揭示了一个意外的关键角色:脾脏中的免疫细胞在唤醒杀伤性 T 细胞方面发挥了重要作用。
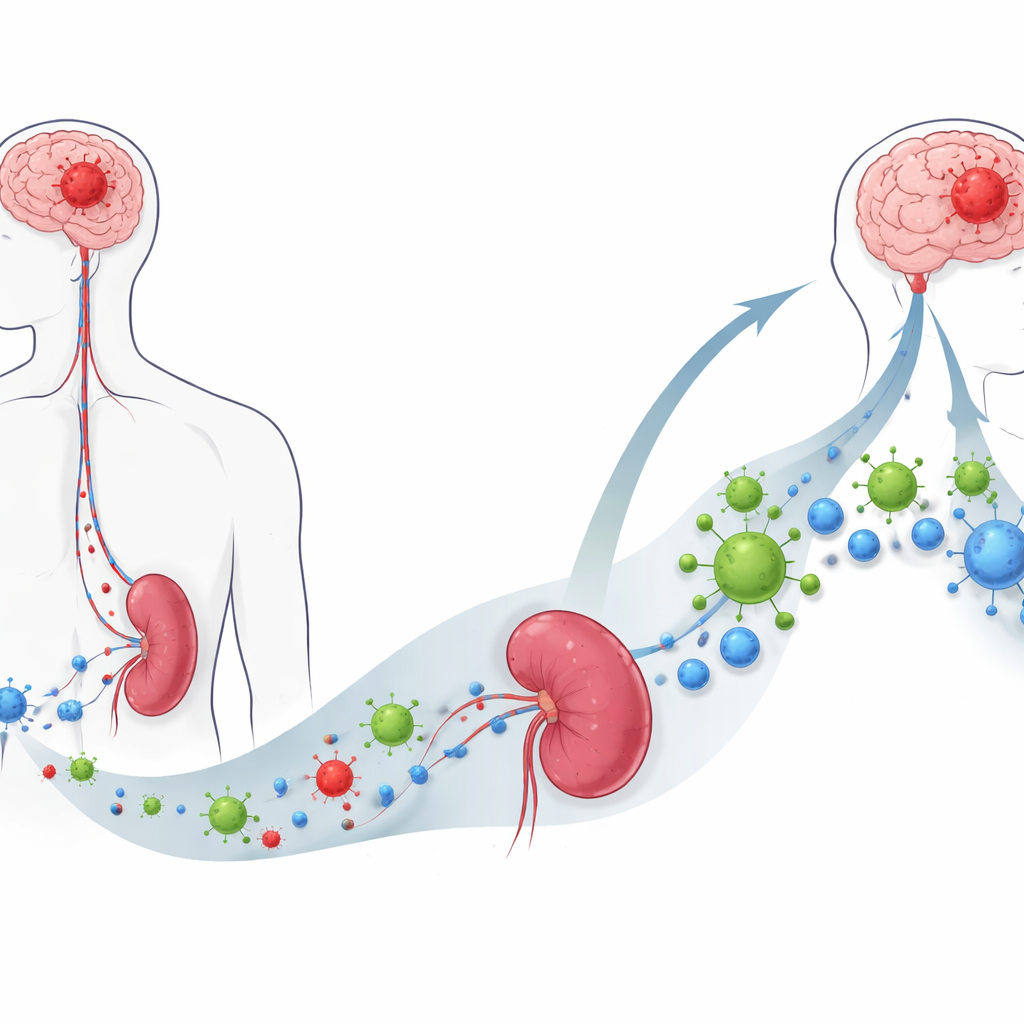
偏好感染癌细胞的病毒
研究人员研究了一种实验性疗法,称为溶瘤病毒 M1(OVM),这是一种改造过的阿尔法病毒,偏好感染并杀死癌细胞而尽量不损伤正常组织。在体外培养中,OVM 高效侵入多种小鼠和人类胶质母细胞瘤细胞系,并诱导一种伴随分子“危险信号”的细胞死亡形式。在对新鲜切除的人类肿瘤碎片进行测试时,OVM 在胶质母细胞瘤组织中强烈复制,而在邻近的非肿瘤脑组织中则不显著复制,这表明其比标准化疗更能区分恶性与健康细胞,后者会同时损伤两者。
逆转全身性免疫失能
除了脑内局部影响,胶质母细胞瘤还导致广泛的免疫崩溃:患者和小鼠模型表现为脾脏萎缩及循环 T 细胞显著减少。在肿瘤负荷小鼠中静脉注射 OVM 后,这一情形发生了明显改变。脾脏恢复了体积,血液中 CD4 和 CD8 T 细胞水平回升,免疫抑制性分子如 IL-10 和 TGF-β 降低。在肿瘤部位,更多 T 细胞——尤其识别示范性肿瘤抗原的 CD8“杀伤”T 细胞——进入到脑内,使先前“冷”的肿瘤环境转变为充满免疫战士的区域。
脾脏为何重要
令人意外的是,脾脏对 OVM 的疗效至关重要。切除脾脏后,病毒不再能减缓肿瘤生长或延长存活期,血液和脑内 T 细胞激增也大多消失。对脾脏免疫细胞的单细胞 RNA 测序显示,OVM 处理后脾脏中的 B 细胞与 T 细胞之间形成了特别强的通信网络。在体外培养中,来自 OVM 处理小鼠的 B 细胞相比未处理动物的 B 细胞能更有效地促使 CD8 T 细胞增殖和激活,而树突状细胞并未表现出相同的增强,提示 B 细胞是关键中介。
能激活肿瘤杀手的特殊 B 细胞
深入研究发现,一类以表面分子 Bst2 为标志的特殊 B 细胞亚群在 OVM 处理后在脾脏中扩增。这些 Bst2 阳性 B 细胞富集有参与摄取肿瘤物质、细胞内加工及以可被 CD8 T 细胞识别的形式在表面呈递片段的基因。实验证明,这些细胞更高效地捕获肿瘤抗原,与 CD8 T 细胞形成紧密接触区,并且激活 T 细胞需要直接的细胞—细胞接触和特定的蛋白加工通路。当将纯化的 Bst2 阳性 B 细胞转入 B 细胞缺陷且带有脑肿瘤的小鼠时,它们显著延长了存活期,而其他 B 细胞类型则没有这种效果。
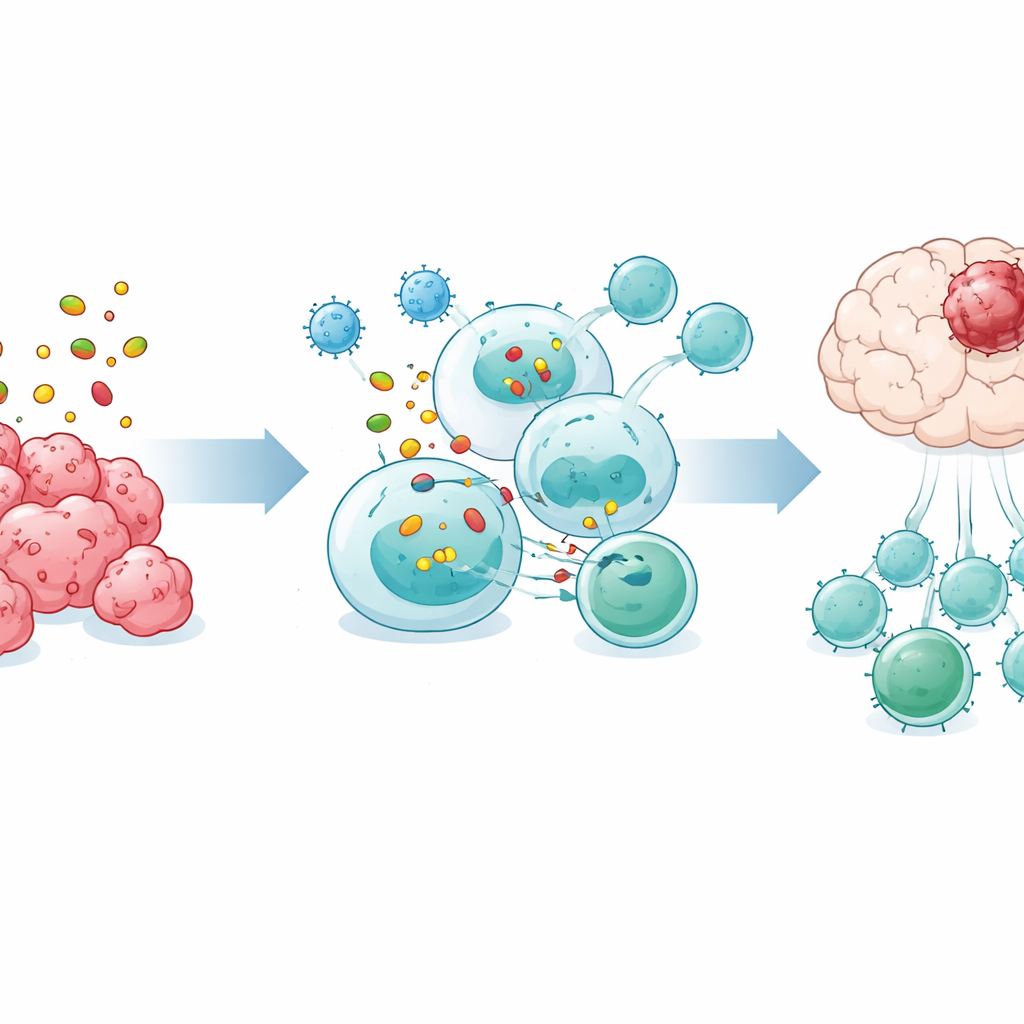
当今主流的免疫疗法——阻断 PD-1 或 PD-L1 的检查点抑制剂——在胶质母细胞瘤中效果令人失望。在此使用的鼠模型中,单用 PD-1 或 PD-L1 抗体收效甚微。然而,将 OVM 与 PD-1 阻断抗体联合使用显著增加了脑内肿瘤中的 CD8 T 细胞数量,使循环 T 细胞由幼稚状态转向激活状态,恢复了脾脏体积并延长了存活期。OVM 治疗还提升了肿瘤浸润 CD8 T 细胞上的 PD-1 水平,使其更易被 PD-1 阻断所拯救。
这对患者可能意味着什么
综上所述,这项工作表明,静脉输注的溶瘤病毒不仅能感染并裂解胶质母细胞瘤细胞。通过招募脾脏中一类专门的 B 细胞来处理肿瘤物质并将其呈递给 CD8 T 细胞,OVM 重建了全身免疫并驱动杀伤性 T 细胞重返脑内攻击肿瘤。在前临床模型中,这一策略不仅单独抑制肿瘤生长,还能使耐药的脑肿瘤对 PD-1 检查点疗法产生反应。如果这些发现可转化到人体,OVM 与 Bst2 阳性 B 细胞可能成为新型联合疗法乃至个性化疫苗的核心,最终让免疫系统在对抗胶质母细胞瘤时重新获得机会。
引用: Han, Y., Guo, C., Chen, C. et al. Oncolytic virus M1 reinvigorates CD8+ T-cell immunity against glioblastoma through B-cell-dependent antigen cross-presentation in the spleen. Cell Mol Immunol 23, 349–366 (2026). https://doi.org/10.1038/s41423-026-01396-w
关键词: 胶质母细胞瘤, 溶瘤病毒, 肿瘤免疫学, B 细胞, 免疫检查点疗法