Clear Sky Science · zh
应对铜毒性:从代谢重编程到肿瘤治疗利用
当一种有益金属反过来对抗癌症时
铜最为人所知的是电线和管道的组成材料,但它也在细胞内静静运行,帮助酶产生能量并保护我们免受损伤。本文综述探讨了一个令人意外的转折:在特定条件下,过量的铜会将癌细胞推向一种特殊的死亡方式。理解这一过程——称为“铜毒性”(cuproptosis)——可能为治疗已躲过常规疗法的肿瘤打开新的途径。
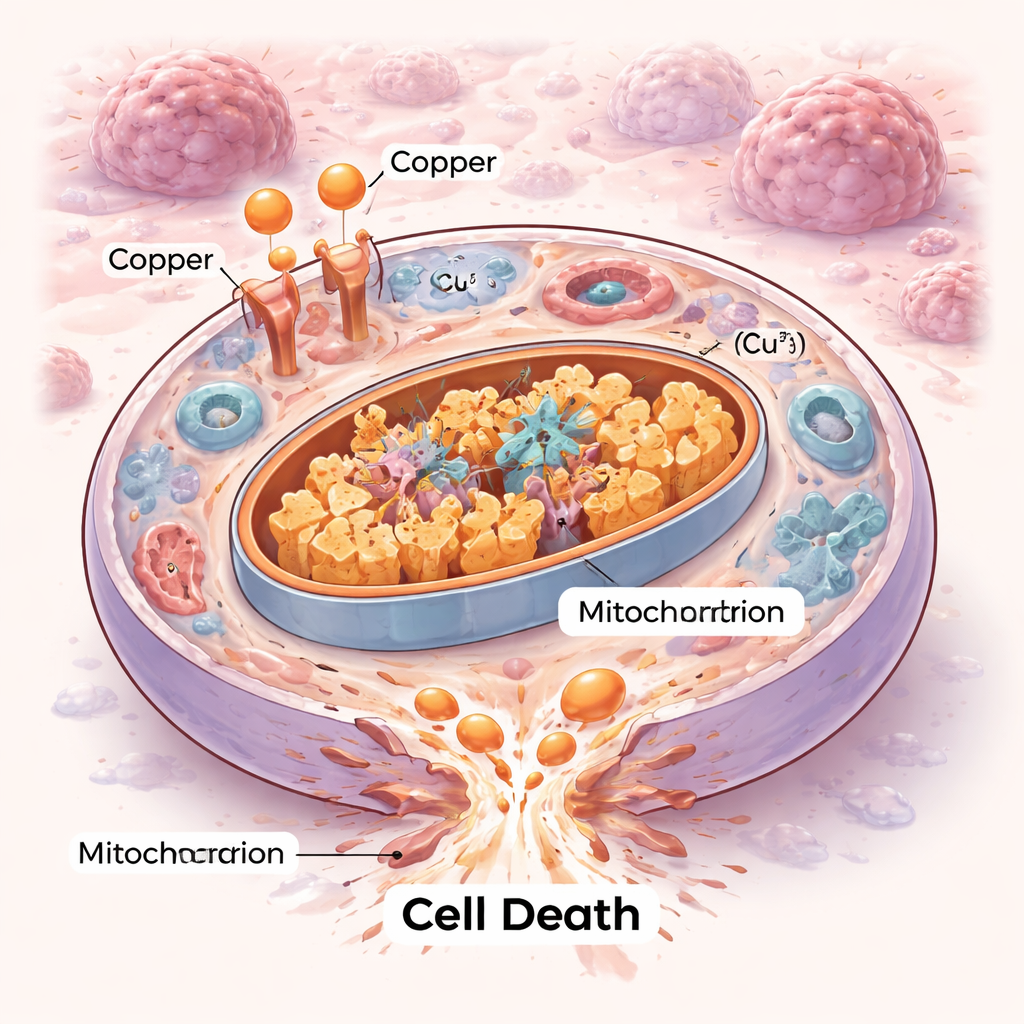
细胞死亡的一种新方式
细胞并非都以相同方式死亡。几十年来,科学家们绘制了程序性自我毁灭通路如凋亡,以及更新发现的形式如铁死亡。铜毒性为这一体系增添了新篇章。在这一过程中,过量铜淹没细胞的“能量站”——线粒体,并与通常参与燃料氧化的特定代谢酶结合。这种结合导致这些酶发生聚集,并破坏线粒体所需的小型铁‑硫簇组件。结果是一种内部“交通堵塞”和机械性崩溃,细胞无法修复,最终因蛋白毒性压力而死亡,而非经典的自杀式通路。
癌细胞如何控制铜与能量
因为铜既必需又有害,细胞维持着复杂的物流网络以安全转运铜。专门的转运蛋白将铜带入细胞,护送蛋白将其引至线粒体和其他去处,金属硫蛋白和谷胱甘肽等储存分子则清除多余铜。肿瘤往往重编程这一系统:一些肿瘤提升进口蛋白或护送蛋白以满足高能需求;另一些则增加输出或储存蛋白以避免铜过载。同时,许多癌症改变代谢——在表层的糖代谢与更深入的线粒体呼吸之间切换。综述指出,铜毒性最容易攻击依赖线粒体的细胞,因此具有这一代谢特征的肿瘤尤其脆弱。
调节铜敏感性的主控开关
一些主要的细胞“决策者”会影响铜毒性是否发生。例如,抑瘤蛋白p53倾向于将细胞从快速的糖酵解推向更有序的线粒体燃料利用。通过这样做并改变铜结合酶的处理方式,p53可使癌细胞更易受铜诱导的死亡——而p53的突变形式常常产生相反效果。相反,缺氧诱导因子HIF‑1α在缺氧的肿瘤核心被激活,它通过下调关键线粒体酶并增强铜结合屏障,帮助细胞逃避铜毒性。其他通路,如Wnt/β‑catenin和AKT,通过促进铜外排或化学修饰关键蛋白使其不再响应铜过载,从而推动耐受性。这些网络共同像恒温器一样,上调或下调肿瘤对铜基治疗的敏感性。
铜、免疫系统与更智能的药物递送
铜的作用不仅限于直接杀死癌细胞;它还塑造肿瘤周围的免疫格局。可控的铜应激可使濒死的癌细胞更“可见”,释放危险信号以招募并激活T细胞、树突状细胞和巨噬细胞。铜还可影响诸如PD‑L1等免疫检查点的水平,肿瘤通过这些检查点关闭抗癌T细胞,这提示可以将铜靶向药物与现代免疫疗法联合使用。由于游离铜可能损害健康组织,研究者正在构建精确工具——小分子离子载体选择性地将铜护送入癌细胞,以及将铜或铜驱动药物装入靶向颗粒或水凝胶的纳米医学平台。这些技术旨在将铜提升到肿瘤内的致死水平,同时将全身保持在安全范围内。
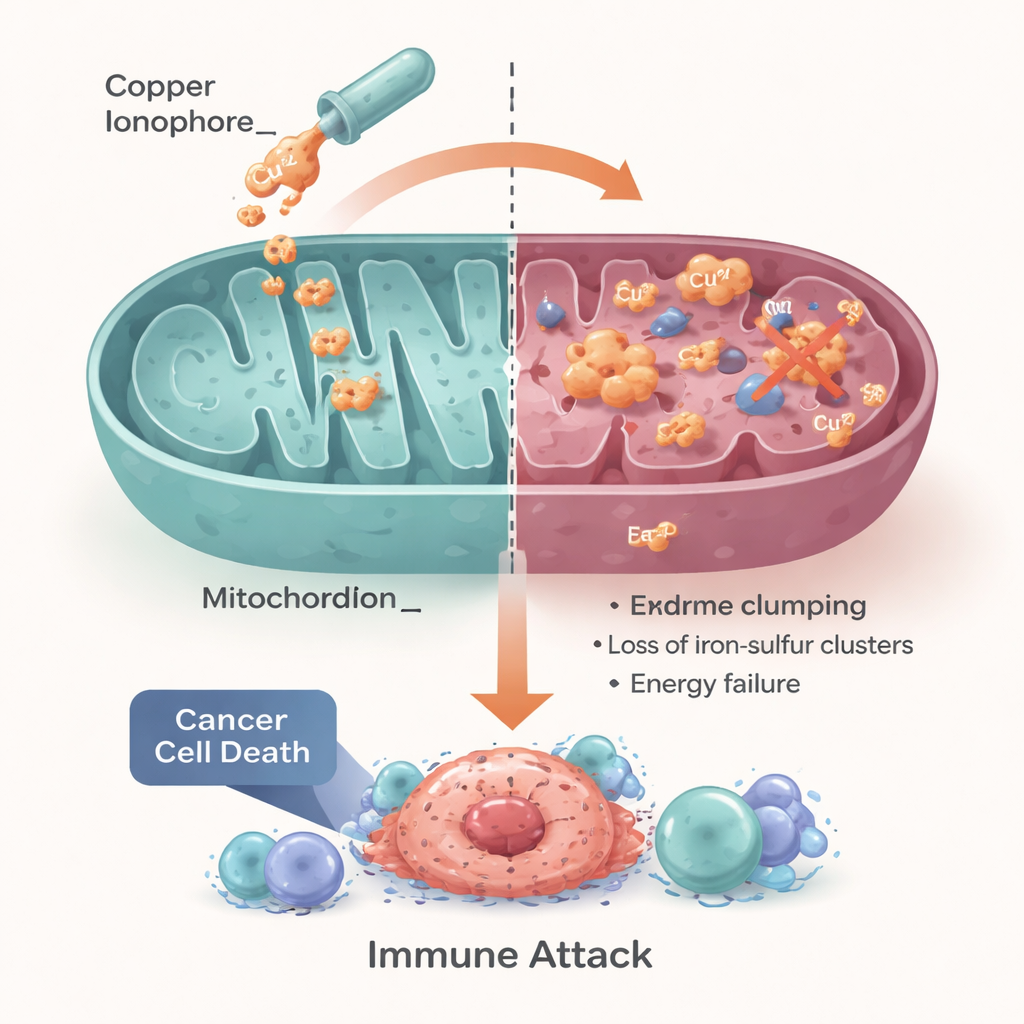
将细胞弱点转化为治疗策略
作者总结认为,铜毒性将一种基本的细胞需求——对铜与能量的精细管理——转变为癌症的潜在阿基里斯之踵。铜处理紊乱或过度依赖线粒体代谢的癌症可能对基于铜的策略特别敏感,包括重新定位的药物如双硫仑和依来曲唑(elesclomol),以及新一代纳米颗粒。然而,他们强调成功将取决于将合适的患者与合适的方法匹配,使用报告铜转运蛋白、线粒体活性以及肿瘤免疫与氧合状态的生物标志物。如果这些障碍能够被克服,利用铜毒性可能为肿瘤学家提供一种新的、金属驱动的手段,用以治疗当前选项有限的肿瘤。
引用: Hao, Q., Gan, Y. & Zhou, X. Tackling cuproptosis: from metabolic rewiring to therapeutic exploitation in cancer. Cell Mol Immunol 23, 239–260 (2026). https://doi.org/10.1038/s41423-026-01387-x
关键词: 铜毒性, 铜代谢, 癌症治疗, 肿瘤代谢, 癌症免疫疗法